人被蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,引起刺痛.蚁酸学名叫甲酸,它的化学式是HCOOH.请回答下列问题:
(1)甲酸属于 (填"氧化物"、"无机化合物"或"有机化合物").
(2)甲酸的相对分子质量是 .
(3)甲酸中碳、氢、氧三种元素质量比是 (最简整数比).
炒菜时加一点酒和醋能使菜味香可口,原因是有脂类物质生成。下列有关乙酸乙酯的叙述正确的是( )

| A. |
乙酸乙酯是由碳、氢、氧元素组成的有机物 |
B. |
乙酸乙酯由碳、氢、氧原子构成 |
| C. |
乙酸乙酯中碳、氧元素的质量比为2:1 |
D. |
乙酸乙酯中氧元素的质量分数最大 |
"冰毒"是毒性极强的毒品之一,其化学式为C 10H 15N,下列有关冰毒解释错误的是( )
| A. |
冰毒是由碳、氢、氮三种元素组成的化合物 |
B. |
冰毒是一种有机物,完全燃烧只生成CO 2和H 2O |
| C. |
冰毒中氮原子的原子结构示意图为 |
D. |
冰毒中碳、氢两种元素质量比为24:3 |
已知柠檬酸的化学式为C 6H 8O 7.请回答:
(1)柠檬酸中碳、氢、氧三种元素的原子个数比是 ;
(2)柠檬酸中碳、氧元素的质量比为 。
质量守恒定律的发现,对化学的发展做出了重要贡献。

(1)通过分别称量下列两组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是 (填标号)a.大理石和稀盐酸 b.NaOH溶液和Na 2SO 4溶液
(2)在足量氧气中点燃镁条的实验过程中,固体质量变化如图一。
①从燃烧条件分析,固体质量在t 1前没有发生变化的原因是
②该反应的化学方程式为
③参加反应的氧气质量为 g
(3)在一定条件下,A和B反应生成C,微观示意图如图二。回答下列问题:
①一个A分子由 个原子构成
②C分子中原子的质量比N:O=
③该反应的化学基本反应类型为
④上述反应中一定发生改变的是 (填标号)
a.元素种类 b.原子种类 c.分子种类
一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二甲苯烷二异氰酸酯(其分子式为C15H10N2O2)。请回答下列有关问题:
①二甲苯烷二异氰酸酯是 (填“有机物”或“无机物”)。
②二甲苯烷二异氰酸酯中氢、氧两元素的质量比为 (填最简整数比)。
日常生活中食用的白糖的主要成分是蔗糖(化学式为C 12H 22O 11),请计算:
(1)蔗糖分子中C、H、O三种原子的个数比为 ;
(2)蔗糖中H、O元素的质量比为 。
淀粉〔(C 6H 10O 5) n〕是人们食用的最主要糖类,许多谷物和植物块茎富含淀粉.
(1)淀粉中氢、氧元素质量比为 (填最简比).
(2)81g淀粉中碳元素的质量是 g.
生活离不开化学.
(1)豆浆已成为众多家庭喜爱的饮品,下表是豆浆中部分营养成分的平均质量分数,请根据下表回答问题:
| 成分 |
蛋白质 |
油脂 |
糖类 |
钙 |
铁 |
维生素 |
| 质量分数/% |
1.8 |
0.7 |
1.1 |
0.01 |
0.0005 |
0.015 |
①豆浆中含有人体所需的微量元素是 ,青少年因缺 而导致佝偻病.
②豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是 .
(2)下列食品中富含油脂的是 .
A、豆腐 B、花生 C、面包 D、草莓
(3)香烟燃烧产生的烟气中含有尼古丁(化学式为C 10H 14N 2)、焦油和CO等有害物质,其中尼古丁属于 (填"有机物"或"无机物"),尼古丁中C、N两种元素的质量比为 .
(4)胃酸过多的病人,其胃液的pH较正常人的要 (填"大"或"小"),服用含氢氧化铝的药物后可使病人恢复正常,原因是 (用化学方程式表示).
将100g氯化钾样品(含有碳酸钾杂质)加入到50g盐酸中,样品完全反应,产生的气体全部逸出,并测得反应后的溶液总质量为145.6g。请计算:
(1)K 2CO 3中K、C、O元素的质量比为 。
(2)产生气体的质量为 g;
(3)样品中氯化钾的质量分数。(写出计算过程,最后结果精确到0.1%)
2015年10月5日,中国籍科学家屠呦呦因发现治疗疟疾的新药物疗法而获得诺贝尔奖,青蒿素(化学式为C 15H 22O 5)是一种用于治疗疟疾的药物。青蒿素的发现挽救了全球特别是发展中国家数百万人的生命。
(1)青蒿素的相对分子质量是 。
(2)青蒿素中碳、氧元素的质量比为 。(填最简比)
醇厚鲜香的沙蟹汁是北海特产。请回答下列问题:
(1)腌制沙蟹汁时需要加入碘盐和白酒,碘盐就是在食盐中加入 。
白酒的主要成分是乙醇(C 2H 5OH),乙醇中碳元素和氧元素的质量之比为 。
(2)沙蟹汁有多钟氨基酸,但含人体生命活动所需能量主要来源的 类营养素少,所以不能作为主食。
(3)沙蟹汁可用陶罐贮存,陶罐属于 (填"无机非金属""复合"或"有机合成")材料;外包装使用的聚乙烯塑料袋不能随意丢弃,避免造成" 污染"。
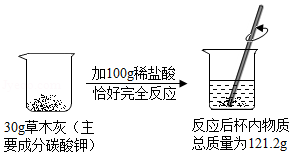
草木灰是农家肥料,其主要成分是碳酸钾,某化学兴趣小组进行如图实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出)。请你回答下列问题:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为 ;
(2)反应后生成的气体质量为 g;
(3)稀盐酸中溶质质量分数是多少?
阅读下列材料,按要求回答问题。
2020年新冠肺炎在全球爆发,给人们生命健康带来严重威胁。为了有效预防新冠病毒的传播,国家卫健委提出一系列措施进行防护。
(1)勤洗手,洗手液配方及生产工艺如表所示。
| 原料 |
重量(斤) |
生产工艺 |
| AES﹣A |
5 |
1.将AES﹣A和6501混合搅拌均匀,再倒入装有60斤70℃左右水的容器内,搅拌至完全溶解 2.加入丙三醇、色素、香精、卡松搅拌均匀 3.用饱和氯化钠溶液调至最佳粘稠度,不足百斤加水补足 |
| 6501 |
1 |
|
| 丙三醇 |
2 |
|
| 色素 |
适量 |
|
| 卡松 |
0.1 |
|
| 香精 |
0.05 |
|
| 氯化钠 |
约3.5 |
(2)常消毒:84消毒液各种浓度配制方法(原液浓度5%)如表所示。
| |
物表、物品、地面 |
室内地面、空气、物表 |
分泌物、排泄物、污水 |
便器 |
| 配制浓度(mg/L) |
250﹣500 |
1000﹣2000 |
2500﹣3000 |
4000﹣5000 |
| 欲配制体积(mL) |
1000 |
1000 |
1000 |
1000 |
| 84原液用量(mL) |
5﹣10 |
20﹣40 |
50﹣60 |
80﹣100 |
| 用水量(mL) |
995﹣990 |
980﹣960 |
950﹣940 |
920﹣900 |
(3)戴口罩:熔布是口罩最核心的材料,制造熔喷布以聚丙烯为主要原料,空隙多、结构蓬松、抗褶皱能力好,具有独特的毛细结构,从而使熔喷布具有很好的过滤性、屏蔽性、绝热性和吸油性。可用于空气、液体过滤材料、口罩材料、吸油材料及擦拭布等领城。请回答下列问题:
(1)洗手液的主要原料之一丙三醇的化学式为C 3H 8O 3,则丙三醇分子中各原子的个数比为C:H:O= ;丙三醇中各元素的质量比为C:H:O= 。
(2)欲配制用于物表、物品、地面消毒用84消毒液1000mL,需要用到的仪器是 (填序号)。
| A. |
10mL量筒 |
| B. |
100mL量筒 |
| C. |
500mL烧杯 |
| D. |
1000mL烧杯 |
| E. |
玻璃棒 |
| F. |
药匙 |
(3)制造熔喷布的主要原料是 ,它属于 (填"塑料"、"合成纤维"或"合成橡胶");熔喷布具有的特性是: 。