下列各组物质,不能按照关系图(“→”表示反应一步完成)相互转化的是( )
选项 |
物质 |
||
x |
y |
z |
|
A |
Mg(NO3)2 |
Mg(OH)2 |
MgSO4 |
B |
K2SO4 |
KCl |
KNO3 |
C |
BaCl2 |
Ba(NO3)2 |
BaCO3 |
D |
CaO |
CaCl2 |
CaCO3 |
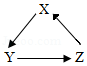
A.AB.BC.CD.D
如图是某化工企业利用“侯氏制碱法”生产纯碱的部分工艺流程示意图:
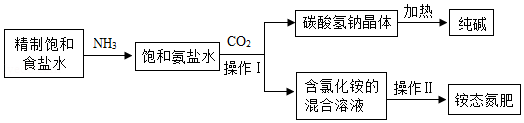
查阅资料知:①NH4Cl NH3↑+HCl↑;②氨气极易溶于水,氨水呈碱性。
(1)检验食盐水是否饱和的方法是 。
(2)操作Ⅰ的名称是 。实验室进行此操作时,玻璃棒的作用是 。
(3)“侯氏制碱法”中,向饱和氨盐水中通入足量的CO2,使氨气、水、NaCl和CO2反应生成NaHCO3等,该反应的化学方程式为 ;先通氨气形成饱和氨盐水,后加压通入二氧化碳,这样操作的目的是 。
(4)处理含氯化铵混合溶液时,不直接加热蒸干得到氯化铵固体的原因是 。
海水是一种重要资源,利用海水可制取镁等物质,某化学兴趣小组的同学设计了如下实验流程进行实验:
分析该流程图,下列说法错误的是( )
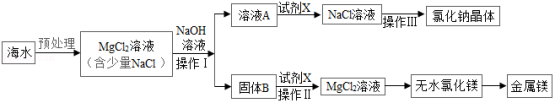
A.操作Ⅰ,操作Ⅲ都需用到的玻璃仪器是玻璃棒
B.固体B是Mg(OH. 2,试剂X是盐酸
C.加入NaOH溶液应过量,其目的是使MgCl 2完全反应
D.处理等量海水,若将NaOH溶液换成石灰乳,既能节约成本又能提高镁的产量
在给定条件下,下列物质间的转化能一步实现的是( )
A.Cu CuSO4溶液
B.CO CO2
C.KClO3 O2
D.Fe2O3 FeCl2溶液
我国煤炭资源丰富,目前人们除了将煤作为燃料外,更是重要的化工原料。工业上以煤和空气为原料生产尿素[CO(NH2)2]的一种流程如图:
(1)从液态空气中分离出N2的过程属于 (填“物理”或“化学”)变化。
(2)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是 。
(3)水煤气在铜催化下实现CO的转化:CO+H2O CO2+X,其中X的化学式为 。
(4)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为 。
(5)实际生产中,N2和H2不可能全部化为NH3.上述流程中可以循环利用的物质有 。
(6)以CO2和H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为:
2CO2+6H2 C2H6O+3H2O.已知:每克燃料完全燃烧数出的热量叫做热值
物质 |
煤 |
乙醇 |
热值/kJ•g﹣1 |
约33 |
30 |
若将含12g碳的煤为原料合成的乙醇完全燃烧,理论上最多可放出 kJ的热量,从而提高了煤的利用效率。
实验室以一种工业废渣(主要成分为MgCO3、MgO和SiO2)为原料制备MgCO3•3H2O.其主要实验过程如图:

已知:SiO2不溶于水,常温下不与硫酸、碳酸钠反应。
(1)“酸溶”时发生反应的化学方程式为 和 。
(2)“过滤Ⅱ”所得滤液中含有的主要离子有 (填离子符号)。
(3)“反应”步骤前后均有过滤,能否省去“过滤Ⅰ”只进行“过滤Ⅱ”。 (填“能”或“否”),理由是 。
(4)“酸溶”时所加硫酸溶液不宜过量太多的原因是 。
无水氯化钙(CaCl 2)是重要的干燥剂,CaCl 2•6H 2O与冰的混合物是实验室常用的制冷剂,将CaCl 2•6H 2O加热可得CaCl 2.某工厂以石灰石为原料生产无水氯化钙的流程如图所示,原料石灰石中含有的杂质主要是MgCO 3、MgSO 4。

(1)过滤和蒸发均用到的玻璃仪器是 。
(2)石灰石溶解时,杂质MgCO 3发生反应的化学方程式为 ,该反应是 (填基本反应类型)
(3)加入BaCl 2溶液除去的杂质离子是 ,加入氢氧化钙溶液除杂的化学方程式为 。
(4)由CaCl 2•6H 2O得到CaCl 2是 变化(填"物理"或"化学")。
自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀请你参与并完成相关内容。
(1)第一站:初识金属镁。①金属镁的物理性质: (写一条);②金属镁的化学性质:镁能与氧气反应,反应的化学方程式为 。
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是 ,化学方程式为 。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如下:
苦卤 Mg(OH)2 MgCl2 Mg,流程中X为 。
(4)第四站:再探金属镁。
[提出问题]镁能否与热水反应?如果反应,产物是什么?
[相关信息]①Mg+2H2O=Mg(OH)2+H2↑;②氢氧化镁在热水中能部分溶解。
实验操作 |
实验现象 |
实验结论 |
① ② |
① ② |
镁能与热水反应,生成氢氧化镁和氢气 |
(5)上述寻镁之旅中你收获到镁的化学性质有 。
海洋是人类宝贵的自然资源,海水“制盐”体现了人类利用化学科学征服和改造自然的智慧。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl2、CaC12等),工业上以粗盐为原料制取精盐,其生产流程如图所示
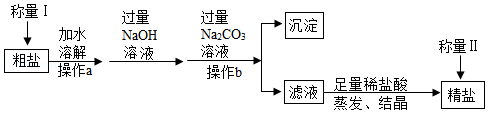
请回答下列问题:
(1)操作b中玻璃棒的作用是 。
(2)加入Na2CO3溶液除去的离子是 (填离子符号),加入NaOH溶液发生反应的化学方程式为 ;
(3)滤液中溶质的主要成分是 (填化学式),加入足量稀盐酸的目的是 。
(4)如果称量Ⅰ中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是 (填字母)
A.精盐的产率为103.3%
B.蒸发操作中可能有水分没有蒸干
C.除杂过程中有NaCl生成
D.溶解操作中粗盐没有完全溶解
以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的工艺流程如图
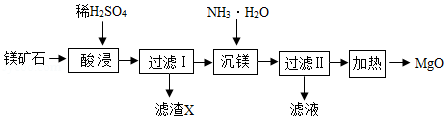
注:SiO2难溶于水和常见的酸;“沉镁”过程中有Mg(OH)2生成。
(1)滤渣X的主要成分为 (填化学式)。
(2)实验室中用图一所示装置进行过滤。
①该装置中仪器A的名称为 。
②若过滤时滤液出现浑浊,可能的原因是 (填字母)。
a.滤纸已破损 b.漏斗中液面低于滤纸边缘 c.滤纸未紧贴漏斗内壁
(3)“沉镁”时MgSO4与NH3•H2O发生反应。结合图二,写出该反应的化学方程式 。
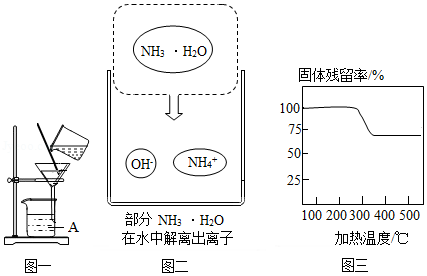
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如题图三所示。“加热”时温度至少要达到350℃,原因是 。
绘制知识网络是化学学习的一种有效方法,元素单质及其化合物的“价态—类别”二维图就是其中的网络图之一。如图是铁及其化合物的“价态—类别”二维图,下列有关说法或方程式正确的是( )
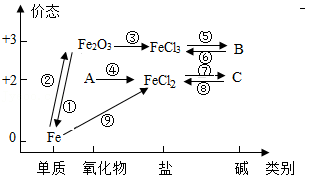
A.物质A的名称是氧化铁
B.①反应可能是Fe2O3+3Al 3AlO+2Fe
3AlO+2Fe
C.⑤反应可能是FeCl3+3NaOH═Fe(OH)3↓+3NaCl
D.⑤~⑨全部是复分解反应
某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)
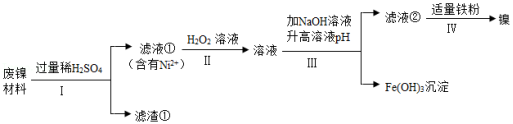
查阅资料:a.H 2O 2溶液可将Fe 2+转化为Fe 3+。
b.Fe 3+、Ni 2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni 2+、无Fe 3+,则滤液②pH可能为 (填序号)。
A.pH=1
B.pH=2
C.pH=6
D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
2021年6月8日是第13个“世界海洋日”。烟台有漫长的海岸线,蕴藏着丰富的海洋资源。某兴趣小组设计的综合利用海水的部分流程图如图。据如图回答:
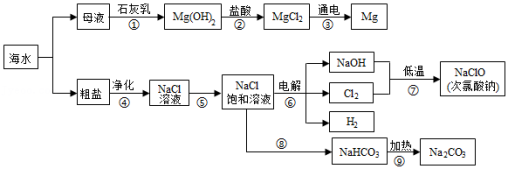
(1)海水制镁,步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是 。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。
(2)海水晒盐。通常采用 (填“降温”或“蒸发”)结晶的方法使海水中的氯化钠析出。通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是 。
(3)海水制碱。步骤⑧⑨是氨碱法制纯碱的流程,步骤⑧中需要向NaCl饱和溶液中先后加入的两种物质是 (写化学式)。步骤⑨中发生反应的化学方程式是 。
(4)步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是 。
(5)步骤⑦用烧碱低温制取次氯酸钠的反应原理为:Cl2+2NaOH═X+NaClO+H2O,则X的化学式是 。
无水氯化钙在工业上有广泛的用途。以石灰石矿粉(含有SiO 2、Fe 2O 3、MgSO 4等杂质)为原料,生产无水氯化钙的流程如图:
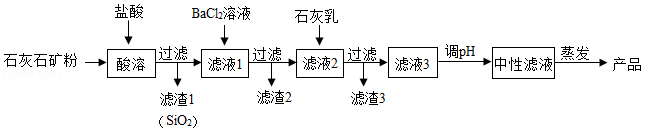
回答下列问题:
(1)从流程图中推知:SiO 2具有的化学性质是 。
(2)氧化铁与盐酸反应的化学方程式为 。
(3)滤渣3中除有Ca(OH) 2外,还有 (填化学式,下同)。
(4)产品中的杂质除极少量H 2O外,最有可能含的是 。