汽车给人们的生活带来方便的同时,也带来节能和减排的问题。如图是某种汽车的燃料燃烧过程示意图
(1)从燃烧的条件看,火花塞的作用是 。
(2)将汽油与空气的混合气充分压缩,有助于节省燃料,说明主要原因。
(3)乙醇的含碳量比汽油的低。分析在汽油中加入适量乙醇,对尾气中炭黑排放量的影响。
(4)利用催化净化装置,可使燃烧过程中产生的CO和NO在催化剂的作用下,转化为两种空气中常见的无害气体,该反应的化学方程式为 。
从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:
(1)反应池I中用硝酸不用稀硫酸的主要原因是 。
(2)反应池Ⅱ中加入氨水的目的是 。
(3)反应池Ⅲ用生成碳酸钙的化学方程式是 。
(4)过滤Ⅱ中所得滤液在农业生产中的一种用途是 。
覆铜板是制作印刷线路板的基本材料。覆铜板中的金属Sn占2﹣10%,Cu占90﹣98%.简易工艺流程如图:
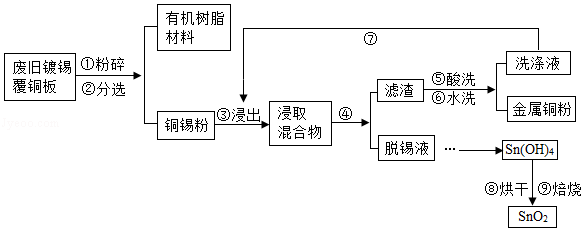
(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是 的性质(填字母代号)。
a.溶解性不同
b.密度不同
c.沸点不同
(2)步骤④中涉及的分离操作是 (填操作名称)。
(3)通过步骤⑤和⑥所得洗涤液的pH 7(填“>”、“<”、“=”)。
(4)设计步骤⑦的主要目的是 。
(5)步骤⑨中涉及的主要化学方程式为 。
侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。工业上以半水煤气(主要成分是N2、H2、CO、CO2和H2O)、食盐等为原料制取纯碱的流程如下:

(1)流程中循环利用的物质有H2O和 。
(2)步骤Ⅰ中,在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应实现了CO转化,化学方程式是 。
(3)实验室从混合气体H2、N2、CO2中分离出CO2的实验装置如图所示。广口瓶和分液漏斗中盛放的药品分别是 、 。
(4)除去纯碱中少量碳酸氢钠杂质的方法是 。
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3,达到减少污染、节约资源的目的。反应过程中溶液组成变化如图3所示。
①吸收初期(图中A点以前)反应的化学方程式为 。
②不断通入SO2,最终产物是 。

利用废弃的黄铜(含铜、锌)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图(反应条件已略去):
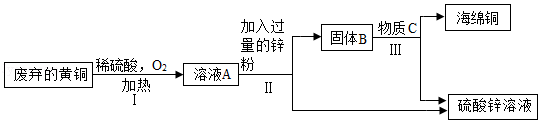
已知:2Cu+2H2SO4+O2 2CuSO4+2H2O
(1)过程Ⅱ中加入过量锌粉的目的是 。
(2)过程Ⅲ中有气体产生,所选用的物质C是 (填一种酸)。
海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
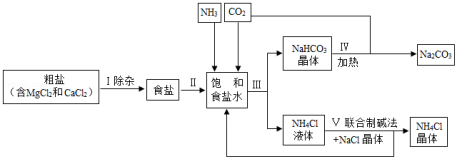
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
自然界并不缺少镁,缺少的是发现镁的眼睛。某化学兴趣小组开启寻镁之旅,现邀请你参与并完成相关内容。
(1)第一站:初识金属镁。①金属镁的物理性质: (写一条);②金属镁的化学性质:镁能与氧气反应,反应的化学方程式为 。
(2)第二站:再遇金属镁。将打磨过的镁条放入稀盐酸中,反应现象是 ,化学方程式为 。
(3)第三站:制备金属镁。小组同学模拟工业上从海水晒盐剩下的苦卤中提取镁,流程如下:
苦卤 Mg(OH)2 MgCl2 Mg,流程中X为 。
(4)第四站:再探金属镁。
[提出问题]镁能否与热水反应?如果反应,产物是什么?
[相关信息]①Mg+2H2O=Mg(OH)2+H2↑;②氢氧化镁在热水中能部分溶解。
实验操作 |
实验现象 |
实验结论 |
① ② |
① ② |
镁能与热水反应,生成氢氧化镁和氢气 |
(5)上述寻镁之旅中你收获到镁的化学性质有 。
制造芯片的基材主要是高纯硅。如图是制备高纯硅的一种工艺流程:
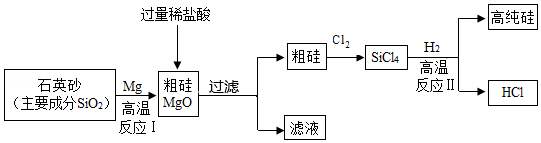
回答下列问题:
(1)反应Ⅰ的化学方程式是 。
(2)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和 (填化学式)。
(3)反应Ⅱ的基本类型属于 ;反应Ⅱ要在无氧气环境中进行,原因是 (答出一种即可)。
(4)上述生产流程中,可以循环利用的物质是 (填化学式)。
硫酸亚锡(SnSO4)广泛应用于电镀工业。该物质易与氧气反应而变质。实验室模拟工业上制取SnSO4的一种实验方案如下:

(1)SnCl2由Sn与盐酸反应制得,同时生成氢气,该反应的化学方程式为 ↑ 。
(2)Na2CO3俗称 。
(3)过滤所得滤液中的溶质为 (填化学式)。
(4)用已知质量分数和密度的浓硫酸配制质量分数为15%的稀硫酸,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和 。稀释浓硫酸的正确操作为 。
(5)反应2属于基本反应类型中的 反应。从反应2所得溶液中获得SnSO4晶体的部分操作须在隔绝空气条件下进行的原因是 。
新冠肺炎疫情防控期间,湘潭市各学校开展全域喷洒低浓度“84”消毒液进行消毒。“84”消毒液的有效成分是NaClO(次氯酸钠),模拟制备“84”消毒液的流程如图所示,其中A是密度最小的气体,B俗称烧碱,Cl2是一种黄绿色的有毒气体。请回答下列问题:
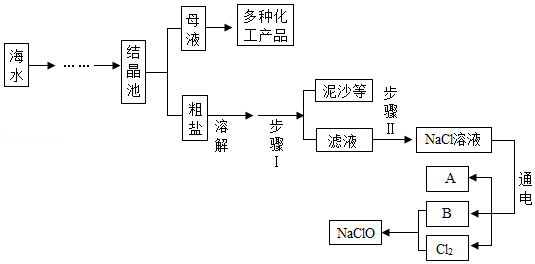
(1)A的化学式为 ,B的化学式为 。
(2)溶解过程中玻璃棒的作用是 ,步骤Ⅰ中主要的操作名称是 。
(3)步骤Ⅱ中,通常用碳酸钠来除去滤液中的氯化钙杂质,请写出有关反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(4)电解水时,一般在水中加入少量硫酸钠或氢氧化钠的目的是 ,不能加入NaCl的原因是 。
我国古代曾用“地糠法”制取Cl2,两用Cl2与石灰乳反应生产漂白粉,流程如下:

已知:漂白粉的有效成分是Ca(ClO)2,Ca(ClO)2的化学名称叫做次氯酸钙。Ca(ClO)2中,氯元素的化合价为+1价。请回答下列问题:
(1)HCl与O2反应的化学方程式为 ,该反应所属的基本反应类型为 。
(2)Ca(ClO)2在物质的分类上属于 。
A.氧化物 B.酸 C.碱 D.盐
(3)“84消毒液”(主要成分为次氯酸钠)与“洁厕灵”(主要成分为盐酸) 不能混合使用,否则会产生氯气使人中毒。请写出次氯酸钠的化学式 。
(4)石灰乳 (填“属于”或“不属于”)溶液。
氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:
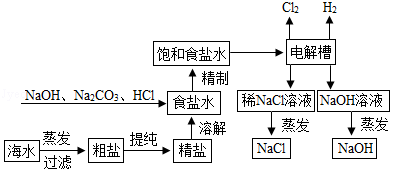
(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是 (填名称)
22等物质,“精制”过程中加入NaOH的目的是 。
(3)写出“电解槽“中发生反应的化学方程式 ,流程中可以循环使用的物质有 (填化学式)
23和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
等级 |
氢氧化钠含量 |
碳酸钠含量 |
优等品 |
≥99.0% |
≤0.5% |
一等品 |
≥98.5% |
≤0.8% |
合格品 |
≥98.0% |
≤1.0% |
23的原因是 23,下列试剂中可选择使用的是
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是 (不考虑其他杂质参加反应)
MgSO4•7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO4•7H2O的主要流程如图:

已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作a”的名称是 。
(2)“废渣Y”中含有少量的 FeOOH,其中铁元素的化合价是 。
(3)MgCO3溶于稀硫酸的化学方程式为 。
(4)“溶液A”中加入H2O2溶液会生成Fe2(SO4)3,该反应的化学方程式为 。
(5)选用MgO调节pH使Fe3+转化为沉淀,而不选用NaOH的原因是 。
一水硫酸四氨合铜的化学式为[Cu(NH3)4]SO4•H2O,是一种高效、安全的杀菌剂。它在乙醇﹣﹣水混合溶剂中的溶解度随乙醇体积分数的变化曲线如图甲所示。小明在实验室以氧化铜为主要原料合成该物质,他设计的合成路线如图乙所示:

(1)溶液A中一定存在的溶质为 。
(2)溶液B中含硫酸四氨合铜,“一系列操作”是指向溶液B中加入适量 、过滤、洗涤、干燥等。