甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是( )

A.C、CO、CO2B.H2O2、H2O、O2
C.KOH、K2CO3、KNO3D.Fe2O3、FeCl3、Fe(OH)3
甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物质按照甲乙丙的顺序不符合要求的是( )
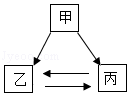
A.C、CO2、COB.H2O2、O2、H2O
C.CuO、Cu、Cu(NO3)2D.NaOH、NaCl、NaNO3
下列各组转化中,一定条件下均能一步实现的组合是( )
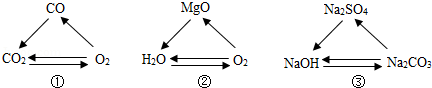
| A. |
①② |
B. |
②③ |
C. |
①③ |
D. |
①②③ |
下列各组内物质间的转化关系中,存在不能一步转化的是( )
A.Cu→CuO→CuSO4B.H2O2→O2→P2O5
C.NaCl→NaNO3→NaOHD.Fe2O3→Fe→FeCl2
下列物质间的转化,不能一步完成的是( )
A.Fe→CuB.KNO3→NaNO3C.Mg→MgOD.H2SO4→HCl
氨气(NH 3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,氨水显碱性.实验室里加热氯化铵(NH 4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水.
(1)下列装置是实验室制取气体的一些发生装置,a仪器为 ,b仪器为 .制取二氧化碳的发生装置是 (填字母序号);制取氨气的发生装置是 (填字母序号),收集氨气的方法是 .
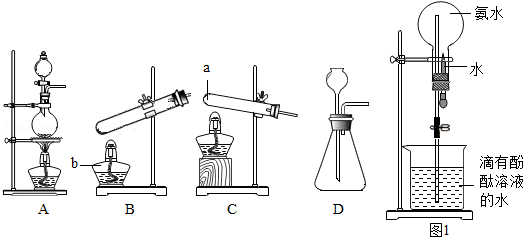
(2)图1是氨气的喷泉实验装置.打开橡皮管上的夹子,将胶头滴管中的水挤入盛满干燥氨气的烧瓶中,因为氨气极易溶于水,烧瓶内的压强降低,烧杯中的水就会进入烧瓶,形成 色的喷泉.
(3)当喷泉实验结束后,测烧瓶内溶液的pH.
步骤如下:
步骤一:用手撕一小段pH试纸,放到干净的玻璃片上.
步骤二:用蒸馏水润湿pH试纸.
步骤三:用玻璃棒蘸取待测液滴到pH试纸上.
步骤四:把试纸显示的颜色与标准比色卡对比,读取pH.
该实验步骤有几处错误? 处,请改正: .
某工厂产生的废水中含有硫酸锌和少量的硫酸铜以及污泥,为了变废为宝,利用废水制取七水硫酸锌( ZnSO 4•7H 2O),其工艺流程图如下:

回答下列问题:
(1)步骤①的操作名称 .
(2)步骤②需如入过量的物质是 ,目的是 .
(3)步骤③需加入的溶液是 .
(4)步骤④的操作是蒸发浓缩, ,过滤.
(5)如果用ZnSO 4•7H 2O来配制100g 32.2%的硫酸锌溶液,需要 g七水硫酸锌.
氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。CuCl的制备流程如下:
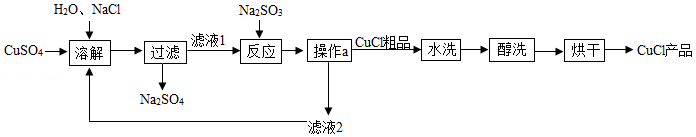
(1)“滤液1”中除了Na+、SO42﹣外,还存在较多的离子是 、 (写离子符号)
(2)“反应”中发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为 。
(3)“操作a”的名称是 。本流程中可以循环利用的物质(水除外)是 。(写化学式)
(4)可用“水洗”的原因是 ,“醇洗”的目的是 。
(5)160g CuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是 g。
深圳是海滨城市,海水资源丰富。镁被称为“国防金属”广泛地应用于火箭、飞机、轮船等制造业。工业上可从海水中提取镁,其物质的转化关系如图所示。(其中部分生成物已省略)
根据以上转化关系,回答下列问题:
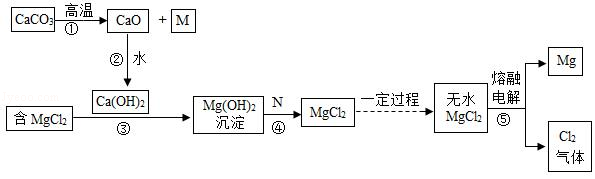
(1)M是一种常用于灭火的气体,M的化学式是 ,若在M的饱和溶液中滴入几滴紫色石蕊溶液,则溶液变 色;
(2)反应②过程中会 (填“吸收”或“放出”)热量;
(3)反应③属于 反应(填基本反应类型);
(4)N是 (只有一个正确选项,选填字母);
A.硫酸 B.盐酸 C.氢氧化钠溶液 D.氯化钠溶液
(5)写出反应④的化学方程式: ;
(6)写出反应⑤的化学方程式: 。
保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:

(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应类型为 .
(2)反应Ⅱ为复分解反应,该反应的化学方程式为 .
(3)操作a的名称为 .
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是 ,加入NaCl的原因是 .
(5)198gZn(OH)2理论上能得到Zn的质量为 g.
下列物质间的转化不能一步完成的是( )
| A. |
H 2O→H 2 |
B. |
Mg→MgO |
| C. |
Na 2CO 3→NaOH |
D. |
KNO 3→NaNO 3 |
甲、乙、丙三种物质间只通过一步反应就能实现如箭头所指方向的转化,下列不符合要求的甲、乙、丙依次为( )
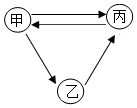
| A. |
O 2、CuO、H 2O |
B. |
Na 2CO 3、Na 2SO 4、NaOH |
| C. |
FeSO 4、FeCl 2、Fe |
D. |
CaCO 3、CaCl 2、CO 2 |
日常生活中使用的干电池是一种锌锰电池,它的构造是:负极为锌做的圆筒,正极是一根碳棒,它的周围被二氧化锰,碳粉和氯化铵的混合剂所填充,其结构如图1所示。某学校化学兴趣小组的同学准备从废旧的干电池中分离出二氧化锰,并制备硫酸锌固体。
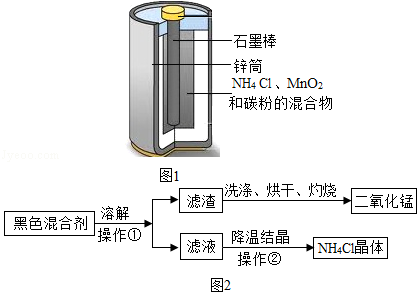
Ⅰ:设计回收二氧化锰的流程如图2所示:
(1)操作①和操作②的名称都是 ,该操作中玻璃棒的作用是 。
(2)上述操作中灼烧滤渣的目的是 。
(3)为了有效回收、利用二氧化锰,小茗同学用回收的二氧化锰与双氧水来制取氧气,请你写出该反应的化学方程式 。
Ⅱ:制备硫酸锌固体的实验步骤:
①将剪碎后的锌皮放入烧杯中,加入足量的稀硫酸,充分反应
②将滤液加热浓缩,得到热的饱和溶液
③将上述反应后的混合物过滤
④降温结晶
⑤过滤,得到ZnSO 4•7H 2O晶体
(1)正确的实验操作顺序为(填序号) 。
(2)步骤①中反应的化学方程式 。
Ⅲ:废旧干电池随意丢弃会造成环境污染。请你指出对废旧干电池的处理意见(只填一条): 。
下列变化不能通过一步反应实现的是( )
| A. |
CaCl 2→CaCO 3 |
B. |
KOH→KNO 3 |
| C. |
Cu→Cu(OH) 2 |
D. |
Na 2CO 3→NaOH |