过氧化钙( CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3为原料制备CaO2的一种工艺流程如图1:

[查阅资料]
Ⅰ.Ca(OH)2+2NH4Cl=CaCl2+2NH3•H2O
Ⅱ.CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl
Ⅲ.CaO2•8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是 ;Ca(OH)2的俗名为 ;“过滤1”所得滤渣的主要成分是 。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、 。生产过程中为了精确测定溶液的pH,常使用 (填仪器名称)。
(3)在其他条件不变的情况下,制备CaO2•8H2O的反应时间(t)对其产率(w)的影响如图2所示。
①平均反应速率最快的时间段为: (填字母)。
a.0~10min b.10~20min c.20~30min d.30~40min
②30min后,w开始下降的主要原因是 。
(4)为了测定加入的NH4Cl溶液中溶质的质量分数,取30.00g NH4Cl溶液于烧杯中,加入稍过量的AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确定该溶液中NH4Cl的质量分数(精确到0.1%) 。
氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:
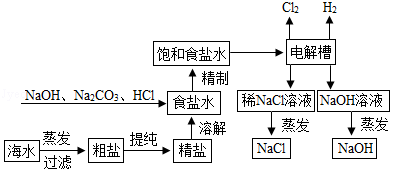
(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是 (填名称)
22等物质,“精制”过程中加入NaOH的目的是 。
(3)写出“电解槽“中发生反应的化学方程式 ,流程中可以循环使用的物质有 (填化学式)
23和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
等级 |
氢氧化钠含量 |
碳酸钠含量 |
优等品 |
≥99.0% |
≤0.5% |
一等品 |
≥98.5% |
≤0.8% |
合格品 |
≥98.0% |
≤1.0% |
23的原因是 23,下列试剂中可选择使用的是
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是 (不考虑其他杂质参加反应)
我国古代曾用“地糠法”制取Cl2,两用Cl2与石灰乳反应生产漂白粉,流程如下:

已知:漂白粉的有效成分是Ca(ClO)2,Ca(ClO)2的化学名称叫做次氯酸钙。Ca(ClO)2中,氯元素的化合价为+1价。请回答下列问题:
(1)HCl与O2反应的化学方程式为 ,该反应所属的基本反应类型为 。
(2)Ca(ClO)2在物质的分类上属于 。
A.氧化物 B.酸 C.碱 D.盐
(3)“84消毒液”(主要成分为次氯酸钠)与“洁厕灵”(主要成分为盐酸) 不能混合使用,否则会产生氯气使人中毒。请写出次氯酸钠的化学式 。
(4)石灰乳 (填“属于”或“不属于”)溶液。
某化学活动小组在实验室以MnO2固体为原料制取少量MnCO3,基本流程如下:
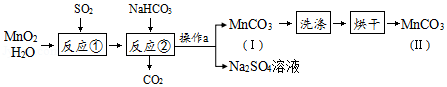
已知:MnSO4与MnCl2都可溶于水;MnCO3难溶于水且在100℃时开始分解。
(1)反应①为化合反应,产物为MnSO4.该反应的化学方程式为 ,下列物质中不能与MnSO4反应的有 。
A.稀硫酸 B.BaCl2 C.盐酸 D.Na2CO3
(2)操作a要用到的实验用品中,除玻璃仪器外,还有 (填具体的实验用品)。
(3)产品MnCO3(Ⅱ) 比MnCO3(Ⅰ) 更纯净,原因是产品MnCO3(Ⅰ) 经过洗涤、烘干以后,表面附着的H2O及 (填化学式)等杂质已被除去。
(4)为了获得纯净的MnCO3,烘干时需要控制的条件是 。
某兴趣小组在实验室模拟水厂将浑浊的湘江水净化成自来水,并最终制成蒸馏水,其实验流程如图所示:

请回答下列问题:
(1)加入明矾的作用是 ;操作1的名称是 。
(2)利用如图所示的装置进行操作2,此操作的作用是 待处理的水应该从 端通入(填"a"或"b"),理由是 。

(3)取少量的液体D于试管中,滴入肥皂水振荡,发现有较多的浮渣产生,说明此液体为 (填"软水"或"硬水"),生活中常用 的方法软化硬水。
(4)通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是 。
2018年5月23日至25日,第九届中国卫星导航年会在哈尔滨拉开帷幕,中海达、华大北斗等一批国内企业先后发布了自主研发的北斗芯片产品。芯片的主要成分是硅,如图是工业上以石英砂(SiO2)为主要原料制取纯硅的种方法,请回答以下问题。
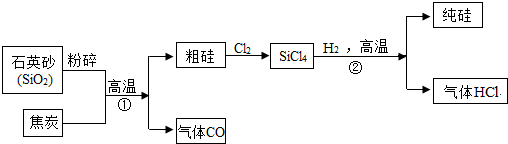
(1)地壳中硅元素的含量仅次于 元素;
(2)写出反应①的化学方程 ;
(3)反应②的基本反应类型是 ;
(4)尾气氯化氢必须收集处理,不能排放到空气中,请简要说明原因 。
结构观、微粒观、元素观和转化观都是化学学科的基本观念。
(1)将“宏观﹣微观﹣符号”表征相结合是化学学科独特的思维方式。科学家最近在﹣100℃合成了一种化合物,其分子模型如图所示。该物质的化学式是 ;从物质结构的观点说明该物质具有可燃性的原因是 ,该物质在空气中完全燃烧的化学反应方程式为 。
(2)在制备物质时,根据所制物质的组成成分选择原料,要考虑原料中能否提供产品所需的成分,且能够转化到产品中。如利用海水中的NaCl制纯碱(Na2CO3)的过程中,NaCl只提供了Na2CO3所需的“Na”,则还需要能提供含有 元素的物质。按此思路,若用Na2CO3制取NaOH,需要用到生活中一种常见的廉价原料是 (填俗称)。
(3)已知由Cu到Cu(OH)2可经三步转化:Cu→CuO→CuSO4→Cu(OH)2,而Fe经两步反应得到Fe(OH)2,请补全转化的过程:Fe→ →Fe(OH)2。

CaCl2应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产CaCl2的流程如下:

(1)氧化铁和盐酸反应的化学方程式为 。
(2)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和 。
(3)滤液1中的溶质有HCl、FeCl3、MgSO4和 。
(4)写出滤液1中加入BaCl2发生的化学反应方程式 。
(5)滤液2中加入Ca(OH)2可以除去HCl、MgCl2和 。
(6)滤液3呈碱性,为使溶液pH降低,可加入适量的 。
含硫煤燃烧会产生大气污染。为防治该污染,某工厂设计的新的治污方法不仅吸收了SO2,同时还得到了某种化工产品。该工艺流程如图所示,下列叙述不正确的是( )
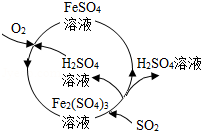
A.该流程中可得到化工产品H2SO4
B.图中FeSO4→Fe2(SO4)3的反应类型是复分解反应
C.该流程中化合价发生改变的元素为Fe、S和O
D.图中吸收SO2的化学反应方程式为:Fe2(SO4)3+SO2+2H2O═2FeSO4+2H2SO4
下列关于碳和碳的化合物知识网络图(图中表示转化关系)的说法正确的是( )

A.“C→CO”的反应中碳发生还原反应
B.“CO→CO2”的反应类型为置换反应
C.“CO2→CaCO3”的反应可用于检验二氧化碳
D.“CO2⇌H2CO3”的反应可用酚酞试剂验证
老师要求用规定量的BaCl2溶液与适量的Na2SO4溶液制备BaSO4.完成操作I后,丁丁发现自己错把Na2CO3溶液当成Na2SO4溶液,而此时BaCl2溶液已完全消耗。老师启发他,可用生成物和其他试剂完成制备BaSO4的实验。整个实验流程如图所示:
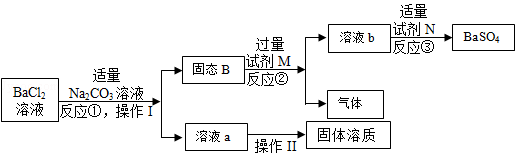
(1)反应②的化学方程式为 ,溶液b中的溶质有 。
(2)反应③的基本反应类型为 。
(3)操作Ⅱ的名称为 。
(4)从理论上讲,该实验过程最终得到的BaSO4质量与原方案得到的BaSO4质量是否相等? (填“是”或“否”)
某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。
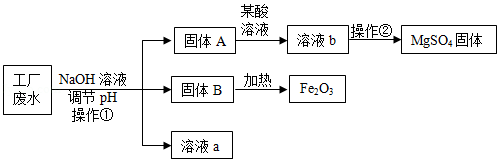
(1)固体A与某酸反应的化学方程式为 。操作②时,当 即可停止加热。
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为 。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是 (填化学式)。
在牙膏中常用轻质碳酸钙粉末作摩擦剂.小李在实验室以石灰石(杂质不反应也不溶于水)为原料制取轻质碳酸钙和氢氧化钠.

(1)操作②的名称是 .
(2)该流程中有两个反应,产物中均出现碳酸钙,这两个反应的化学方程式分别为 .
(3)为验证加入Na2CO3溶液后,溶液M中的溶质是否反应完全,可取上层清液加入 (填序号)进行检验.
A.碳酸钠溶液 B.铁粉 C.无色酚酞.