水和溶液在生命活动和生活中起着十分重要的作用。
(1)海水中含有大量的氯化钠,可以通过 方法获得粗盐,粗盐提纯得到精盐。
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是 。若用10%的NaCl溶液来配制
100 g 0.9%的氯化钠溶液,需加水 g。
(3)熟石灰在部分温度下的溶解度如下表所示。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 溶解度/g |
0.18 |
0.17 |
0.16 |
0.15 |
0.14 |
0.13 |
0.12 |
①20℃时,0.56 g氧化钙放入到盛有100 g水的烧杯中。恢复到20℃时,所得溶液中水的质量 (填“增大”、“减小”或“不变”),溶液中溶质的质量分数是 (写计算式)。
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液。下列说法正确的是 。
A.溶液的质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大 D.可以升温使之变成不饱和溶液
溶液在生命活动和生产、生活中起着十分重要的作用。
(1)生理盐水中的溶质是 。
(2)在一定温度下,向质量均为50g的四份水中分别加入一定质量的KNO3固体,搅拌至充分溶解(如有不溶解的KNO3,则过滤除去),得到溶液。加入KNO3的质量与得到相应
溶液的质量如下表所示。
①该温度下KNO3的溶解度是 g。
②实验1、2、3、4配得的溶液中,溶质的质量分数分别为a、b、c、d,则它们的关系为
a b c d(填“大于”、“等于”或“小于”)。
(3)向盛有饱和石灰水的烧杯中加入生石灰,溶液立即变浑浊,可能的原因是______(填字母)。
| A.生石灰与水反应的生成物不再溶解 |
| B.反应放热,溶液温度升高,溶解度降低 |
| C.空气中的二氧化碳与石灰水反应生成碳酸钙 |
| D.生石灰与水反应消耗水,溶剂减少,有溶质析出 |
溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)衣服上沾由的油污,可用汽油洗去,是因为汽油能_______________(填“溶解”或“乳化”)油污。
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与_________有关。
(3)某固体物质的溶解度曲线如下图所示:

20ºC时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们分别是______________、_______________、_______________。
已知200C氯化钠和硝酸钾的溶解度分别为36克,31.6克。现有一烧杯盛有200C的水100克,先加入36克氯化钠,充分搅拌,再向其中加入30克硝酸钾。
(1)下列说法则正确的是
A.氯化钠不再饱和 B.不能溶解30克硝酸钾 C.得到的硝酸钾溶液是不饱和的
(2)此时溶液中氯化钠的溶质的质量分数为_____________%(准确到0.1%)
某同学做了以下两个实验:
(1)实验1中澄清石灰水的现象是 ,产生此现象的原因是
(2)实验2中澄清石灰水的现象是 ,产生此现象的原因是
下列关于“一定”的说法存在科学性错误,请举一实例说明:
(1)均一、稳定、无色透明的液体一定是溶液(写名称,下同)
(2)含有氢、氧元素的化合物一定是碱
(3)由同种元素组成的物质一定是单质
(4)化学反应前后分子的数目一定不变(用化学方程式表示)
根据下表回答问题。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度 g/100g水 |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
①根据表中信息可得知在 (17) 温度范围内某一温度时,NaCl和NH4Cl具有相同的溶解度;
②60℃时,向两个分别盛有25g NaCl和NH4Cl的烧杯中,各加入50 g的水,充分溶解后,形成饱和溶液的是 (18) 溶液,该饱和溶液的质量是 (19) 克;
③采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。以下操作方法可行的是 (20) (填字母序号)。
A.过滤 B.升温至80℃
C.加入20 mL,60℃的水 D.搅拌使剩余固体全部溶解
大量实验表明,少量固体物质溶于水所形成的溶液具有与水不同的性质,常被人们应用于日常生活.如:冬天常在汽车的水箱内加入少量的乙二醇,其目的是
▲ ;在高原煮鸡蛋,在水中加食盐的目的是 ▲ ;做溶液导电性实验时,向水中滴几滴稀硫酸,能增强溶液的 ▲ 性.
某化学兴趣小组的同学探究酸碱中和反应实验:
(1)配制76g质量分数为10%的稀盐酸,需要 g质量分数为38%的盐酸,需要 mL水。
(2)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞试液, 溶液变成 色,pH 7(填“>”、“<”或“=”),向锥形瓶逐滴滴入(1)配制的稀盐酸并振荡,至溶液恰好褪成无色。写出反应的化学方程式 。此反应属于中和反应,请用文字叙述一例中和反应在日常生活或工农业生产中的应用
溶液变成 色,pH 7(填“>”、“<”或“=”),向锥形瓶逐滴滴入(1)配制的稀盐酸并振荡,至溶液恰好褪成无色。写出反应的化学方程式 。此反应属于中和反应,请用文字叙述一例中和反应在日常生活或工农业生产中的应用  。
。
20℃时氯化钠的溶解度为36克。该温度下,某氯化钠溶液的组成模型如图,请你回答: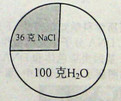
(1)该溶液的溶质是
(2)保持温度不变蒸发10克水后,氯化钠溶液的溶质质量分数 。(填“变大”、“变小”、“不变”)
无土栽培是利用营养液栽培作物的一种方法。
(1)下列化学肥料中属于复合肥的是 (填序号)。
①硝酸铵 ②磷酸二氢铵 ③硝酸钾 ④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为
g。
(3)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验。
实验1 实验2
根据以上实验,请你进行有关推断。
①由实验1可确定原营养液中一定没有的物质是 ;
②根据实验1、实验2推测原营养液的组成可能有 种情况;
③若测得原营养液中K+和Cl一的数目之比为1:1,则原营养液的组成中的溶质是
(5分)溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能 (填“溶解”或“乳化”)油污。
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与 有关。
(3)某固体物质的溶解度曲线如下图所示:
20℃时,要使接近饱和的该物质的溶液变为饱和溶液,通常可采用三种方法,它们
分别是 、 、 。
(3分)如图为硝酸钾和氯化钠的溶解度曲线。由图可知:
(1)当温度为30℃时,硝酸钾的溶解度 (填“>”、 “<”或“=”)氯化钠的溶解度。(2)当硝酸钾中含有少量氯化钠时,可用 法提纯硝酸钾。
(3)硝酸钾、氯化钠都属于 (填“易溶”、“可溶”、“微溶”或“难溶”)物质。
某化学兴趣小组进行溶液的配置和粗盐的初步提纯实验.
(1)配置150g质量分数为10%的氢氧化钠溶液.
①计算:需要氢氧化钠固体的质量为 g;水的体积为 mL(水的密度近似看作1g/cm3)
②称量:调节托盘天平平衡后,将 放在托盘天平的左盘,称量其质量.然后再右盘添加 .最后添加氢氧化钠固体,直至天平平衡.
③溶解:用量筒量取所需的水,倒入装有氢氧化钠固体的烧杯里,用玻璃棒 ,使其溶解,并冷却至室温.
④存储:把配好的溶液装入试剂瓶,塞好橡皮塞并 ,放到指定的地方.
(2)粗盐的初步提纯实验
①称取5.0g粗盐,用药匙逐步加入10mL水中,知道粗盐不再溶解为止.还需要进行的实验步骤的顺序为:称量剩余粗盐、 (填编号)
| A.过滤 | B.计算产率 | C.蒸发 | D.称量精盐 |
②过滤操作如图所示,指出其中的错误之处: ; ; ;
.