今年底我国首只火星探测器“萤火一号”将踏上访问火星的旅程,其重要部件太阳能帆板使用的高纯硅制备原理是:2H2+SiCl4高温 Si+4HCl。该反应属于
| A.化合反应 | B.置换反应 | C.分解反应 | D.复分解反应 |
某兴趣小组对某化学反应进行了探究,实验测定结果如下,下列说法正确的是
| 物质 |
A |
B |
C |
D |
| 反应前质量/g |
20 |
12 |
2 |
6 |
| 反应后质量/g |
0 |
2 |
2 |
待测 |
A.该反应是分解反应 B.反应后D物质的质量是30g
C.C物质可能是该反应的催化剂 D.以上说法均不正确
某物质在氧气中燃烧后,产物只有水和二氧化碳,则该物质的组成中
A.一定只含C、H元素
B.一定含C、H元素,可能含O元素
C.一定含C,可能含H
D.一定含C、H、O元素
初中化学学习中,我们初步认识了物质的微观结构。
(1)氯化钠、金刚石、干冰三种物质中,由离子构成的物质是 。
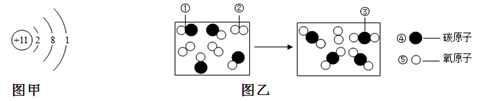
(2)图甲是某粒子的结构示意图,该粒子在化学反应中容易 电子(填“得到”或“失去”)。
(3)图乙是CO与O2反应的微观示意图,反应前后没有发生变化的粒子是 (填序号)。
| A.①② | B.②③ | C.③④ | D.④⑤ |
在一个密闭容器内有如下反应,反应前后两次测得各物质的质量如表所示,则下列说法错误的是
| 物质 |
M |
N |
P |
Q |
| 反应前的质量/g |
40 |
4 |
3.6 |
4.8 |
| 反应后的质量/g |
待测 |
13 |
12.6 |
10. 8 |
A.上述化学反应一定为分解反应
B.该反应生成的Q和P的质量之比为2:3
C.N和P的相对分子质量之比为1:1
D.第二次测得M的质量为16
草酸钙(化学式为CaC2O4,相对分子质量为128)是一种难溶于水的白色固体,受热能分解。小红同学为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量随时间变化如图所示。请回答下列问题:

(1)t1~t2时问段内固体质量减少的原因是产生了一种极易与血红蛋白结合的有毒气体,该气体的化学式为 ;同时生成一种白色同体,它与大理石的主要成分相同,则该段时问内反应的化学方程式为
(2)t2~t3时间段内固体质量不变的原因是
(3)t3~t4时间段内反应的化学方程式为
在一定条件下,科学家利用从烟道气中分离出的CO2与太阳能电池电解水产生的H2合成甲醇(CH3OH)同时生成水,其过程如下图所示,试回答下列问题:

注:上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),它的作用是CO2吸收剂。
(1)试写出上述合成线路中的两个化学反应的化学方程式:
①____________________________;
②____________________________。
(2)上述合成路线对于环境保护的价值在于____________________________。
(3)上述合成线路中可以循环利用的物质为___________
在一定条件下有如下转化关系(其中A和B均为黑色粉末,C为红色粉末)
① A + B ="=" C + D ② A + D ="=" E
A、B、C的化学式分别是:A B C
写出下列反应的化学方程式并注明类型
(1)碳不充分燃烧 ( )类型
(2)碳高温还原氧化铁
(3)将氨气(NH3)通入氧化铜中加热,生成了铜、水和一种单质气体________________
1.6 g某物质在氧气中完全燃烧,生成4.4 g二氧化碳和3.6 g水,关于该物质的组成有下列判断:①一定含有C、H元素 ②一定不含O元素 ③可能含O元素 ④一定含O元素 ⑤分子中C、H原子个数之比为1:2 ⑥分子中C、H原子个数之比为1:4;正确的是
A.①②⑥ B.①②⑤ C.①③⑥ D.①④⑤
在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如图所示。正确的说法是
| A.该反应是分解反应 |
| B.若消耗3g乙,则生成17g丙 |
| C.丁一定是该反应的催化剂 |
| D.参加甲、乙的质量之和一定等于生成丙的质量 |
地质考察人员发现一种带螺纹的矿石,研究时发现该矿石能在氧气中燃烧,主要反应是4X+11O2 2Fe2O3+8SO2。下列有关说法中不正确的是
2Fe2O3+8SO2。下列有关说法中不正确的是
| A.X的化学式是Fe4S8 |
| B.SO2分子中的硫、氧原子的个数比为1:2 |
| C.反应前后氧元素的化合价发生改变 |
| D.Fe2O3中铁元素的质量分数为70% |
①氧气;②干冰;③石灰浆;④活性炭的一些用途为:保存食物、做吸附剂、冶炼钢铁、砌砖抹墙。按四种物质的用途排列次序正确的是
| A.①②③④ | B.①③②④ | C.④③②① | D.②④①③ |