向10g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。
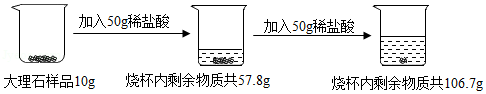
请计算:
(1)该大理石样品中碳酸钙的质量分数是 ;
(2)计算所用稀盐酸的溶质质量分数。
向60g Na 2CO 3溶液中逐滴加入一定溶质质量分数的CaCl 2溶液,实验过程中生成沉淀的质量与加入CaCl 2溶液的质量关系如图所示。
(1)恰好完全反应时,生成沉淀的质量为 g;
(2)计算恰好完全反应时,所得溶液中溶质的质量分数。

学习小组的同学通过如图实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
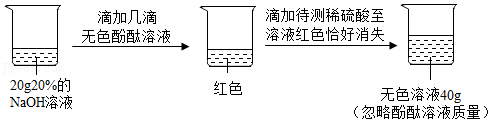
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量为 g。
(2)计算稀硫酸中溶质的质量分数。
某食用纯碱中含有少量的氯化钠,为测定高纯碱中碳酸钠(Na 2CO 3)的含量,现取纯碱样品12.5g,加入150.0g稀盐酸溶液恰好完全反应,测得反应后溶液总质量变为158.1g.计算:
(1)反应中产生CO 2的质量.
(2)纯碱样品中Na 2CO 3的质量分数.
为测定一标签破损(如图)的钙片中碳酸钙的含量,某同学做如图实验:取10片钙片,放入干燥、洁净的烧杯中,然后逐滴滴加稀盐酸,当加入50g盐酸后,恰好完全反应,此时称量烧杯内剩余物质的总质量为65.6g(钙片中其他成分不和稀盐酸反应,反应中产生的气体全部放出).
(1)反应中生成 g二氧化碳,该钙片中碳酸钙的质量分数为 ;
(2)试计算所用稀盐酸中HCl的质量分数.

某腐蚀印刷电路板的废液经处理后只含有CuCl2和FeCl2两种溶质.为了分析处理后废液的组成,取1000g该废液,设计如下实验流程进行探究:
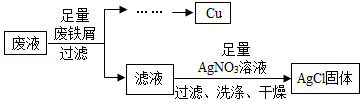
实验过程中加入废铁屑的质量、析出Cu的质量的数据记录如下表:
废铁屑的质量/g |
20 |
40 |
80 |
100 |
析出Cu的质量/g |
19.2 |
38.4 |
64 |
64 |
(注:废铁屑中的杂质不溶于废液,不与废液反应,不考虑过滤中的损失.)
(1)废铁屑中单质Fe的质量分数为 .
(2)1000g废液中CuCl2的质量为 g.
(3)若在实验流程中分别加入足量废铁屑、足量AgNO3溶液,最终得到861g AgCl固体,则1000g废液中FeCl2的质量分数是多少?
为了测定一瓶硫酸铜溶液的溶质质量分数,取出50克该溶液,向其中逐滴加入溶质质量分数为16%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关量系如图所示,请你仔细分析此关系图,并进行计算:
(1)当滴入氢氧化钠溶液 克时,硫酸铜与氢氧化钠恰好完全反应。
(2)计算此硫酸铜溶液中溶质的质量分数(写出计算过程)。

向盛有20.0g稀硫酸的烧杯中倒入5.0g黄铜(铜锌合金)样品粉末,恰好完全反应.称得未溶物质量为3.7g.完成下列计算:
(1)该黄铜样品中含Zn的质量为 g
(2)所用稀硫酸中溶质的质量分数
(3)反应后所得溶液中溶质质量分数(结果保留一位小数)
碳酸氢铵(化学式NH 4HCO 3)是农业生产中常用的铵态氮肥。
(1)①碳酸氢铵中氮、氢、碳、氧四种元素的最简质量比为 ;
② g碳酸氢铵中含4.8g氧元素。
(2)将15.8g碳酸氢铵加入到盛有100g稀盐酸的烧杯中,恰好完全反应。求反应后所得溶液的溶质质量分数。(写出计算步骤)
将25.6gNaCl和MgCl 2固体混合物完全溶于126g水中配成溶液,再将200g一定溶质质量分数的NaOH溶液不断加入到该溶液中,充分反应后,测得的实验数据如表.
| 实验次数 |
1 |
2 |
3 |
4 |
5 |
| 加入NaOH溶液质量/g |
40 |
40 |
40 |
40 |
40 |
| 共生成沉淀的质量/g |
2.9 |
5.8 |
m |
11.6 |
11.6 |
求:(1)如表中m的值为
(2)恰好完全反应时,所得溶液中溶质的质量分数.
取氯化钙和盐酸的混合溶液51.88g,逐滴滴加10.6%的碳酸钠溶液。所加入碳酸钠溶液的质量和混合溶液pH变化关系如图所示,回答下列问题:
(可能用到的相对分子质量:CaCl2﹣111 HCl﹣36.5 Na2CO3﹣106
NaCl﹣58.5 CaCO3﹣100 CO2﹣44 H2O﹣18)
(1)BC段反应的化学方程式为 。
(2)CD段溶液pH>7的原因是 。
(3)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程,计算结果精确至0.1%)。

取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,请加稀盐酸的质量与产生气体质量的关系如图所示。求:
(1)混合物CaCO3中的质量为 ;
(2)稀盐酸中的溶质质量分数为 ;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)

氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学反应方程式为3Cl2+6KOH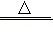 5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
(1)参加反应的氯气的质量为 g。
(2)所用KOH溶液中溶质的质量分数是多少?
小明用石灰石测定某稀盐酸中溶质的质量分数,向盛有100g稀盐酸的烧杯中依次加入石灰石粉末(杂质不参加反应),充分反应后,记录实验数据见下表。请计算:
| 实验次数 |
第一次 |
第二次 |
| 石灰石粉末质量/g |
15 |
15 |
| 烧杯中物质总质量/g |
109.5 |
121.2 |
(1)共生成二氧化碳 g。
(2)所用稀盐酸中溶质的质量分数。
我市锰矿资源丰富,MnO 2是一种无机功能材料,主要用于制造干电池。某校课外活动小组同学得到当地某粗MnO 2样品(主要含有杂质MnCO 3,其它杂质忽略不计),为了测定此样品中MnO 2的含量,把100g粗MnO 2样品放入烧杯中,将40g稀硫酸分4次加入与之充分反应,测得的数据如下表。
| 次数 |
1 |
2 |
3 |
4 |
| 加入稀硫酸的质量(g) |
10 |
10 |
10 |
10 |
| 剩余固体质量(g) |
94.25 |
88.5 |
82.75 |
78.2 |
(已知烧杯中发生的反应为:MnCO 3+H 2SO 4═MnSO 4+H 2O+CO 2↑)
请根据图表数据回答下列问题:
(1)样品中杂质的质量是多少?
(2)该样品中MnO 2的质量分数是多少?
(3)稀硫酸中溶质的质量分数是多少?