除去下列物质中混有的少量杂质(括号内为杂质),所选试剂和操作方法均正确的是( )
选项 |
物质 |
试剂和操作方法 |
A |
CuO(Cu) |
加入适量的盐酸充分反应后,过滤、洗涤、烘干 |
B |
C(MnO2) |
加入H2O2溶液,待无气泡产生后,过滤、洗涤、干燥 |
C |
KCl(AlCl3) |
加入适量的KOH溶液,蒸发 |
D |
BaCl2溶液(NaCl) |
加过量Na2CO3溶液,过滤,向洗涤后的滤渣中加入适量稀盐酸 |
A.AB.BC.CD.D
某品牌补钙剂的主要成分是碳酸钙,实验小组的同学取该补钙剂2.5g,加入溶质质量分数为7.3%的稀盐酸至不再有气泡产生,共收集到二氧化碳0.88g(补钙剂中其他成分均不与稀盐酸反应)。请计算。
(1)该补钙剂中碳酸钙的质量分数。
(2)所用稀盐酸的质量。
化学兴趣小组的同学在验证硫酸的性质时,进行了以下实验。
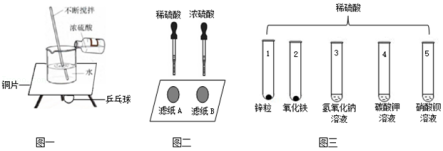
【实验一】浓硫酸稀释过程中的能量变化。
图一实验中,观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水 。
【实验二】溶液浓度对硫酸化学性质的影响。
图二实验中,观察到很快变黑的是滤纸 (填“A”或“B”),由此可知,硫酸溶液的浓度不同,腐蚀性不同。
【实验三】稀硫酸的化学性质。
小组同学按图三进行实验。
(1)试管1中发生反应的化学方程式为 。
(2)试管2中可观察到的现象是 。
(3)向试管3中滴加了足量的稀硫酸仍无明显现象,要证明二者已经发生反应,可选用
(填字母序号)继续进行实验,以达到实验目的。
A.酚酞溶液
B.氯化钡溶液
C.硫酸铜溶液
(4)小组同学将4、5两支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。同学们对白色沉淀的成分产生了兴趣,继续进行实验。
【提出问题】白色沉淀的成分是什么?
【作出猜想】猜想一:
猜想二:BaSO4、BaCO3
【实验与结论】
实验操作 |
实验现象 |
实验结论 |
取少量白色沉淀与试管中,向其中加入足量的稀盐酸。 |
。 |
猜想二成立。 |
实验结束后,在老师指导下同学们对废液缸中的固体物质进行了回收。在检验废液时发现硫酸过量,为防止其污染环境,从实验成本的角度考虑,向该废液中加入适量的
(填一种具体物质),处理后再排放。
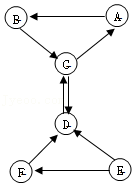
A~F为初中化学常见的物质。D、E、F为不同类别的化合物,A是C通过绿色植物光合作用产生的气体,E是常用的食品干燥剂。它们的转化如图所示(“→”表示一种物质可以转化为另一种物质,部分反应物、生成物和反应条件已略去)。请回答。
(1)A物质是 。
(2)B物质所属的类别是 (填“单质”、“氧化物”、“酸”、“碱”或“盐”)。
(3)E→F的反应 (填“吸收”或“放出”)热量。
(4)F→D发生复分解反应的化学方程式为 。
许多化学反应无明显现象,氢氧化钠溶液和二氧化碳的反应就是其中之一。
【提出问题】怎样证明氢氧化钠溶液和二氧化碳发生了反应?
【实验设计】同学们写出该反应的化学方程式 ,并根据该反应原理分别设计了图一、图二两个实验。
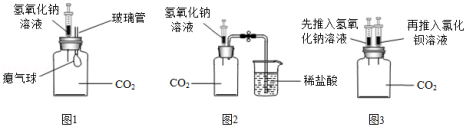
【实验验证】
(1)第一组同学按图一所示,将氢氧化钠溶液全部推入集气瓶中,过一会儿观察到气球鼓起,认为二者发生了反应。第二小组同学认为该实验不严谨,理由是 。于是同学们将该装置中氢氧化钠溶液换成 ,做了对比实验,证明二者发生了反应。
(2)第二组同学按图二所示,先将氢氧化钠溶液全部推入集气瓶中,过一会打开止水夹,观察到 ,也证明二者发生了反应。
【拓展延伸】同学们经过反思,设计并进行了图三所示的实验,观察到瓶中产生 ,再次证明氢氧化钠溶液与二氧化碳发生了反应。
【归纳总结】通过以上实验,同学们经过讨论,认为对于无明显现象的化学反应,可以通过检验反应物减少和 两个不同的角度证明反应的发生。
【废液处理】实验结束后,同学们将上述实验中所有物质倒入同一洁净的烧杯中,得到无色澄清溶液,测得溶液的pH<7,且含有毒的钡离子。从环保的角度考虑,需要向烧杯中加入适量的 (填一种具体物质),将废液处理达标后再排放。
下列实验操作能达到实验目的的是( )
选项 |
实验目的 |
实验操作 |
A. |
鉴别某固体是否为铵态氮肥 |
加稀盐酸,闻气味 |
B. |
鉴别稀盐酸、氢氧化钠、氯化钠三种溶液 |
分别滴加酚酞溶液,再相互混合 |
C. |
除去碳酸钙中混有的少量氯化钙 |
加水溶解、过滤、蒸发 |
D. |
除去硫酸钠溶液中混有的少量氢氧化钠 |
加入过量的硫酸铜溶液,过滤 |
A.AB.BC.CD.D
国家标准规定工业纯碱中碳酸钠的质量分数≥98.0%为合格品。为测定某工业纯碱是否为合格品,兴趣小组成员分别进行了如图的实验。(杂质不参与反应,过滤后滤渣损失忽略不计)

(1)溶解时玻璃棒的作用是 。
(2)实验中加入过量CaCl2溶液的目的是 。
(3)通过计算判断该工业纯碱是否为合格品。(写出计算过程,结果精确到0.1%)
(4)实验过程中个别同学出现了以下问题。
①过滤时得到的滤液浑浊,原因可能是 ;(任写一种)
②过滤所得的滤渣未经洗涤直接干燥,这一操作会导致该样品中碳酸钠的质量分数计算结果 。(选填“偏大”、“不变”或“偏小”)
江西赣州被誉为“世界钨都”,钨(W)是一种重要的战略资源。如图是一种生产钨的工业流程:
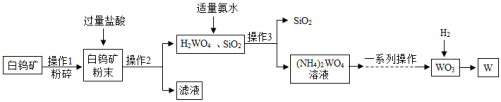
已知:白钨矿的主要成分是钨酸钙(CaWO4),还含有CaO、SiO2等;碳在高温条件下会与金属钨反应生成碳化钨。
(1)操作1中粉碎白钨矿的目的是 。
(2)操作2所得滤液中一定含有的阳离子是 、 。
(3)流程中氨水(NH3•H2O)和H2WO4反应生成(NH4)2WO4的化学方程式为 。
(4)用氢气还原WO3可获得高纯度的钨,此处不宜用焦炭代替氢气的原因是 。
(1)操作1中粉碎白钨矿的目的是增大反应物接触面积,加快反应速率;
(2)白钨矿的主要成分是钨酸钙(CaWO4),还含有CaO、SiO2,加入盐酸后二氧化硅没有参加反应,所以操作2所得滤液中一定含有的阳离子是Ca2+和过量的盐酸中的H+;
(3)反应物是NH3·H2O和H2WO4生成物是(NH4)2WO4,所以方程式是:2NH3·H2O+H2WO4═(NH4)2WO4+2H2O
(4)碳在高温条件下会与金属钨反应生成碳化钨,所以此处不宜用焦炭代替氢气。
以某菱镁矿石(主要成分是MgCO3,含少量MnCO3、SiO2)制取MgSO4•7H2O,流程如图:

(1)“酸浸”时,为了提高浸取率,除了搅拌、提高硫酸浓度外,还可采取的措施有
(写出一种)。此时,MnCO3发生反应的化学方程式是 。
(2)“转化”时主要反应是NaClO+MnSO4+H2O═MnO2↓+NaCl+H2SO4,氯元素反应前后化合价变化情况是 (填“升高”或“降低”)。
(3)硫酸镁溶液在不同温度下进行浓缩结晶,可得到不同的晶体:
温度/℃ |
﹣3.9~1.8 |
1.8~48.1 |
48.1~67.5 |
67.5~200 |
析出晶体 |
MgSO4•12H2O |
MgSO4•7H2O |
MgSO4•6H2O |
MgSO4•H2O等 |
①“操作1”的具体操作是:蒸发浓缩滤液至表面有晶膜出现(此时MgSO4溶液已饱和)、 、过滤、洗涤、低温干燥。
②“操作1”所得滤液中能分离出一种可循环使用的物质,该物质是 H2SO4 (填化学式)。循环使用的目的是 。
(4)已知:MgSO4•7H2O中镁元素质量分数为9.76%。采用热分析法测定所得MgSO4•7H2O样品中镁元素质量分数:
①未加热前,测得样品中镁元素质量分数略大于9.76%,可能的原因是 。
②高于900℃后,测得剩余固体中镁元素质量分数大于20%,可能的原因是 。
(5)若用100t菱镁矿石可制得246t MgSO4•7H2O产品,忽略反应过程中镁元素损失,求该菱镁矿石中MgCO3的质量分数。(写出计算过程)
为测定某石灰石样品中碳酸钙的质量分数,取2.0g石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经过滤,干燥、称重,得实验数据如表:
第一次 |
第二次 |
第三次 |
第四次 |
|
稀盐酸的用量/g |
5.0 |
5.0 |
5.0 |
5.0 |
剩余固体的质量/g |
1.5 |
1.0 |
0.5 |
0.3 |
已知石灰石中的杂质既不与盐酸反应,也不溶解于水。下列说法正确的是( )
A.第三次实验后碳酸钙无剩余
B.第四次实验后盐酸无剩余
C.盐酸中HCl的质量分数是3.65%
D.样品中碳酸钙的质量分数是85%
化学是一门以实验为基础的科学,实验是科学探究的重要手段。
(1)完成“探究某种盐的性质”实验,填写下表。
试管序号 |
甲 |
乙 |
丙 |
实验操作 |
|
|
|
实验现象 |
红色溶液 |
白色沉淀 |
无色气体 |
实验结论 |
该盐是 (选填“NaCl”“Na2CO3”“Na2SO4”),其水溶液呈 性。 |
||
实验解释 |
丙中发生反应的化学方程式: 。 |
||
实验计算 |
全班同学完成试管乙实验,共消耗质量分数为10.4%的BaCl2溶液50g,实验后最多收集到 g白色沉淀。 |
||
(2)处理“CO2的实验室制取与检验”实验废液。全班同学完成该实验共产生1000g含HCl废液(固体已除,大理石中杂质未参加反应),不能直接排放。
【实验方案】先测定废液中HCl的质量分数,再用熟石灰处理废液至中性。
【实验操作】
①称量 g NaOH固体,溶解,配制30g 5%的NaOH溶液。
②取100mL小烧杯,倒入20g废液样品,插入pH计测定溶液的pH,向废液样品中逐滴加入5%的NaOH溶液。实验过程中溶液pH变化如图所示。
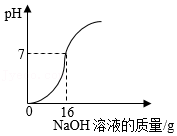
③投入 g熟石灰处理剩余废液(写出计算过程)。
【实验反思】有同学提出也可以根据盐酸具有挥发性直接加热废液除去杂质HCl,并得到CaCl2。写出你的观点及理由: 。
将CO和铁的氧化物FexOy置于密闭容器中,一定条件下充分反应至完全。反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是( )
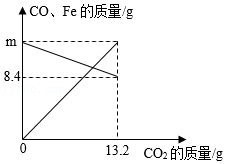
A.m的值为12.6
B.铁的氧化物中x:y=3:4
C.参加反应的铁的氧化物的质量为16g
D.当CO2质量为4.4g时,容器内CO质量为14g
某同学用溶质质量分数为15%的稀盐酸和大理石反应来制取二氧化碳气体:
(1)用20.3g溶质质量分数为37%的浓盐酸能配制上述稀盐酸 g(结果精确到1g)。
(2)若需收集10瓶(每瓶以125mL计算)二氧化碳气体,同至少需要多少克上述稀盐酸与足量的大理石反应才能制得(实验条件下二氧化碳的密度为2g/L)?(写出计算过程,结果精确到0.01g)
向一定量的H2SO4和CuSO4的混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示。
(1)当加入NaOH溶液质量为ag时,溶液中含有的溶质为 。
(2)原混合溶液中,溶质H2SO4的质量(写出计算过程,下同)
(3)恰好完全反应时,消耗NaOH溶液的总质量。

有一包白色固体混合物,可能由NaCl、CuSO4、Na2CO3、Na2SO4、BaCl2、NaOH中的一种或几种组成,为确定其组成,兴趣小组同学进行下列实验:
(1)取少量固体溶于足量的水过滤得到白色固体A和无色滤液B,则原固体中一定不含有 。
(2)向白色固体A中加入足量的稀盐酸,固体全部溶解,且有气泡生成,则原固体中一定有 ,一定不含有 。
(3)小红同学取少量滤液B,滴加无色酚酞试液,溶液变红,她认为原固体中一定含有NaOH。你同意小红的观点吗? (填“是”或“否”)。
(4)小雪同学另取一份滤液B,加入足量的BaCl2溶液,观察到有白色沉淀生成,再向上层清液中滴加无色酚酞试液,溶液变红,则原固体中一定含有 。
(5)以上实验不能确定的物质是 。