A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A的最外层电子数是次外层电子数2倍,B是短周期中金属性最强的元素,C是同周期中阳离子半径最小的元素,D元素的最高价氧化物对应水化物与B元素的最高价氧化物对应水化物反应的产物M是制备木材防火剂的原料,E的最外层电子数与内层电子数之比为3﹕5。请回答:
(1)D的元素符号为 。
(2)F在元素周期表中的位置 。
(3)用电子式表示元素B与元素F形成的化合物: 。
(4)B单质与氧气反应的产物与C的单质同时放入水中,产生两种无色气体,有关的化学方程式为 、 。
(5)工业上将干燥的F单质通入熔融的E单质中可制得化合物E2F2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
(6)某混合物的稀溶液中,只可能含有B、C、F构成的简单离子或A、E的最高价氧化物对应水化物所电离出来的阴离子。现分别取一定体积的该溶液进行实验。两次每次取200.00mL进行实验。
实验1:取2mL溶液,向其中加入AgNO3溶液有沉淀产生;
实验2:取200mL溶液,向其中加入足量BaCl2溶液后,得干燥沉淀12.54g,沉淀经足量盐酸洗涤、干燥后,剩余4.66g。请回答:
①根据以上实验,不能判断是否存在的离子有 。
② B的简单离子是否存在 ;若存在,浓度至少为 mol/L(若不存在,则不必回答第二问)。
暗紫色化合物A可作为电极材料的新型超铁电磁,因具有绿色、高电压和高能量的特点,近年来引起了电化学界的高度重视。在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀。为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验。经组成分析,该粉末仅含有O、K、Fe三种元素。另取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)3.96 g化合物A中含有Fe元素的物质的量为 mol,含有钾元素的物质的量为 mol。化合物A的化学式为 ;
(2)化合物A与H2O反应的离子方程式为 。
(3)为研究温度对化合物A水溶液稳定性的影响,请设计一个实验方案 。
(18分)从化合物A( )出发,可发生图示的一系列反应,图中化合物D能使FeCl3溶液显紫色,G能进行银镜反应。E和H常温下为气体。试回答:
)出发,可发生图示的一系列反应,图中化合物D能使FeCl3溶液显紫色,G能进行银镜反应。E和H常温下为气体。试回答:
(1)A中所含官能团的名称为 ,A的核磁共振氢谱图中有 个峰,写出下列化合物的结构简式B: ;G: 。
(2)反应类型:( I ) ;(Ⅱ) 。
(3)写出C→E的化学方程式: ;
写出D→H的化学方程式: 。
(4)L是D的同分异构体,L具备下列条件,①L能与使FeCl3溶液显紫色,②能进行银镜反应,且能发生水解反应。写出符合要求的L的一种结构简式 。
A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:
已知A溶液显碱性,焰色反应为黄色,且可促进水的电离。
(1)若A、B、C中含有相同的金属元素,则A的化学式为 ,D的化学式为 ;A、C反应生成B的离子方程式为 。
(2)若C是一种无色无味的气体,用离子方程式表示A溶液显碱性的原因_______________,C与E反应生成B的化学方程式为 。
现有A-G七种物质,已知A是赤铁矿的主要成分,E是浓溶液稀释时会放出大量的热,G溶液为蓝色,它们之间存在如图所示的转化关系。
(1)写出下列物质的化学式;E: ,D: .
(2)在反应①②③中,属于置换反应的是 (填序号)。
(3)工业上常利用反应①的原理练铁,写出反应①的化学方程式 。
(4)写出物质C与E的稀溶液发生反应的离子方程式: 。
下图中每一个方格表示有关的一种反应物或生成物(部分的产物已省略);X加热产生A、B、C三种物质,其中A、C为无色气体,B在常温下是一种无色的液体;X与NaOH溶液在加热的条件下产生一种能使湿润的红色石蕊试纸变蓝的气体C;X与HCl反应产生一种无色无味的气体A,它能使澄清的石灰水变浑浊;请填下列空白: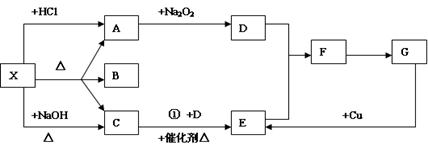
(1)物质x可以是 ,B是 ,C是 ,F是 。(填写化学式)
(2)反应①的化学方程式 。
(3)F→G的化学方程式 。
(14分)在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,F在D中燃烧发出苍白色火焰。H可用于制造光导纤维,J是一种乳白色凝胶状沉淀。(部分生成物和部分反应条件未列出) 请回答下列问题:
(1)形成单质D的元素在周期表中的位置
(2)形成C、D、F单质的元素半径由大到小的顺序(填写元素符号)
(3)C长期暴露在空气中,最终产物是
(4)H在高温下与碳反应方程式为 ,若转移4mol电子参加反应的碳为 mol。
(5)写出反应①的离子方程式
(6)写出反应②的化学方程式
材料科学是近年来与化学有关的科学研究热点。某新型无机非金属材料K由两种非金属元素组成。它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特征。它是以中学化学中常见物质为原料来生产的。下图虚线框内的其它转化是为探究C的组成而设。G、F、H均为难溶于水的白色固体;图中C、H、K均为含A元素。其余物质均为中学化学中常见物质。
请回答下列问题:
(1)实验室通常用MnO2制取气体B,发生该反应的化学方程式为 ,为防止气体B污染环境通常
用 (填化学式)溶液吸收,反应的离子方程式为
(2)化合物H与碳混合加强热可制得单质A,该反应中氧化剂与还原剂的物质的量比为
(3)写出反应③的化学方程式3D==K+8X↑,K的化学式为 ,X的化学式为 。
(4)K抗腐蚀能力很强,但易被氢氟酸腐蚀,K与氢氟酸反应生成一种气体和一种盐,此盐中存在的化学键类型有 。
(5)写出反应②的化学方程式 。
PTT是近几年来迅速发展起来的新型热塑性聚酯材料,具有优异性能,能作为工程塑料、纺织纤维和地毯等材料而得到广泛应用。其合成路线可设计为:
其中A、B、C均为链状化合物,A能发生银镜反应,B中不含甲基。请回答下列问题:
(1)A、B的结构简式分别为 、 。
(2)C中是否含有手性碳原子 。(填“含有”或“不含有”)
(3)写出一种满足下列条件的A的同系物的结构简式 。
①分子式为C4H6O ②含有1个-CH3
(4)1 mol C可与足量钠反应生成 L H2(标准状况)。
(5)由物质C与D反应生成PTT的化学方程式为 ,反应类型为 。
下列框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去)。
请回答:
(1)E的化学式为____________;甲的原子结构示意图为____________;
(2)反应①的离子方程式为____________________________________;
反应②的化学方程式为____________________________________;
(3)实验室制取并收集B的操作中,用____________法收集B,验证B已收集满的方法是_______________________________________________(限答一种)。
(4)实验室制备丁的方程式为____________________________________,工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示)______________________。
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:
据此回答下列问题:
(1)I、II、III、IV四步中分离溶液和沉淀所采取的操作名称是 ,该实验操作所用到的玻璃仪器有 。
(2)根据上述流程,写出D、E所含物质的化学式:
沉淀D ;溶液E 、 。
(3)写出②、③反应的离子方程式:
② ;③ ;
(10分)如下图中A~J分别代表有关反应中的一种中学化学常见单质或化合物,其中B、C、D、I均为无色气体,G为白色沉淀。(部分产物和反应条件已略去)
(1)若A加热后得到等物质的量的B和C,则A的化学式为 。
(2)实验室检验B的方法是 。
(3)写出上述由I生成J的化学方程式: 。
(4)写出C和少量Na[Al(OH)4]溶液反应的离子方程式: 。
(5)若实验室要制备纯净的物质C(可含水蒸气)所需试剂最好选择 (填代号)。
A.石灰石
B.稀硝酸
C.稀硫酸
D.稀盐酸
E.纯碱
所需气体发生装置是 (填代号);所选装置中涉及的玻璃仪器的名称为______。
某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题:

(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:
、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
(5分)A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。其中D与水反应生成酸的名称为______________。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式__________。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的气体。写出④反应的离子方程式_______________。
(4)若A是制造整流器和太阳能电池的材料。C、D为钠盐,两种物质中除钠、氧外的另一种元素为同一主族,且溶液均显碱性。写出②反应的化学方程式__________。
(5)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。写出④反应的离子方程式___________。
下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质。反应①、②均为工业上的重要反应。

请回答下列问题:
(1)G是 ,K是 (填化学式)。
(2)C的原子结构示意图为 。
(3)写出B与C高温反应生成E和F的化学方程式: 。
(4)写出D与J的稀溶液反应生成G的离子方程式: 。