“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图3所示装置进行铜与稀硝酸的反应
| A.②③④ | B.①②③ | C.①②④ | D.①③④ |
下列叙述正确的是
| A.SO2具有还原性,故可作漂白剂 |
| B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C.浓硫酸具有吸水性,因此浓硫酸可以干燥某些气体 |
| D.Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中的Fe也显+3价 |
在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是
| A.Ca2+、Na+、NO3-、CO32- | B.Mg2+、Cl-、Al3+、SO42- |
| C.K+、Cl-、HCO3-、NO3- | D.Cl-、AlO2-、Na+、Fe3+ |
下列离子方程式正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+= Cu2+ + Fe2+ |
| B.Na与H2O反应制备H2: 2Na+2H2O==2Na++2OH-+H2↑ |
| C.将氯气溶于水:Cl2 + H2O= 2H+ + Cl- + ClO- |
| D.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
下列各组中的离子,能在溶液中大量共存的是:
| A.Na+、Cu2+、Cl-、SO42- | B.K+、H+、SO42-、OH-、 |
| C.Na+、H+、Cl-、CO32- | D.Na+、Ca2+、CO32-、NO3- |
设 NA为阿伏加德罗常数的数值,下列说法正确的是
| A.NA个CH4分子的质量为16g/mol |
| B.1mol/LNaCl溶液含有NA个Na+ |
| C.等物质的量的N2和CO所含分子数相同 |
| D.22.4LCO2中含有 NA个CO2分子 |
下列离子方程式正确的是
| A.用大理石跟稀盐酸制二氧化碳:CO32-+ 2H+=H2O + CO2↑ |
| B.Cu丝伸入到AgNO3溶液中: Cu + 2Ag+= Cu2+ + 2Ag |
| C.H2SO4溶液中滴入Ba(OH)2溶液:Ba2++ OH-+ H++SO42-=BaSO4↓+H2O |
| D.用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O |
CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2而得到。现以石墨为阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。电解开始不久,阴极区溶液呈红色,而阳极区溶液呈蓝色。对阳极区溶液呈蓝色的正确解释是 ( )
| A.2I--2e-=I2碘遇淀粉变蓝 |
| B.Cu-2e-=Cu2+Cu2+显蓝色 |
| C.2Cu+4I--4e-=2CuI↓+I2碘遇淀粉变蓝 |
| D.4OH――4e-=2H2O+O2O2将I-氧化为I2,碘遇淀粉变蓝 |
向含Al2(SO4)和AlCl3的混合溶液中逐滴加人1mol/L Ba(OH)2溶液至过量,加人Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
| A.图中C点铝元素存在形式是AlO2- |
| B.向D点溶液中通人C02气体,立即产生白色沉淀. |
| C.原混合液中c{Al2(SO4)3} :c(AlCl3)=1:2 |
| D.OA段反应的离子方程式为: 3Ba2+ +2Al3+ +8OH- +3SO42-=3BaSO4↓+2AlO2-+4H2O |
下列离子方程式书写正确的是
| A.NaHSO3溶液中投入过氧化钠粉末:4HSO3-+2Na2O2 = 4SO32―+O2↑+ 4Na+ |
| B.AlCl3溶液与烧碱溶液反应,当n(OH-)∶n(Al3+) = 7∶2时,2Al3+ + 7OH-= Al(OH)3↓+ AlO2- + 2H2O |
| C.Cl2与FeBr2溶液反应,当n(Cl2)∶n(FeBr2) = 1∶1时,2Fe2++ 4Br-+3Cl2 =" 2" Fe3++ 2Br2 + 6Cl- |
| D.向次氯酸钙溶液通入过量CO2:Ca2++ 2ClO一+ CO2 + H2O = CaCO3↓+ 2HclO |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说中正确的是( )
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| C.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| D.有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
| A.a=b |
| B.混合溶液的PH=7 |
| C.混合溶液中,c(H+)+ c(B+)= c(OH-)+ c(A-) |
D.混合溶液中,c(H+)= |
I2在KI溶液中存在下列平衡:l2(aq)+I-(aq) I3-(aq),c(I-3)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是( )
I3-(aq),c(I-3)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是( )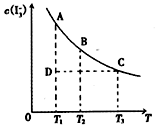
A.反应I2(aq)+I-(aq) I3-(aq)的△H<O I3-(aq)的△H<O |
| B.若温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1>K2 |
C.若反应进行到状态D时,一定有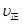 > >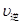 |
| D.状态A与状态B相比,状态A的c(I2)大 |
某溶液中含有的溶质是FeBr2、FeI2,若先向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,溶液变为红色,则下列叙述正确的是( )
①原溶液中的Br-一定被氧化;
②通入氯气之后原溶液中的Fe2+一定有部分或全部被氧化;
③不能确定通入氯气后的溶液中是否存在Fe2+;
④若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的I-、Fe2+、Br-均被完全氧化
| A.①②③ | B.②③④ | C.①③④ | D.①②③④ |
某学生用NaHCO3和KHCO3组成的某固体混合物进行实验,测得如下表数据(盐酸的物质的量浓度相等):
| 实验编号 |
① |
② |
③ |
| 盐酸体积 |
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
| m(混合物) |
9.2g |
16.56g |
27.6g |
| V(CO2)(标准状况) |
2.24L |
3.36L |
3.36L |
分析表中数据,下列说法不正确的是( )
A.由①可以计算出盐酸的物质的量浓度
B.由②、③可知:混合物质量增加,气体体积没有变化,说明盐酸已经反应完全
C.由①、②可知:①中的固体不足而完全反应
D.由①可以计算出混合物的NaHCO3的质量分数