下列是反应2A + 3B =" C" + 4D在不同时刻测得的速率,其中最快的是
A. V(A)=0.6mol/L.s B. V(B)=0.9mol/L.s
C. V(C)=0.4mol/L.s D. V(D)=1.0mol/L.s
在一可变容积的密闭容器中进行反应:C(s) + H2O(g)=" CO(g)" + H2(g),下列条件能使反应速率增大的是
| A.增加C的量 |
| B.将容器的体积缩小一半 |
| C.保持体积不变,充入N2,使体系的压强增大 |
| D.保持压强不变,充入N2,使容器的体积变大 |
在下列事实中,什么因素影响了化学反应的速率?
(1)黄铁矿煅烧时要粉碎成细小颗粒______________________;
(2)夏天的食品变霉,在冬天不易发生该现象
(3)同浓度同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢_____;
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速度不同______________________;
(5)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体________________。
对于可逆反应:H2(g)+I 2(g)  2HI(g),在温度一定下,从正方向开始发生反应,下列说法正确的是
2HI(g),在温度一定下,从正方向开始发生反应,下列说法正确的是
| A.H2的消耗速率与HI的生成速率之比为2:1 |
| B.反应进行的净速率是此时正、逆反应速率之差 |
| C.正、逆反应速率的比值是恒定的 |
| D.达到平衡时,正、逆反应速率相等 |
(共10分)某温度时,在2 L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示:
由图中数据分析求: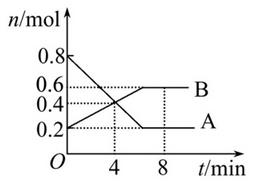
(1)该反应的化学方程式为 。
(2)反应开始 至4 min时,A的平均反应速率为 。(要求写出计算过程)
至4 min时,A的平均反应速率为 。(要求写出计算过程)
(3)第4min末时A、B的物质的量浓度依次为________、________。第4 min时,正、逆反应速率的大小关系为:v(正)________v(逆)(填“>”、“<”或“=”,下同),第8 min时,v(正)________v(逆)。
某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成Z,反应2min后,测得参加反应的X2为0.6mol/L,用Y2变化表示的反应速率v(Y2)= 0.1mol/(L?min),生成的c(Z)="0.4" mol/L,则该反应方程式为
A.X2+2 Y2 2XY2 2XY2 |
B.2X2+Y2 2X2Y 2X2Y |
C.3X2+Y2 2X3Y 2X3Y |
D.X2+3Y2 2XY3 2XY3 |
某温度下按右图安装好实验装置,在锥形瓶内盛有6.5g锌粒(颗粒大小基本相同),通过分液漏斗加入40ml2.5mol/L的硫酸,将产生的氢气收集在一个注射器中,用时10s时恰好收集到气体的体积为50mL(若折合成0℃、101kPa条件下的H2体积为44.8mL), 在该温度下,下列说法不正确的是:
| A.用锌粒来表示10s内该反应的速率为0.013g/s |
| B.忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率0.01mol/(L·s) |
| C.忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率0.01mol/(L·s) |
| D.用H2来表示10s内该反应的速率为0.004mol/(L·s) |
对于可逆反应2A(g)+B(g) 3C(g),在温度一定下由A(g)和B(g)开始反应,下列说法正确的是
3C(g),在温度一定下由A(g)和B(g)开始反应,下列说法正确的是
A. A(g)的消耗速率与c(g)的生成速率比为2:3
B. 由于该反应是等体积反应,所以增大压强正、逆反应速率不变
C. 正、逆反应速率的比值是恒定的
D.当反应达到平衡状态时,充入一定量的A时,v正(A)增大的同时v逆(C)也增大
要增大 Zn 和稀 H2SO4间置换反应的速率,下列措施正确的是
| A.使用高纯度的锌粒 | B.使用浓H2SO4 |
| C.使用小颗粒的锌粒 | D.使用浓HNO3 |
把100mL6mol/LH2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可以在反应物中加入适量的
| A.Na2CO3固体 | B.NaOH固体 |
| C.硫酸钾溶液 | D.硫酸钠固体 |
把0.4 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4 X(g)+5 Y(g)=n Z(g)+6 W (g)。2 min 末已生成0.3 mol W,若测知以Z的浓度变化表示的反应速率为0.05 mol/(L·min),
(1)则这2 min内v(X) = v(W) =
(2)2 min末时Y的浓度
(3)化学反应方程式中n的值是
(4)2min末时,已用去的X占原 来总物质的量分数为
来总物质的量分数为
用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程中产生二氧化碳的体积与时间的关系如图所示,下列叙述正确的是
| A.OE段化学反应速率最快 |
| B.EF段化学反应速率最快 |
| C.FG段收集的二氧化碳气体最多 |
| D.由图可推断出该反应是吸热反应 |
(10分)某化学研究性小组在用铝与稀硫酸的反应制氢气的实验时发现,如果把在空气中放置一段时间的5.0 g铝片放入圆底烧瓶中,然后通过分液漏斗加入500 mL 0.5 mol/L硫酸溶液,充分反应后,该小组同学根据记录数据得到了产生氢气的速率与反应时间的关系图象(如图所示) ,请你帮助该小组同学回答下列问题:
(1)曲线OA段不产生氢气的原因是_____________ _ ______
____________________ _____,
有关的离子反应方程式为_________________________ _____ _____
(2)曲线BC段产生氢气的速率突然加快的主要原因是
____________________________________________________________________________
(3)点C以后产生氢气的速率逐渐减小的主要原因是
____________________________________________________________________________
(4)从理论上分析该小组同学能收集到氢气的体积为(标准状况下)___________
在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.6 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末收集到氢气1.12 L(标况),在此之后,又经过4 min铁粉全部溶解。则:
(1)在前2 min内用FeCl2表示的平均反应速率是多少?
(2)在后4 min内用HCl表示的平均反应速率是多少?
(3)前2 min与后4 min相比,反应速率哪个较快?为什么?试解释原因。