(1) 12.4g Na2R中含Na+0.4mol,则Na2R的摩尔质量为 。
(2)有相同状况下的两种气体12C18O和14N2。若两种气体的质量相等,则12C18O和14N2气体所含质子数之比为 ;若两种气体的分子数相同,则12C18O和14N2的体积之比为 。
常温下,在27.9g水中溶解12.1g Cu(NO3)2·3H2O,恰好达到饱和,设该溶液密度为1.20g /cm3,求:
(1)该溶液中Cu(NO3)2的物质的量浓度。
(2)取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?若要使稀释后溶液中的Cu2+全部转化为单质铜,需要加入铁粉多少克?
(1)5.3g Na2CO3的物质的量为____________,将其配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为____________。取出该溶液10mL,在取出的溶液中通入HCl气体到不再产生气泡为止,共消耗____________mL HCl气体(标准状况)。
(2)V mL Al2(SO4)3溶液中,含有Al 3+ m g,则溶液中SO42-的物质的量浓度为_______。(用含有m、V的式子表示)
(1)0.5 mol CH4的质量为 ,约含有 个H,在标准状况下的体积为 。
(2)相同质量的CO和CO2,它们所含的原子数之比为 ,在同温同压下,它们的密度之比为 ;等物质的量的CO和CO2的混合气体的密度是相同条件下氢气密度的 倍。
(3)已知4gRO32-中核外电子数比质子数多6.02×10²²个,则R的摩尔质量为 。
(4)已知16 g肼(N2H4)含有的电子数为b,则阿伏伽德罗常数为 。(用含b的式子表示)
现有21.6g由CO和CO2组成的混合气体,在标况下其体积为13.44L。回答下列问题:
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的质量为
(3)将混合气体依次通过如下图所示装置,最后收集在气球中(实验在标况下测定)。
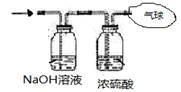
①气球中收集到的气体的摩尔质量为
②气球中收集到的气体中,电子总数为 (用NA表示阿伏伽德罗常数的值)
③气球的体积为___ 。
I.已知某气体单质R3在标况下的密度为ρg.L-1,阿伏伽德罗常数的值用NA表示,现有V L(标况下)该气体,用含有ρ、V、NA的代数式回答下列问题:
(1)该气体所含原子总数为 ;
(2)一个R原子的质量为 。
II.已知20℃时,NaCl在水中溶解度为Sg,此温度下的饱和溶液的密度为pg.cm-3,则20℃时该饱和溶液中溶质的质量分数为 ,溶质的物质的量浓度为 。
取质量为14.8 g的Na2CO3和NaHCO3的固体混合物,与100 mL 2.50 mol·L-1的盐酸恰好完全反应至不再放出气体。(提示:混合物中加入盐酸发生反应:Na2CO3+HCl===NaHCO3+NaCl,当消耗完碳酸钠时发生反应:NaHCO3+HCl===NaCl+H2O+CO2↑)
(1)求原混合物中Na2CO3的质量分数。
(2)若100 mL 2.50 mol·L-1的盐酸是用标签如图所示的浓盐酸制得,则需该浓盐酸的体积是多少?
(3)若取等质量的原混合物配成溶液,逐滴滴入90 mL2.50 mol·L-1的盐酸,并不断搅拌,求生成的气体在标准状况下的体积。
现有0.135 Kg质量分数为10%的CuCl2溶液,溶液体积为100mL。计算;
(1)溶液中CuCl2的物质的量;
(2)溶液中 Cl- 的物质的量浓度。
试回答下列问题:
(1) 9g 水的物质的量是________mol,含有_______mol 氢原子,含有__________个电子。
(2)等物质的量的SO2和SO3所含的原子个数之比是__________,质量比是__________。
(3)0.4mol NH3中所含氢原子数与__________克水中所含氢原子数相等。
(4)质量分数为49%的硫酸溶液,其密度为1.4 g/cm3,则其物质的量浓度为__________。
(5) 在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;若加入足量NaOH 并加热可得到c mol NH3,则原溶液中Al3+的物质的量浓度为_________。
在20℃时,将4.95gKNO3溶于10.0g水中,恰好配成密度为1.15g/cm3的饱和溶液,计算:
(1)此饱和溶液中KNO3的物质的量。
(2)此饱和溶液中KNO3的物质的量浓度。
将一定质量的Mg、Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。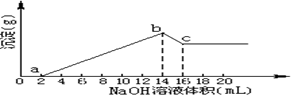
(1)求Mg,Al质量各是多少?考查镁铝化合物性质、混合物的计算,
(2)求盐酸的物质的量浓度为多少mol/L?
向200mlNaOH溶液中投入5.4gAl ,二者恰好完全反应,计算:
(1)参加反应的NaOH的物质的量浓度? (2)生成标况下氢气的体积?
(1)在100 mL 0.5 mol/L AlCl3溶液中,加入100 mL NaOH溶液,得到1.56 g沉淀,NaOH溶液的物质的量浓度 。
(2)某露置的苛性钠经分析含水:9%(质量分数,下同)、Na2CO3:53%、NaOH :38%。取此样品 10.00 g放入 100.00 mL 2.00 mol·L-1 的 HCl(aq) 中,过量的 HCl 可用 1.00mol/L NaOH(aq)中和至中性,蒸发中和后的溶液可得固体_______克。
将密度为1.84g/cm3、质量分数为98%的浓硫酸稀释成1000mL、物质的量浓度为2mol/L、密度为1.10g/cm3的稀硫酸。求:
(1)所需浓硫酸的体积;
(2)所需水的体积。(水的密度可视为1g/cm3)(要求有计算过程。)