填空:
(1)图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL。如果刻度A为4,量筒中液体的体积是______________mL。

图Ⅰ 图Ⅱ
(2)图Ⅱ表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_______________。
A.是a mL B.是(50-a) mL
C.一定大于a mL D.一定大于(50-a) mL
取100 mL 0.3 mol/L的硫酸注入500 mL容量瓶中,加水稀释至刻度线,该溶液中H+的物质的量浓度是
| A.0.06 mol/L | B.0.12 mol/L | C.0.03mol/L | D.0.24 mol/L |
体积为V(mL)、密度为ρ(g·cm-3)的溶液,含有摩尔质量为M的溶质质量为m(g),物质的量浓度为c,质量分数为w。下列表达式中不正确的是
A.c= |
B.m=V·ρ· |
C.w= |
D.c= |
设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.标准状况下,11.2L CH3CH2OH中含有分子的数目为0.5NA |
| D.常温常压下,2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.25 ℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA |
B.1 mol苯乙烯(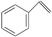 )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA |
| C.加热条件下,4.6 g金属Na与足量O2反应的产物中阳离子和阴离子总数为0.3NA |
| D.常温时,1 L 0.1 mol·L-1的硝酸铵溶液中,NH4+和H+总数为0.1NA |
下列溶液中Cl-浓度最大的是
| A.10ml 0.2mol/L的FeC13溶液 | B.10ml 0.1mol/L的AlC13溶液 |
| C.20ml 0.lmol/L的MgCl2溶液 | D.20ml lmol/L的KClO3溶液 |
下列说法正确的是
① 标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5molH2所占体积为11.2L
③标准状况下,1molH2O的体积为22.4L
④标准状况下,28gCO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L/mol
⑥标准状况下,体积相同的气体的分子数相同
| A.①③⑤ | B.④⑥ | C.③④⑥ | D.①④⑥ |
向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的 CO2后,再稀释到100mL。
(1)在 NaOH 溶液中通入一定量的 CO2后,溶液中溶质的可能组成是①NaHCO3 ②Na2CO3 ③NaOH、Na2CO3 ④______________。
(2)在稀释后的溶液中逐滴加入0.1mol/L的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示:

①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是 mL(标准状况)。
②原NaOH溶液的物质的量浓度为_________。
下列说法中错误的是
| A.从1 L 1mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1mol·L-1 |
| B.制成0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况) |
| C.0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D.10g 98%的硫酸溶液(密度为1.84 g·cm-3)与10 mL 18.4mol·L-1的硫酸溶液的浓度不相同 |
下列说法不正确的是
| A.1mol 氧气的质量为32g |
| B.常温常压下,1mol CO2气体体积约为22.4L |
| C.CO2的摩尔质量为44g/mol |
| D.1L 2mol/L的BaCl2溶液中含Cl-的个数为2.408×1024 |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.在常温、常压下,11.2L N2含有的分子数为0.5 NA |
| B.0.5 NA个氯气分子的物质的量是0.5mol |
| C.标准状况下,18g H2O的体积是22.4L |
| D.0.1 mol·L-1稀硫酸中含硫酸根个数为0.1NA |
关于浓度的关系,下列说法错误的是
A.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
B.新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.室温下,向0.01mol/LNH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)>c(ClO-)
D.物质的量浓度均为 的
的 和
和 混合溶液中,浓度可能的关系为:
混合溶液中,浓度可能的关系为:
c(Na+)>c(OH-)>c(HA)>c(HB)
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,3.4gH2O2含有极性键的数目为0.2NA |
| B.1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA |
| C.电解精炼铜时,若转移了NA个电子,则阳极质量减小32g |
| D.标况下,11.2LSO3所含的分子数目为0.5NA |