某物质A在一定条件下受热分解,产物都是气体,有关的化学方程式为:
 。若生成的混合气体对氘气的相对密度为d,则A的相对分子质量为( )
。若生成的混合气体对氘气的相对密度为d,则A的相对分子质量为( )
| A.2d | B.2.5d | C.5d | D.10d |
在①硫酸 ②芒硝 ③三氧化硫 ④硫酸亚铁四种化合物中,硫元素的质量分数由高到低的顺序是……( )
| A.①>②>③>④ | B.③>①>④>② | C.①>③>④>② | D.②>③>④>① |
(6分)用NaOH与Na2CO3·nH2O的混合物共28 g配制成100 mL溶液,测得该溶液中c(Na+)=4 mol·L-1。另取相同质量的上述混合物,加入足量的盐酸完全反应后,放出的气体在标准状况下的体积为3.36 L,试计算:
(1)原混合物中NaOH的质量分数。(2)Na2CO3·nH2O中的n值。
下列反应一定不会有气体产生的是……( )
| A.盐与碱溶液的反应 | B.盐与盐在碱溶液中的反应 |
| C.酸与碱在溶液里的中和反应 | D.非金属与氧组成的化合物与水反应 |
如果a克某气体中含有的分子数为b,则c克该气体在标准状况下的体积是(式中NA为阿佛加德罗常数)。
| A.22.4bc/aNA L | B.22.4ab/cNA L |
| C.22.4ac/bNA L | D.22.4b/acNA L |
某气球不充气时质量为m kg,当充入氦气达5000 m3时进行飞行(假设气球内外均在标准状况下),求气球能提起物体的最大质量。(空气的平均摩尔质量为29g/mol)
对下列化学反应从不同的角度进行分类:
①碳在氧气中燃烧;②硫在氧气中燃烧;③铁丝在氧气中燃烧;④铝粉在氧气中燃烧;⑤蜡烛在氧气中燃烧。
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是 ( )
| 编号 |
化学反应 |
离子方程式 |
评价 |
| A |
向硫酸铝溶液加入过量的氨水 |
Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
正确,氢氧化铝两性氢氧化物 |
| B |
碳酸钠溶液中滴加过量的盐酸 |
CO32-+2H+=" " CO2↑+H2O |
正确 |
| C |
石灰水反应滴加少量NaHCO3溶液 |
HCO3-+Ca2++OH-= CaCO3↓+H2O |
错误,不满足Ca(OH)2的配比 |
| D |
硫酸氢钠溶液与足量氢氧化钡溶液混合 |
2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O |
正确 |
下列物质的体积约为22.4L的是
| A.标准状况下1mol H2O | B.20℃、101 kPa时36.5g HCl |
| C.常温常压下17g NH3 | D.标准状况下0.4 mol H2和0.6mol O2的混合气 |
下列各项中表达正确的是( )
| A.白磷的分子式:P | B.Na+结构示意图是: |
| C.乙醇的结构简式C2H6O | D.HClO的电子式: |
下列各组物质关系中,与O2和O3关系相同的一组是( )
| A.Na和Na+ | B.S4和S8 | C. H和 H和 H H |
D.H2O和D2O |
用 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A. 中含有的原子数为 中含有的原子数为 |
B. 中含有的氢原子数为2 中含有的氢原子数为2 |
C.常温常压下,11.2L 中含有的分子数为0.5 中含有的分子数为0.5 |
D.1L0.1mol·L-1NaNO3溶液中含有的钠离子数为 |
计算题
取1.43g Na2CO3·XH2O 溶于水配成10ml 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0ml,并收集到112ml CO2(标况)。
求(1)稀盐酸物质的量浓度(2)Na2CO3·xH2O的摩尔质量(3)x值
将V1mL 1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )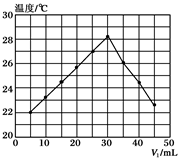
| A.做该实验时环境温度为22℃ |
| B.该实验表明化学能可能转化为热能 |
| C.NaOH溶液的浓度约为1.0mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
已知:2H2 ( g ) + O2 ( g ) = 2H2O ( l ); △H = -571.6kJ/mol
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ); △H = -890 kJ/mol
标准状况下,取甲烷和氢气的混合气体11.2 L完全燃烧后恢复到常温,放出的热量为203.32kJ,试求混合气体中甲烷和氢气体积比.