体积为VmL,密度为dg/cm3的溶液,含有式量为M的溶质m g,其浓度为C mol·L-1,
质量分数为w%,下列表示式中正确的是
A.c=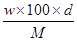 |
B.m=V×d×w |
C.w%= |
D.c= |
一定条件下磷与干燥氯气反应,若0.25磷消耗掉314
氯气(标准状况),则产物中
与
的物质的量之比接近于
| A. | 1:2 | B. | 2:3 | C. | 3:1 | D. | 5:3 |
在一定温度下向饱和Na2SO4溶液中加入ag无水硫酸钠粉末,搅拌,静置后析出bgNa2SO4·10H2O晶体,(b-a)g是 ( )
| A.原饱和溶液失去的水的质量 |
| B.原饱和溶液中减少的硫酸钠的质量 |
| C.原饱和溶液中失去的水和硫酸钠的总质量 |
| D.析出的晶体含有的硫酸钠的质量 |
你认为下列数据可信的是
| A.某溶液中溶质的质量分数超过100% | B.某常见气体的密度为1.8g/cm3 |
| C.某澄清石灰水的浓度是2.0mol/L | D.某元素的原子半径是0.160nm |
下列关于“变化”的说法中正确的是
| A.所有化学变化一定遵循质量守恒和能量守恒 |
| B.所有化学变化的能量都可以通过原电池转化为电能 |
| C.化学键的变化必然会引起能量变化,所以,能量变化也一定会引起化学变化 |
| D.化学变化定会引起物质种类变化,所以体系内物质种类变化一定发生了化学变化 |
下列说法正确的是
①热稳定性:HF>H2O>H2S ②离子半径:Na+>Mg2+>O2-
③碱性:Ca(OH)2>Mg(OH)2>NaOH
④相同物质的量浓度溶液的pH:NaOH>CH3COONa>NaCl
| A.①③ |
B.②④ |
C.①④ |
D.②③ |
下列叙述正确的是( )
| A.SO2的水溶液能够导电,但SO2是非电解质 |
| B.饱和氯水的导电性很好,所以氯气是强电解质 |
C. 和 和 为不同的核素,二者核外电子数不同 为不同的核素,二者核外电子数不同 |
| D.化合反应和分解反应一定属于氧化还原反应 |
下列物质的体积约为22.4L的是
| A.标准状况下1mol H2O | B.20℃、101 kPa时36.5g HCl |
| C.常温常压下17g NH3 | D.标准状况下0.4 mol H2和0.6mol O2的混合气 |
下列说法正确的是(NA表示阿伏加德罗常数的值)
| A.在常温常压下,11.2 L N2含有的分子数为0.5 NA |
| B.在常温常压下,1mol Ne含有的原子数为NA |
| C.71gCl2所含原子数为2NA |
| D.在同温同压下,相同体积的任何气体单质所含的原子数相同 |
依据物质的相关数据,可以推断物质的结构和性质。下列利用物质的相关数据作出的相应推断不合理的是
| A.依据元素的原子序数,推断该元素原子的核外电子数 |
| B.依据气体的摩尔质量,推断相同状况下不同气体密度的大小 |
| C.依据物质摩尔质量,推断物质熔、沸点的高低 |
| D.依据液体物质的沸点,推断用蒸馏法分离两种互溶液态物质组成的混合物的可行性 |
计算题
取1.43g Na2CO3·XH2O 溶于水配成10ml 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0ml,并收集到112ml CO2(标况)。
求(1)稀盐酸物质的量浓度(2)Na2CO3·xH2O的摩尔质量(3)x值
下列叙述正确的是 ( )
| A.发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B.金属阳离子被还原后,一定得到该元素的单质 |
| C.溶解度表示物质在一定温度下溶解的限度,其大小只与电解质的强弱有关 |
| D.绝大多数物质的溶解度都会因为温度的不同而发生变化 |
下列说法正确的是( )
| A.N2的摩尔质量为28g |
| B.17gNH3的物质的量是1mol |
| C.18gH2O在标准状态下体积是22.4l |
| D.将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L |