在室温下等体积的酸和碱的溶液,混合后pH一定等于7的是( )
| A.pH=3的硝酸和pH=11的Ba(OH)2溶液 | B.pH=3的盐酸和pH=11的氨水 |
| C.pH=3的硫酸和pH=11的KOH | D.pH=3的醋酸和pH=11的KOH溶液 |
根据事实,写出下列有关化学反应的符号表达式及其所属的基本反应类型
(1)点燃镁条做信号弹 属于 反应
(2)铁丝燃烧 属于 反应
(3)向过氧化氢中加入二氧化锰 属于 反应
(4)蜂窝煤中硫燃烧 属于 反应
(5)加热氯酸钾 属于 反应
下列变化属于物理变化的是
| A.水沸腾产生大量水蒸气 | B.木材燃烧 |
| C.钢铁生锈 | D.黑火药爆炸 |
①pH=2的CH3COOH; ②pH=2的HCl; ③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,不正确的是 ( )
| A.水电离的c(H+):①=②=③=④ |
| B.将②③两溶液等体积混合所得的溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.等体积的①②④溶液分别与足量铝粉反应,生成H2的量②最大 |
D.向溶液中加入100mL水后,溶液的pH:③>④> ②>① ②>① |
下列表达方式正确的是( )
A.CCl4的电子式: |
B.MgCl2的电子式: |
C.S2-的结构示意简图 |
D.中子数为20的氯原子:20Cl |
欲使0.1mol/L的稀氨水中,C(NH3·H2O)/C(OH-)逐渐减小,可采取的措施是:
| A.加入少量Al(OH)3固体 | B.加入少量NaOH晶体 |
| C.加入少量NH4Cl晶体 | D.继续加0.1mol/L的稀氨水 |
有下列比较中,正确的是 ( )
| A.溶解度:NaHCO3 >Na2CO3 |
| B.热稳定性:K2CO3>KHCO3>H2CO3 |
| C.与水反应的剧烈程度:Li>Na>K>Rb |
| D.同质量的Na2CO3和NaHCO3分别与足量稀硫酸反应,同温同压下产生CO2的体积:Na2CO3>NaHCO3 |
下列化学用语正确的是( )
| A.乙烯分子的结构简式:CH2CH2 | B.氯化镁的电子式: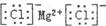 |
C.质量数为137的钡原子: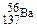 |
D.K+离子的结构示意图: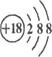 |
向体积为Va的0.05mol/L CH3COOH溶液中加入体积为Vb的0.05mol/LKOH溶液,下列关系错误的是:
| A.Va>Vb时:C(CH3COOH)+ C(CH3COO-)>C(K+) |
| B.Va=Vb时:C(CH3COOH)+ C(H+)="=" C(OH-) |
| C.Va<Vb时:C(CH3COO-)>C(K+)>C(OH-)>C(H+) |
| D.Va与Vb任意比时:C(K+)+C(H+)==C(OH-)+C(CH3COO-) |
设NA为阿伏加德罗常数,下列叙述中不正确的是
| A.1LpH=1的甲酸溶液中,H+数目为0.1 NA |
| B.标准状况下,3.36L乙醇中含有的分子数为0.15 NA |
| C.1 mol甲基(-CH3)所含电子数9NA |
| D.1L 1mol/L的FeCl3溶液所含的Fe3+数目为NA |
设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A.1mol甲基正离子(CH3+)所含电子数为8NA |
| B.NA个H2分子的质量约为2g,它所占的体积约为22.4L |
| C.标准状况下,11.2LCHCl3中所含的分子数为0.5N |
| D.500mL 0.5mol/L的Ca(ClO)2溶液中,含有ClO-的数目为0.5N |
往含有S2-和Cl-的稀溶液中逐滴加入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。则原溶液中c(S2-)/c(Cl-)的比值为:
| A.2V1/V2 | B.2(V2-V1)/V1 | C.2V2/V1 | D.V1/2(V2-V1) |
下列化学用语正确的是
A.镁离子的结构示意图: |
| B.乙酸乙酯的结构简式:C4H8O2 |
C.二氧化碳分子的电子式: |
| D.次氯酸钙的电离方程式:Ca(ClO)2=Ca2++2ClO一 |