下列叙述中,正确的是
| A.1s电子云界面图是一个球面,电子云中的每个小黑点代表一个电子 |
| B.NaH中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠形成的 |
| C.对于组成结构相似的分子,一定是相对分子质量越大,熔、沸点越高 |
| D.在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析 |
下列有关判断化学基本概念的依据中,一定正确的是
| A.离子晶体:由阴阳离子构成的晶体 |
| B.共价化合物:含有共价键的化合物 |
| C.酸性:PH<7 |
| D.强电解质:能溶于水的化合物 |
下列有关化学用语表示正确的是
| A.二氧化硅的分子式:SiO2 |
B.熔融状态下硫酸氢钾的电离方程式:KHSO4 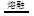 K++HSO4- K++HSO4- |
C.甲基的电子式: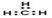 |
| D.HClO的结构式:H-Cl-O |
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
| A.NH4Cl=NH3↑+ HCl↑ | B.NH3+CO2+H2O=NH4HCO3 |
| C.2NaOH+Cl2=NaCl+NaClO+H2O | D.2Na2O2+2CO2=2Na2CO3+O2 |
下列各项中表达正确的是
A.NaCl的电子式: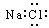 |
B.CO2的分子模型示意图: |
C.CrO5的结构式为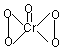 ,该氧化物中Cr为+6价 ,该氧化物中Cr为+6价 |
| D.次氯酸的结构式:H-Cl-O |
固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子电子层结构。则下列有关说法中错误的是
| A.1 mol NH5中含有5NA个N-H键(NA表示阿伏加德罗常数的值) |
| B.NH5中既有共价键又有离子键 |
C.NH5的电子式为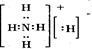 |
| D.它与水反应的化学方程式为NH5+H2O=NH3·H2O+H2↑ |
下列表示电子式的形成过程正确的是
A. |
B. |
C. |
D. |
下列物质中,存在非极性键的化合物的是
| A.NaOH | B.CH4 | C.H2 | D.Na2O2 |
下列每组中各物质内既有离子键又有共价键的一组是( )
| A.NaOH、H2SO4、(NH4)2SO4 | B.MgO、Na2SO4、NH4HCO3 |
| C.Na2O2、KOH、Na2SO4 | D.HCl、Al2O3、MgCl2 |
NH3分子的空间构型是三角锥形,而不是正三角形的平面结构,解释该事实的充分理由是
| A.NH3分子是极性分子 |
| B.分子内3个N—H键的键长相等,键角相等 |
| C.NH3分子内3个N—H键的键长相等,3个键角都等于107° |
| D.NH3分子内3个N—H键的键长相等,3个键角都等于120° |
下列描述正确的是( )
| A.CS2为V形极性分子 |
| B.SiF4与SO32-的中心原子均为sp3杂化 |
| C.C2H2分子中σ键与π键的数目比为1∶2 |
| D.水加热到很高温度都难分解是因水分子间存在氢键 |
以下微粒含配位键的是( )
①N2H5+ ②CH4 ③OH-④NH4+ ⑤Fe(CO)3 ⑥Fe(SCN)3 ⑦H3O+⑧[Ag(NH3)2]OH
| A.①④⑥⑦⑧ | B.③④⑤⑥⑦ | C.①④⑤⑥⑦⑧ | D.全部 |
根据价层电子对互斥理论,判断下列分子或者离子的空间构型不是平面三角形的是( )
| A.SO3 | B.BF3 | C.CO32- | D.PH3 |