A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体,而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、B、E的化学式:A_______________;B_______________;E_______________
(2)写出F和H反应的化学方程式 。
(3)按要求写方程式:
① 加热固体D发生反应的化学反应方程式 。
② C与足量盐酸反应的离子方程式 。
③ A溶液与金属铝反应的离子方程式 。
如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。

(1)若F是由Na+和SO42﹣组成的溶液,则甲的化学式是 ,列举A物质的一种用途 。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为 ,丁属于单质、酸、碱中的 ;在I溶液中加入氢氧化钠溶液,可以观察到的现象是 ,对应的离子方程式和化学方程式依次是 。
(3)写出G→A+C的化学方程式: 。
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目: 。
(5)若A中混有杂质Al2O3,除去杂质的方法是加入过量的NaOH溶液,该反应的离子方程式为。
(6)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1.则反应物中A、E、H2SO4的物质的量之比为 。
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。

(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 。将C长期露置于空气中,最后将变成物质D。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能用下图装置制取的气体,请结合所学知识,回答下列问题:

①写出实验室制取A的化学方程式 。
②收集A的方法是 ,验证A是否已经收集满的方法是:
(任写一种)。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,其中A在常温下能与水发生剧烈反应,B是目前使用最多的金属。物质之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙 ; F ;
(2)写出下列反应的离子方程式:
①金属A和水反应的离子方程式 。
②D和G的水溶液反应的离子方程式 。
(3)将G浓溶液逐滴加入到沸水中会产生一种红褐色的液体。你认为该液体中的分散质粒子直径在 之间,验证的简单方法是: 。
如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,B为液体,C能使湿润的红色石蕊试纸变蓝,由X受热分解生成的A、B、C的物质的量之比为1:1:1.

(1)写出下列各物质的化学式:D:______;F: 。
(2)写出X分解为A、B、C的化学方程式 。
(3)写出G→E变化的离子方程式 。
中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去)。下列推断正确的是( )

A.若A是CaC2,X是H2O,则Y一定是溴水
B.若A是金属钠,X是H2O,则E一定能还原Fe2O3
C.若Y是NaOH,C是白色沉淀,则A与X一定发生置换反应
D.若Y是氧气,D是氧化物,则A与X一定发生氧化还原反应
已知A、B、D、E、F、G、X、Y、Z满足下列转化关系。其中A、B、E为固体化合物,D、G为固体单质,F、X、Z为可燃性气体,F和X的燃烧火焰分别为蓝色和淡蓝色。

(1)写出E的名称:____________________________;
(2)B的电子式为 ;
(3)E生成Z的反应中用饱和食盐水的目的是 ;
(4)A和D反应的化学方程式:____ 。
A、B、C、D、E均为中学化学常见的纯净物,B为自然界中含量最多的液体,它们之间有如下的反应关系:

(1)常温下,若A为气态单质,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则该反应的化学方程式为: ,检验D中阴离子所用试剂为: 。
(2)若A为短周期的金属单质,D为气态单质,C溶液呈酸性或强碱性时,该反应都能进行。写出C溶液呈强碱性时反应的离子方程式: 。
(3)若A、C均为化合物,E为白色沉淀,C为引起温室效应的主要气体,写出E可能的物质的化学式(写两种): , 。
下图是中学化学中常见物质间的转化关系。其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体且1 mol E中含有 10 mol电子。乙和丁为黑色固体,将它们混和加热后发现固体由黑色变为红色。

(1)写出化学式:甲_________ ;乙________;丙_______;
(2)丁的摩尔质量为 。
(3)写出丙和E反应生成A和B的化学方程式: 。
(4)有学生将乙和丁混和加热后收集到标准状况下气体8.96 L ,测得该气体对氢气的相对密度为16,若将气体通入足量的澄清石灰水中,得到白色沉淀物 g。
某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下:

该同学得出的结论正确的是( )
| A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素 |
| B.根据现象2可推出该固体粉末中一定含有NaNO2 |
| C.根据现象3可推出该固体粉末中一定含有Na2SO4 |
| D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3 |
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )

A. 若A的单质,B和D的反应是OH-+HCO3-="=" H2O+CO32-,则E是一种清洁的能源
B. 若D为CO,C能和E反应,则A一定为Na2O2,其电子式是
C. 若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若X是Na2CO3,C为含极性键的分子,则A一定是氯气,且D和E能发生反应
下图为相关物质之间的转化关系,其中甲、乙为生活中常见的金属单质,丙、丁
在常温下为气态非金属单质,A~F为化合物(水均已略去)。

请回答:
(1)组成丙的元素在元素周期表中的位置 为 ;利用反应①,工业上常制备____(填产品名称)。
(2)C的电子式为____ ;反应②的离子方程式为 ____。
(3)将A、B的水溶液混合,反应的离子方程式为________。
(4)将B的稀溶液加水稀释,在图中画出溶液pH随加水体积的变化趋势曲线。

(5)工业上冶炼金属甲的化学方程式为__ __。
(6)将等物质的量的A和NaOH混合溶于水,该溶液中各离子的物质的量浓度由大到小的顺序为 。
(7)检验F中阳离子的方法为__ __
A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:____________________________________________________________。
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为_____________________________________。
②X可能为__________________(填代号)。
A.NaHCO3 b.Na2CO3 C.Na2SO3 D.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为_____________。
②若X为非金属单质,通常为黑色粉末,写出E的化学式______________。
③若X为一种造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为______(填代号)。
A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。
①A与H2O反应的化学反应方程式为__________________________________。
②检验溶液D中还可能存在Fe2+的方法是_________________________________(注明试剂、现象)。
A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体。E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶水成为无色溶液,G溶于水得黄棕色溶液。这九种物质间反应的转化关系如图所示

(1)写出四种单质的化学式
A________ B_______ C______ D______
(2)写出H+B→G的离子方程式 ;
(3)写出G+I→H+D+E的化学方程式 ;
(4)某工厂用B制漂白粉。
①写出制漂白粉的化学方程式 。
②为测定该工厂制得的漂白粉中有效成分的含量,某该小组进行了如下实验:称取漂白粉3.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸(此时发生的离子方程式为: ),静置。待完全反应后,用0.2mol·L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2 =Na2S4O6+2NaI,共用去Na2S2O3溶液20.00mL。则该漂白粉中有效成分的质量分数为 保留到小数点后两位)。
I:A、B、C、D均为中学化学中常见的物质,它们之间转化关系如下图(部分产物已略去):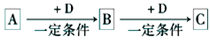
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________(填元素符号)
(2)若D是金属,C溶液在储存时应加人少量D,其理由是(用必要的文字和离子方程式表示)_______________________.
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_______________________。
化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E的混合物投人500m1稀硫酸中,固体全部溶解并产生气体。待反应完全后.向所得溶液中加人NaOH溶液,生成沉淀的物质的是与加入溶液的体积关系如下图所示:
则固体混合物中Mg的质量为_____________;NaOH溶液的物质的量浓度为___________。
II某一离子反应体系有反应物和产物共以下六种:MnO4—、H+、O2、H2O、H2O2、Mn2+。已知该反应中的H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是___________。
(2)该反应中.发生还原反应的过程是_____→_____。
(3)溶液随着酸性的增强氧化性不断增强,应选择__________(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(4)如反应转移了0.6mo1电子,则产生的气体在标准状况下体积为__________。