下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、D是金属单质,L为红褐色沉淀,E为食盐的主要成分,I的水溶液呈强酸性。
(1)写出反应①的化学方程式:______________________________________。
(2)写出反应②的离子方程式:______________________________________。
(3)向M溶液中加入足量的I溶液反应的离子方程式为______________________。
(4)写出一个由化合反应生成L的化学方程式______________________________。
已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30。A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去)。其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取。D为烃,不能使酸性高锰酸钾溶液褪色。E、G为生活中常见的有机物,且E有特殊香味,H有香味。
(1)写出下列各物质的官能团的名称:
A ___________;F ___________;G___________。
(2)按要求写出下列各步变化的化学方程式(注明反应条件)
反应①_____________________________________________________;
反应④_____________________________________________________;
反应⑦ _____________________________________________________。
(3)写出下列反应类型:
反应① ___________,反应②___________,反应④___________,反应⑦___________。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出气体丙的电子式
(2)写出反应①的化学方程式
反应③的离子方程式:
反应⑤的离子方程式:
(3)若在F溶液中加入D溶液,并露置于空气中,能观察到的现象是 。
某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为红褐色沉淀。
(此转化关系中所用的试剂都是足量的)
(1)写出下列物质的化学式:F ,G 。
(2)D→E的转化中,加入过量的X可能是 。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(3)写出下列转化的化学方程式:
A→C: ;
H→I: 。
下图中A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,已知B、D为常温下气态化合物,C为常温下液态化合物,图中有部分生成物未标出。
请填写以下空白:
(1)A的化学式 。
(2)写出下列反应的化学方程式:
A→B+C+D _______________________________D→ H ___________________。
I→J _______________________________________________。
(3)写出在溶液中A+NaOH→D完全反应的离子方程式:______________________________________。
A—J均为中学化学中常见物质,C、D、G、H、I常温下均为气体,且G为单质,C常参加光合作用,其中H和I为大气污染物,E为常见的无色液体。F的焰色反应为黄色,反应①、②、③为工业反应。固体A是一种化肥,产物C、D、E的物质的量之比为1:1:1。它们之间的转化关系如下图:
(1)写出A的化学式 ,B的电子式为 ,B中含有的化学键类型是 。
(2)写出反应①的化学方程式 。
(3)少量J溶液加入F的水溶液中发生反应的离子方程式为 。
(4)氯气遇到D会产生大量白烟,常用D的浓溶液检验氯气管道是否漏气。其发生反应化学方程式为 。
(5)将G和I的混合气体60 mL通入水中,充分反应后余下气体10 mL(在相同条件下测定),则混合气体中G和I的体积比为 。
下图中的B~K分别代表有关反应的一种反应物或生成物,其中A、C、F、K是固体;E是常见的气体单质而I是红棕色的气态氧化物。固态物质A加热后生成的气体混合物若通过碱石灰只剩余气体B,若通过浓硫酸则只剩余气体D。各物质间的转化关系如下图所示: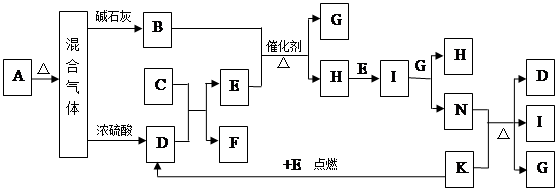
请回答下列问题:
(1) 写出实验室检验A物质中含有的阳离子的方法 。
(2) B与E反应得到1molH,则此时转移电子的物质的量为 mol。
(3) 写出实验室制取B的化学方程式 。
(4) 写出N的稀溶液与过量的铁粉反应的离子方程式 。
(5) 若混合气体通过碱石灰得到的气体B与通过浓硫酸得到的气体D的物质的量之比是8∶5,则用物质的量的关系表示此固体A的组成为 。
图所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图
所示。
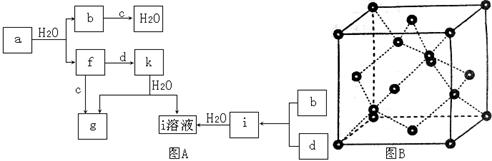
回答下列问题:
(1)图对应的物质名称是,其晶胞中的原子数为,晶体类型为。
(2)d中元素的原子核外电子排布式为。
(3)图中由二种元素组成的物质中,沸点最高的是,原因是,该物质的分子构型为,中心原子的杂化轨道类型为。
(4)图中的双原子分子中,极性最大的分子是。
(5)k的分子式为,中心原子的杂化轨道类型为,属于分子(填"极性"或"非极性")。
已知A、B、C为金属单质,甲、丙为无色气体,乙为黄绿色气体,D、E、F、G、H为中学常见的化合物,其中H为红褐色沉淀,它们之间能发生如下反应(图中的产物和条件未全部标出)
根据推断结果回答下列问题:
(1)写出下列物质的化学式:B ,丙 ;
(2)写出③的化学方程式: ;
(3)写出⑤的离子方程式: ;
(4)F与D反应后的产物在空气中转化为H的化学方程式为:
;现象为
。
有一包固体粉末(纯净物),可能含有下列阳离子和阴离子中的若干种:K+、Cu2+、Mg2+、Cl-、SO42-、CO32-,为确定其成分进行如下实验:取少量固体,加适量蒸馏水,搅拌后固体全部溶解,得到无色透明溶液。
②向①形成的溶液中加入NaOH溶液无明显变化。
③再取少量固体,加入稀硝酸,搅拌后固体全部溶解,无气体放出。
试根据以上实验现象判断:
(1)这包粉末中一定不含有的离子是 ;
(2)这包粉末可能是:______________________;为进一步确定该物质的实验操作和现象:
。
A、B两种液态有机物均由碳、氢、氧三种元素组成,物质A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与Na2CO3溶液混合时冒气泡。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能跟钠反应放出氢气,不能与Na2CO3溶液反应。请填空:
(1)A的结构简式为 ,B的结构简式为 。
(2)写出B与Na反应的化学方程式 。
(3)写出A与B反应的化学方程式 。
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)。
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为________,反应④的化学方程式为______________________________________________。
若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行。反应②也在水溶液中进行,其离子方程式是____________________________________________,
写出反应④的化学方程式:____________________。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为_____________________________________________。
已知A~O各代表一种物质,除O外其余物质均由短周期元素组成,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2︰3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
请回答下列问题:
(1)组成B单质的元素位于周期表第 周期,第 族。化合物C和D的电子式为 ___ 、_____________。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是 。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:
(4)写出D与足量的N反应生成E和F的化学方程式: 。
写出G与F加热反应生成K、I和J的化学方程式: 。
(5)上图中在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有 个。
A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的―1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是第______周期______族。
(2)画出D元素的原子结构示意图____________。
(3)与E的氢化物分子所含电子总数相等的分子是____________(举一例、填化学式,下同)、离子是____________。
(4)A与C形成的化合物中含有化学键的类型是____________。
(5)用电子式表示BD的形成过程________________________________
分X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知:①X可分别与Y、W形成X2Y,X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。请回答:

(1)Z2Y的化学式是 。
|
(2)Z2Y2与X2Y反应的化学方程式是 。
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:C(I)的电极名称是_________(填写正极或负极);C(II)的电极反应式是 。