往100mL pH=0的硫酸和硝酸混合液中投入3.84g铜粉,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
化学是一门以实验为基础的学科。
(1)下列实验操作的描述中,正确的是________(填序号)
①为使稀硫酸和锌制取氢气的反应速率加快,可向稀硫酸中加入用铜丝网包裹的锌粒
②粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌漏斗中的液体
③配制一定物质的量浓度的溶液时,容量瓶洗涤后不用进行干燥
④蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶壁
⑤可以在试管中加热氯化铵固体制备少量氨气
⑥盛放石灰水的试剂瓶内壁常有一层白色固体物质,可用稀硫酸清洗除去
(2)下列叙述中正确的是 (填序号).
| A.分液漏斗、滴定管和容量瓶使用前必须检查是否漏水 |
| B.将碘水倒入分液漏斗,再加适量乙醇,充分振荡、静置,可从碘水中萃取碘 |
| C.洁净的铁钉在食盐水中浸泡一段时间,铁钉上有气泡,说明铁发生了析氢腐蚀 |
| D.铁丝在氯气中剧烈燃烧,火星四射,生成黑色固体 |
E.酸碱中和滴定实验中,锥形瓶用蒸馏水洗净后直接使用,而滴定管用蒸馏水洗净后,必须润洗后使用
(3)用铜片与稀硝酸反应制取NO气体,如图装置中适合的是 (填图甲或图乙);装置B中的试剂最好是 ,该装置的作用是

为了避免NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:2NO2+2NaOH═NaNO3+NaNO2+H2O;NO2+NO+2NaOH═2NaNO2+H2O).现有由1mol NO、2mol NO2、1mol N2O4组成的混合气体恰好被1L氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为
| A.3 mol/L | B.4 mol/L | C.5 mol/L | D.6 mol/L |
向21.6 g铁粉和铜粉的混合物中加入1 L 1 mol·L-1硝酸溶液,充分反应,放出NO气体且金属有剩余。则反应后溶液中c(NO3-)可能为(忽略溶液体积的变化)
| A.0.45 mol·L-1 | B.0.6 mol·L-1 | C.0.75 mol·L-1 | D.0.9 mol·L-1 |
取4.6 g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生4480 mL的 NO2气体和336 mL的N2O4气体(都已折算到标准状况),在反应后的溶液中加入足量的氢氧化钠溶液,生成沉淀的质量为
| A.9.02g | B.8.26g | C.8.51g | D.7.04g |
氢气是化工行业重要原料之一。
(1)电解饱和食盐水是生产H2的方法之一。常温下,电解250 mL饱和食盐水一段时间后,溶液质量减轻0.365 g(假设气体全部逸出)。生成的氢气在标准状况下的体积为 mL。
(2)在电弧炉中,甲烷裂解产生乙炔和氢气,若1 m3 甲烷经此过程生成0.27 m3氢气,则甲烷的裂解率为 %(体积均在相同条件下测定)。
(3)已知:CxHy + H2O → CO + CO2 + H2(未配平)。工业上用甲烷、乙烷的混合气体利用上述反应生产氢气,反应后气体经干燥组成如下表所示:
| 组分 |
CO |
CO2 |
H2 |
| 体积分数 |
20% |
5% |
75% |
计算原混合气体中甲烷与乙烷的物质的量之比。
(4)合成氨生产过程中,消耗氮氢混合气2000 m3(其中CH4的体积分数为0.112%,下同),分离液氨后的氮氢混合气中含CH4 2.8%。计算分离出液氨为多少吨(保留2位小数,所有体积均已折算至标准状况)。
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定。试确定A、B、C、D、X各代表何种溶液,把对应物质的化学式填入下列空白:
A:_______,B:________,C:_______,D:_______,X:_______。
向含有0.8 mol的稀硝酸中慢慢加入22.4 g的铁粉,假设反应分为两个阶段。
第一阶段为:Fe+HNO3(稀)→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段: 。
第二阶段: 。
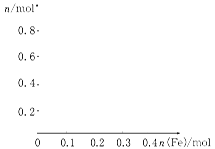
(2)在图中画出溶液中Fe2+、Fe3+、NO3-的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)。
下图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。

(1)若锥形瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞:
① 锥形瓶内产生的气体主要有(写化学式) 。
② 用产生的气体做氨的催化氧化实验,各仪器装置按气流方向从左到右连接顺序是(填字母)( )→( )→( )→E
③试管B中的现象为 ,反应方程式为 。
(2)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末。
①此实验的目的是 ,
D装置的作用是 。
②为了使B中CuO反应充分,在不改变现有药品的条件下,可采取的方法有 。(写出一种即可)
③加热前必须进行的操作是 。
某稀溶液中含有Fe(NO3)2、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为( )

| A.1:1:1 | B.1:3:1 | C.3:3:8 | D.1:1:4 |
氮元素在自然界中存在多种价态,结合题干回答下列问题:
23.氮元素原子核外有 个未成对电子,最外层有 种能量不同的电子。
24.氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是 (填编号)。
a.NH3比PH3稳定性强
b.氮气与氢气能直接化合,磷与氢气很难直接化合
c.硝酸显强氧化性,磷酸不显强氧化性
d.氮气常温是气体,磷单质是固体
25.已知,氯胺NH2Cl熔点-66℃,NH4Cl熔点340℃,氯胺的电子式为 ,从物质结构的角度解释两者熔点相差较大的原因 。
26.NH2Cl比HClO稳定性高,易水解,因水解后能产生可杀菌消毒的物质而成为饮用水的缓释消毒剂,NH2Cl发生水解的化学方程式为 。
27.工业上利用铝粉除去含氮废水中的NO3-,当控制溶液pH在10.7左右时,反应过程中生成AlO2-、氮气和氨气,若氮气和氨气的体积比为4:1,则还原剂和氧化剂的物质的量之比为 ,若氮气和氨气的体积比为1:1,则除去0.1mol NO3-,消耗铝______g。
“封管实验”具有简易、方便、节约、绿色等优点,观察下列四幅图(夹持装置未画出),判断下列说法正确的是 ( )


| A.加热时,a上部聚集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.在惰性电极e和f附近分别滴加紫色石蕊试液,e电极附近呈红色,f电极附近呈蓝色 |
向一定体积含HC1、H 2SO 4、NH 4NO 3、A1C1 3的混合溶液中逐滴加入Ba(OH) 2溶液,溶液中产生沉淀的物质的量与加入Ba(OH) 2溶液的体积关系正确的是

“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差 |
| B.加热时,②、③中的溶液均变红,冷却后又都变为无色 |
| C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
| D.四个“封管实验”中都有可逆反应发生 |