(8分)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_______ __ ___。
(2)若溶液M由10 mL 2 mol·L-1 NaHA溶液与2 mol·L-1 NaOH溶液等体积混合而得,
则溶液M的pH_ __7(填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为_ _ __。
(3)若溶液M有下列三种情况:
①0.01 mol·L-1的H2A溶液
②0.01 mol·L-1的NaHA溶液
③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液,
则三种情况的溶液中H2A分子浓度最大的为______;pH由大到小的顺序为______。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液c(H+)/c(OH-)=104,V1与V2的大小关系为________(填“大于、等于、小于”或“均有可能”)。
(本题共12分)Na2S2O3、Na2S、Na2SO3等含硫化合物在工业上有广泛的用途。
完成下列填空:
28.若将Na2S2O3中的硫元素看作为+2价,下列反应中与Na2S2O3+H2SO4(稀) → Na2SO4+S↓+SO2↑+H2O属于同一类型的是_______(填序号)。
a.2H2S+SO2→ 3S↓+2H2O
b.3NaClO 2NaCl+NaClO3
2NaCl+NaClO3
c.S+2H2SO4(浓)  3SO2↑+2H2O
3SO2↑+2H2O
d.4P+3NaOH+3H2O → 3NaH2PO2+PH3↑
29.棉织物用氯气漂白后,加入Na2S2O3除去余氯时,发生如下反应:
____S2O32―+____Cl2+________ → ___SO42―+___Cl―+___H+
完成并配平该反应方程式;若反应中生成0.2 mol SO42―,则转移电子___________mol。
30.下图是Na2SO3溶液中各离子浓度的相对大小关系示意图。其中,②是_______,④是______(填微粒符号)。
31.已知Na2S溶液显碱性,其主要原因是_________________(用离子方程式解释)。往装有Na2S溶液的烧杯中加入足量的ZnCl2溶液,产生白色的ZnS沉淀;再向烧杯中滴加CuCl2溶液,沉淀转变为黑色。请用溶解平衡原理解释上述现象______________________________________。
泡沫灭火器的工作原理就是我们学习的盐类水解,它是彻底的双水解,
(1)灭火器有两个桶构成,一个是外面的钢桶,用来盛装 (硫酸铝、碳酸氢钠填药品的化学式)一个是里面看不到的塑料桶,用来盛装 。(同上)
(2)用离子方程式表示塑料桶盛放该试剂的原因 。
(3)用离子方程式表示其工作原理 。
(4)用碳酸氢钠而不用碳酸钠做灭火器的药品其原因是 。
(5)碳酸氢钠溶液中质子守恒的表达式是 。
(本题共12分)
27.硫元素位于元素周期表第____列;硫元素原子核外有2个未成对电子,这2个电子所处亚层的符号是_______;硫、氯元素的原子均可形成与Ar原子电子层结构相同的简单离子,且硫离子的半径更大,请解释______________________________________。
28.S8和P4的分子中都只有共价单键,若P4分子中有6个P-P键,则可推断S8分子有________个S-S键;
己知:H-S键键能:339 kJ/mol; H-Se键键能:314kJ/mol。以上键能数据能否比较S,Se非金属性的强弱_______(选填“能”、“否”;下同);能否比较H2S、H2Se沸点的高低_______。
29.在25℃,Na2SO3溶液吸收SO2得到的NaHSO3溶液中c(SO32-)>c (H2SO3),据此断NaHSO3溶液显_____性。
30.在25℃,Na2SO3溶液吸收SO2后,若溶液pH=7.2,则溶液中c(SO32- )=c(HSO3-);若溶液pH=7,则以下浓度关系正确的是(选填编号)_____________________。
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)> c(HSO3-)> c(SO32-)>c(H+)= c(OH-)
c.c(Na+)+ c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
31.己知Na2SO3溶液中存在水解平衡:SO32-+H2O HSO3-+OH-,请用Na2SO3溶液和a试剂及必要的实验用品,设计简单实验,证明盐类的水解是一个吸热过程。a试剂是________,操作和现象是___________.
HSO3-+OH-,请用Na2SO3溶液和a试剂及必要的实验用品,设计简单实验,证明盐类的水解是一个吸热过程。a试剂是________,操作和现象是___________.
Ⅰ.在一个容积固定为2L的密闭容器中,发生反应:aA (g) + bB(g)  pC(g) ,△H=?,反应情况记录如下表:
pC(g) ,△H=?,反应情况记录如下表:
| 时间/(min) |
n(A)/( mol) |
n(B)/( mol) |
n(C)/( mol) |
| 0 |
1 |
3 |
0 |
| 第2 min |
0.8 |
2.6 |
0.4 |
| 第4 min |
0.4 |
1.8 |
1.2 |
| 第6 min |
0.4 |
1.8 |
1.2 |
| 第8 min |
0.1 |
2.0 |
1.8 |
| 第9 min |
0.05 |
1.9 |
0.3 |
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率v(A)= mol•L-1• min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8 min时分别改变了某一个反应条件,则改变的条件分别可能是:
①第2min 或 ;
②第6min ;③第8 min 。
(3)若从开始到第4 min建立平衡时反应放出的热量为235.92kJ则该反应的△H= 。
(4)反应在第4 min建立平衡,此温度下该反应的化学平衡常数K= 。
(5) 判断第9 min时是否达平衡,说明理由 。
Ⅱ.已知:常温下,A酸的溶液pH=a, B碱的溶液pH=b
(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为 。
A.大于7 B.等于7 C.小于7
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为 mol•L-1,B溶液中水电离出的氢离子浓度为 mol•L-1。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为: 。
将0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则:
(1)混合溶液中c(A-)________c(HA)(填“>”“<”或“=”,下同)。
(2)混合溶液中c(HA)+c(A-)________0.1 mol·L-1。
(3)混合溶液中,由水电离出的c(OH-)________0.2 mol·L-1 HA溶液中由水电离出的c(H+)。
(4)25 ℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
草酸(H2C2O4)是二元中强酸,酸性KMnO4溶液能与草酸(H2C2O4)溶液反应。
Ⅰ、某探究小组利用该反应,用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸。
(1)写出滴定过程中发生反应的离子方程式为 。
(2)滴定过程中操作滴定管的图示正确的是 。
(3)本滴定达到终点的标志是: ;
(4)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度 ,(填“偏高”、“偏低”、或“不变”)。
Ⅱ、草酸氢钠溶液显酸性,常温下,向10 mL 0.01mol/LNaHC2O4溶液中滴加0.01mol/LNaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是: 。
| A.V(NaOH)=0时,c(H+)= 1×10-2 mol/L |
| B.V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
| C.V(NaOH)=10mL时,c(H+)= 1×10-7 mol/L |
| D.V(NaOH)>10mL时, c(Na+)> c(C2O42-)> c(HC2O4-) |
铜合金及铜的氯化物在生产生活中有着广泛的应用。请回答下列问题:
(1)向硫酸铜、氯化钠混合溶液中滴加亚硫酸钠溶液生成CuCl沉淀,实验测得溶液的pH与亚硫酸钠溶液体积的关系曲线如图所示。
①用离子方程式解释亚硫酸钠溶液呈碱性的原因: 。
②用离子方程式解释图像中V<a时溶液酸性增强的原因: 。
当V>a时,随着亚硫酸钠溶液的体积增大,溶液pH增大的原因是 。
(2)已知:Ksp(AgCl)=8×10-10,Ksp(CuCl)=1.2×10-6。向CuCl 浊液中滴加硝酸银溶液,发生反应CuCl(s)+Ag+(aq) AgCl(s)+Cu+(aq),该反应平衡常数K= 。
AgCl(s)+Cu+(aq),该反应平衡常数K= 。
(3)硫酸铜溶液中含少量硫酸铁,加入氢氧化铜,过滤,除去三价铁离子,写出加入氢氧化铜时发生反应的离子方程式: 。
(4)测定CuCl和CuCl2混合物中CuCl含量的原理为用氯化铁溶液溶解样品,以邻菲罗啉作指示剂,用Ce(SO4)2溶液滴定至终点,滴定反应为Ce4++Fe3+=Fe2++Ce3+。氯化铁与氯化亚铜反应的离子方程式为 。
I常温下,浓度均为0.1molL-1六种溶液的PH如表所示:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
Na2SO4 |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
7.0 |
请回答下列问题:
(1)上述盐溶液中的阴离子,结合质子的能力最强的是 。
(2)将CO2气体通入 饱和的碳酸钠溶液中,可以观察到的现象为 (结合离子方程式加以描述)。
(3)要增大氯水中的HClO的浓度,可向氯水中加入少量的碳酸钠溶液,用离子方程式解释原因 。
II、已知:25ºC时,A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,酸碱按体积比为1:10混合后溶液显中性,则a+b= 。
(2)若A为醋酸,B为氢氧化钠,且a+b=14,用体积为VA的醋酸和体积为VB的氢氧化钠溶液混合后,溶液显中性,则其体积关系VA VB。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为 。
(1)在25℃条件下将pH=10的氨水稀释10倍后溶液的pH为(填序号)________。
A.9 B.11 C.9~10之间 D.9~11之间
(2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,溶液pH_________(填“增大”、“减小”或“不变”),主要原因是________________。
(3)已知某溶液中只存在NH4+、H+、OH-、Cl-四种离子,该溶液中各离子浓度大小顺序可能有如下几种关系:
A.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
①上述离子浓度大小关系不可能的是_________(填序号)。
②若溶液中只溶解了一种溶质,则该溶质是____________,上述离子浓度大小顺序关系中正确的是(选填序号)________________。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) ________ c(NH3·H2O)(填>、<或=)
(4)25℃时,如果将0.1molNH4Cl和0.05molNaOH溶于水,形成混合溶液,(假设无气体逸出损失),则NH4+和NH3·H2O两种粒子的物质的量之和等于________mol。
I.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如下图:
①从图中推断NaH2PO4溶液呈 性(填“酸”、“碱”或“中”),这说明 。
②在Na3PO4溶液中,c(Na+)/c(PO43—) 3(填“>”“=”“<”);向该溶液中滴入几滴浓KOH溶液后,c(Na+)/c(PO43-)的值减小,原因是 。
③羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料,有关反应为:
5Ca(OH)2+3H3PO4=Ca5(PO4)3OH+9H2O。下图是生产羟基磷灰石时得到的实验曲线,请计算磷酸的初始浓度为0.70mmol/L,pH=10.0条件下,反应前10min内磷酸的沉淀速率 。
II. 在某温度下,把1.0mol NH3溶于水中配成1L溶液,测得溶液中OH-浓度和时间的图像如下:
①求该温度时,氨水的电离平衡常数K(写出计算过程,结果保留三位有效数字)
②在t1时刻时再加入H2O配成2L溶液,在t2时刻时重新达到平衡,请在坐标系中画出t1~t2时间内OH-浓度随时间变化的曲线。
③将a mol/L的盐酸和b mol/L氨水等体积混合,所得溶液呈中性(忽略混合前后溶液体积的变化),则混合后溶液中:c(NH3·H2O)= 。(用含有a、b的式子表示)
I. 对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。下表为几种弱酸在25℃时的电离平衡常数
| 酸 |
电离平衡常数K |
| CH3COOH |
1.76×10-5 |
| H2CO3 |
K1=4.3×10-7 K2=5.61×10-11 |
| H3PO4 |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
回答下列问题:
(1)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是_________,最弱的是________。
(2)等浓度的下列溶液中由水电离出的OH-浓度由大到小的顺序是__(用序号作答)
①CH3COONa ②NaH2PO4 ③NaHPO4 ④NaHCO3 ⑤Na2CO3
(3)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的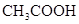 的电离转化率为a,则该温度下醋酸的电离平衡常数KCH3COOH=_____。
的电离转化率为a,则该温度下醋酸的电离平衡常数KCH3COOH=_____。
II.已知t℃时,Kw=1×10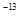 ;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=________。
;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=________。
III.现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:
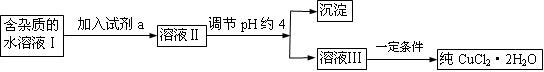
25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀pH |
2.7 |
7.6 |
4.7 |
| 完成沉淀pH |
3.2 |
9.7 |
6.7 |
请回答下列问题:
(1)流程中加入的试剂a最合适的是_____________(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是 。
(2)调节pH约4应该加入的物质可以是 。
A.CuO B.CuCl2 C.Cu(OH)2 D.NaOH
利用平衡移动原理简述加入该物质的理由 。
(3)最后能不能直接蒸发结晶得到CuCl2·2H2O?__________(填“能”或“不能”)。如不能,应如何操作?(若能,此空不填) 。
(一)对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。下表为几种弱酸在25℃时的电离平衡常数
| 酸 |
电离平衡常数K |
 |
 |
 |
  |
 |
   |
回答下列问题:
(1)K只与温度有关,当温度升高时,K值____(填“增大”、“减小”、“不变”)。
(2)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是_________,最弱的是________。
(3)对于同一种多元弱酸,有不止一个电离平衡常数,多个常数K1、K2、K3、之间存在某种大小关系,此关系是________________;以碳酸为例,用离子方程式和必要的文字说明产生此规律的原因_________________________。
(4)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的 的电离转化率为____,则该温度下醋酸的电离平衡常数
的电离转化率为____,则该温度下醋酸的电离平衡常数 _____。
_____。
(二)化合物SOCl2是一种液态化合物,沸点77 ℃。在盛有10 mL水的锥形瓶中,小心地滴加8~10滴SOCl2,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出。该气体可使滴有品红试液的滤纸褪色。
(1)写出SOCl2和水反应的化学方程式:_____________________________。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是 ;用SOCl2与AlCl3·6H2O混合共热得到无水AlCl3,原因是________________________ 。
某溶液经检测只含有NH4+、Cl-、H+、OH-四种离子,
(1)若该溶液中只有一种溶质,则该溶质是 (写化学式)。
(2)若该溶液呈中性,则溶液中c(NH4+) c(Cl-)(填“>”、“<”或“=”),此时溶液中的溶质有 。
(3)若该溶液由0.02mol·L-1HCl与0.01mol·L-1NH3·H2O等体积混合而成,则溶液中四种离子的浓度由大到小的顺序为 。
直接排放含SO2,的烟气会形成胶雨,危害环境。利用钠碱循环法可脱除烟气中的SO2
(1)在钠碱循环法中,Na2 SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,
该反应的离子方程式是
(2)吸收液吸收SO2的过程中,pH随n(SO3²-):n(HSO3﹣变化关系如下表:
| n(SO3²--):n(HSO3﹣) |
91:9 |
1:1 |
9:91 |
| PH |
8.2 |
7.2 |
6.2 |
①上表判断NaHSO3溶液显 性,原因:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
a、C(Na+)==2C(SO32-)+C(HSO3-)
b、C(Na+)> C(HSO3-)> C(SO32-)>C(H+)==C(OH-)
c、C(Na+)+ C(H+)="=" C(SO32-)+ C(HSO3-)+ C(OH-)