向20mL 0.1mol/L NH4HSO4溶液中滴入0.1mol/L NaOH溶液,下列说法正确的是
| A.整个反应过程中:c(H+) + c(Na+) + c(NH4+)=c(OH-) + c(SO42-) |
| B.当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+) |
| C.当滴入20mL NaOH溶液时:2c(SO42-)=c(NH3·H2O)+ c(NH4+) |
| D.当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)= c(OH-) |
常温下,用0.10 mol·L—1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L—1 CH3COOH溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是
| A.点①和点②所示溶液中:c(CH3COO—)< c(CN—) |
| B.点③和点④所示溶液中:c(Na+)>c(OH—) >c(CH3COO—) >c(H+) |
| C.点①和点②所示溶液中: c(CH3COO—)-c(CN—) =" c(HCN)-" c(CH3COOH) |
| D.点②和点③所示溶液中都有:c(CH3COO—)+c(OH—)= c(CH3COOH) +c(H+) |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液: c(CO32-)> c(HCO3-)> c(OH-)>c(H+) |
| D.常温下,CH3COONa和CH3COOH混合溶液[pH=6, c(Na+)=0.1 mol·L-1]: |
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
下列说法正确的是
| A.由图甲可知,升高温度醋酸钠的水解程度增大 |
| B.由图乙可知,a点Kw的数值比b点Kw的数值大 |
C.由图丙可知,反应A(g)+B(g) 2C(g)是吸热反应 2C(g)是吸热反应 |
| D.由图丁可知,反应C(金刚石,s)= C(石墨,s)的焓变△H=△H1—△H2 |
25℃时,下列叙述正确的是
| A.NH4HSO4溶液中滴加NaOH溶液至pH=7,则c(Na+)=2c(SO42-) |
| B.0.1 mol·L-1CH3COOH溶液与0.1 mol·L-1CH3COONa等体积混合pH<7,则c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| C.AgCl在水中溶解度与在稀盐酸中溶解度相同 |
| D.KNO3溶液和CH3COONH4溶液pH均为7,则两溶液中水的电离程度相同 |
已知H2R为二元弱酸:H2R HR-+H+ Ka1 HR-
HR-+H+ Ka1 HR- R2-+H+ Ka2
R2-+H+ Ka2
常温下,向某浓度的H2R溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2R、HR-、R2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是
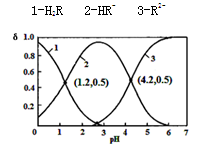
| A.pH=1.2溶液中:c(K+) + c(H+) = c(OH-) + c(H2R) |
| B.pH=2.7溶液中:c2(HR-) / [c(H2R) × c(R2-)]= 1000 |
| C.将相同物质的量KHR和K2R固体完全溶于水可配得pH为4.2的混合液 |
| D.向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离程度一直增大 |
某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是( )
| A.c( NH4+ )>c(Cl-)>c(OH-)>c(H+) |
| B.c( NH4+)>c(OH-)>c(Cl-)>c(H+) |
| C.c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.c( NH4+)>c(H+)>c(Cl-) >c(OH-) |
下列说法中正确的是
| A.体积相同、pH值相同的①盐酸 ②硫酸 ③醋酸,被NaOH溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ |
| B.25℃时,0.1 mol·L—1氨水和0.05mol·L—氨水中[OH—]之比是2:1 |
| C.25℃时,向CH3COONa溶液中加入适量CH3COOH使混合液pH=7,此时溶液中 [Na+]=[CH3COO-] |
| D.向含有HCO3-、CH3COO-、CO32-、SO32-离子的溶液中加入足量的Na2O2固体后,假设溶液体积不变,则以上四种离子浓度基本保持不变的是CO32-和CH3COO-。 |
下列溶液中有关物质的量浓度关系正确的是
A.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH) < c(CH3COONa) < c(Na2CO3)
B.已知0.1 mol·L-1二元酸H2A溶液的pH=4,则在0.1 mol·L-1 Na2A溶液中:
c(OH-) = c(HA-) + c(H+) + 2c(H2A)
C.将0.1 mol·L-1醋酸溶液加水稀释,则溶液中的c(H+)和c(OH-)都减小
下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/ c(HCO3-)的比值保持增大
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO
)+c(HCO )]
)]
③在0.1 mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH)=l0-a mol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)-c(H2S)-c(HS-)
| A.①④ | B.②⑤ | C.①③ | D.②④ |
在常温时,将V1 mL c1 mol·L-1 CH3COOH溶液中滴加到V2 mL c2mol·L-1NaOH溶液中,下列结论中,错误的是
| A.如果V1=V2,c 1= c 2,则混合溶液中c(CH3COO-) = c(Na+) |
| B.如果混合溶液的pH=7,则混合溶液中c(CH3COO-) = c(Na+) |
| C.如果混合溶液的pH>7,则不可能V1 c 1 = V2 c 2 |
| D.如果V1=V2,且混合溶液的pH<7,则c 1> c 2 |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.常温下,将pH="2的盐酸和pH=12的氨水等体积混合:" c(NH4+)>c(Cl-)> c(OH-)>c(H+) |
| B.0.1mol·L-1 Na2CO3溶液:c(Na+)=c(HCO3-)+2c(CO32-)+2c(H2CO3) |
| C.0.1mol·L-1 NH4Cl溶液:c(NH4+)="c(" Cl-) |
| D.向醋酸钠溶液加适量醋酸,得到的混合溶液:c(Na+)+ c(H+)=c(CH3COO-)+c(OH-) |
下列关系的表述中,正确的是
A.0.1mol·L-1NaHSO4溶液中:c(Na+)+c(H+)=c( )+c(OH-) )+c(OH-) |
| B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1 |
| C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等 |
D.0.1mol·L-1NaHCO3溶液中:c(Na+)>c( )>c( )>c( )>c(H2CO3) )>c(H2CO3) |
用0.10mol·L-1的盐酸滴定0.10mol·L-1的氨水,滴定过程中不可能出现的结果是
A.c( )>c(Cl-),c(OH-)>c(H+) )>c(Cl-),c(OH-)>c(H+) |
B.c( )=c(Cl-),c(OH-)=c(H )=c(Cl-),c(OH-)=c(H |
C.c(Cl-)>c( ),c(OH-)>c(H+) ),c(OH-)>c(H+) |
D.c(Cl-)>c( ),c(H+)>c(OH-) ),c(H+)>c(OH-) |
下列溶液中有关微粒的物质的量浓度关系正确的是
| A.同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl ③NH3·H2O ④CH3COONH4,其中c(NH4+)由大到小的顺序是:①>②>③>④ |
| B.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1 mol·L-1盐酸、 ③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
| C.常温下将NaHSO3和NaHCO3两溶液混合后,溶液呈中性,则混合后的溶液中: c (Na+)=c(HSO3—)+c(HCO3—)+2c(CO32—)+2c(SO32—) |
| D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ |