下列实验操作中错误的是( )
| A.蒸馏操作时,先得到的少量液体可能会与器壁等接触而含杂质较多,可以弃掉 |
| B.分液操作时,首先要打开分液漏斗的上口活塞,或使活塞上的小孔与上口部的小孔对准,然后进行分液 |
| C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D.萃取分液后,要得到被萃取的物质,通常还要进行蒸馏,为了更好的控制温度,用水浴加热比直接加热要好 |
电制法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42―杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下: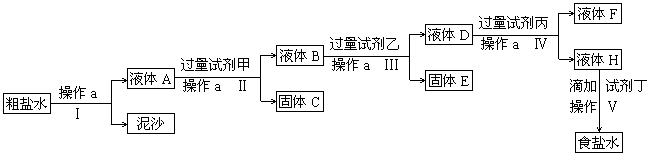
请回答以下问题:
(1)操作a的名称是____________,所用玻璃仪器是________________________________。
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。
(3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式________________。
下列行为中符合安全要求的是( )
| A.进入煤矿井时,用火把照明 |
| B.节日期间,在开阔的广场燃放烟火爆竹 |
| C.用点燃的火柴在液化气钢瓶口检验是否漏气 |
| D.实验时,将水倒入浓硫酸配制稀硫酸 |
某学生设计了三个实验方案,用以检验淀粉的水解情况。
(1)方案甲:
淀粉液 水解液
水解液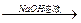 中和液
中和液 溶液变蓝。结论:淀粉没有水解。
溶液变蓝。结论:淀粉没有水解。
(2)方案乙:
淀粉液 水解液
水解液 无红色沉淀。结论:淀粉完全没有水解。
无红色沉淀。结论:淀粉完全没有水解。
(3)方案丙:
淀粉液 水解液
水解液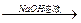 中和液
中和液 有红色沉淀。结论:淀粉已水解。
有红色沉淀。结论:淀粉已水解。
(4)方案丁: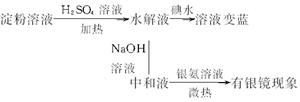
结论:淀粉部分水解。
以上四种方案的设计及结论是否正确?如不正确,请简述理由。
今有Ba(NO3)2、AgNO3、Fe(NO3)3的混合液,欲将Ba2+、Ag+、Fe3+
分离,分别得到三种元素的不溶物,按下图所示实验:
(1)加入的试剂(写化学式):X______,Y______,Z______。生成的沉淀(写化学式):A______,B______,C______。
(2)写出反应①②③的离子方程式:①____________,②____________,③____________。
右图是一套检验气体性质的实验装置。向装置中缓慢地通入气体X,若关闭活塞K,则品红试液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红试液褪色。据此判断气体X和洗气瓶内液体Y可能是( )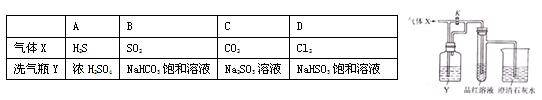
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A K+一定存在 B 100mL溶液中含0.01mol CO32-
C Cl-可能存在 D Ba2+一定不存在,Mg2+可能存在
以下离子检验的结论可靠的是( )
| A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+ |
| B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,说明有I- |
| C.往溶液中加入盐酸,产生的气体能使澄清石灰水变浑浊,说明有CO32— |
| D.往溶液中加入 BaC12溶液和稀 HNO3 ,有白色沉淀生成,说明有SO42- |
离子检验的常用方法有三种:
| 检验方法 |
沉淀法 |
显色法 |
气体法 |
| 含义 |
反应中有沉淀产生或溶解 |
反应中有颜色变化 |
反应中有气体产生 |
下列离子检验的方法不合理的是( )
A NH4+-气体法 B I--沉淀法 C Fe3+-显色法 D Ca2+-气体法
下列各组稀溶液,不用其他试剂或试纸,仅利用溶液间的相互反应,就可以将它们区别开的是( )
| A.硝酸钾、硫酸钠、氯化钙、氯化钡 | B.硫酸、硫酸铝、氯化钠、氢氧化钠 |
| C.盐酸、硫酸钠、碳酸钠、氢氧化钠 | D.硫酸氢钠、硫酸镁、碳酸钠、氢氧化钠 |
如下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )

| A.a为负极、b为正极 |
| B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 |
| D.电解过程中,氯离子浓度不变 |
(9分)氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O、H+、SO)能使氧化铜溶解。请你和他一起通过如图所示的Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
(1)某同学提出的假设是____________________________________________________。
(2)通过实验Ⅰ可以证明___________________________________________________。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步确认的实验操作是:在Ⅲ中先加入________,再加入________。
(4)探究结果为______________________。你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是________。
工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是;溶液的出口为(填字母);精制饱和食盐水的进口为(填字母);干燥塔中应使用的液体是。

(2)多晶硅主要采用还原工艺生产,其副产物
的综合利用收到广泛关注。
①可制气相白炭黑(与光导纤维主要原料相同),方法为高温下
与
和
反应,产物有两种,化学方程式为。
②可转化为
而循环使用。一定条件下,在20L恒容密闭容器中的反应:
达平衡后,
与
物质的量浓度分别为0.140mol/L和0.020mol/L,若
全部来源于离子交换膜法的电解产物,理论上需消耗纯
的质量为kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气 (标准状况)。
(标准状况)。