如图所示,往装满CO2的软矿泉水瓶加水,迅速拧紧瓶盖,震荡后CO2溶于水中,生成碳酸,矿泉水瓶变瘪,瓶变瘪表明瓶内气体压强 瓶外气体压强(选填“大于”、“等于”、“小于”),而瓶外的气体压强 ,因此推测瓶内气体压强与反应前相比 (后两空选填“变大”、“不变”、“变小”). 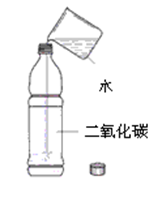
相关知识点
推荐套卷
如图所示,往装满CO2的软矿泉水瓶加水,迅速拧紧瓶盖,震荡后CO2溶于水中,生成碳酸,矿泉水瓶变瘪,瓶变瘪表明瓶内气体压强 瓶外气体压强(选填“大于”、“等于”、“小于”),而瓶外的气体压强 ,因此推测瓶内气体压强与反应前相比 (后两空选填“变大”、“不变”、“变小”). 