运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3: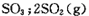
 混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题: 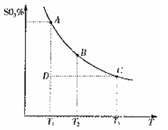
① 的△H 0(填“>”
的△H 0(填“>”
或“<”);若在恒温、恒压条件下向上述平衡体系中通入氦气,
平衡 移动(填“向左”、“向右”或“不”);
②若温度为T1、T2,反应的平衡常数分别为K1、K2,
则K1 K2;反应进行到状 态D时,V正 v逆(填“>”、“<”或“=)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业
生产、生活中有着重要作用。
① 图是一定的温度和压强下是N2和H2反应生成1molNH3过
程中能量变化示意图,请写出工业合成氨的热化学反应方程式:
。(△H的数值用含字母Q1、Q2的代数式表示)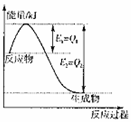
②氨气溶于水得到氨水。在25°C下,将a mol·L-1的氨水与
b mol·L-1的盐酸等体积混合,反应后溶液中显中性,则
c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含a和b的代数式表示该混合溶液中一水合出氨的电离平衡常数表达式 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。已知:25 ℃时,KSP(AgCl)=1.6×10-10mol2·L-2、KSP(AgI)=1.5×10-16mol·L-2,在25℃下,向100mL 0.002mol·L-1的NaCl溶液中逐滴加入100mL 0.002mol·L-1硝酸银溶液,有白色沉淀生成。从沉淀溶解平衡的角度解释产生沉淀的原因是 ,向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
℃时,KSP(AgCl)=1.6×10-10mol2·L-2、KSP(AgI)=1.5×10-16mol·L-2,在25℃下,向100mL 0.002mol·L-1的NaCl溶液中逐滴加入100mL 0.002mol·L-1硝酸银溶液,有白色沉淀生成。从沉淀溶解平衡的角度解释产生沉淀的原因是 ,向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号