为了探究力是不是维持物体运动的原因,小刚做了下面的3次实验,如图是小车从相同的斜面上滑下,分别在木板、毛巾、棉布表面前进一段距离后停下来的情况。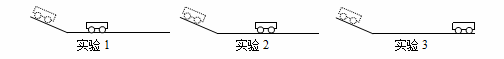
①由图可知实验1是小车在 表面,实验3是小车在 表面。
②小刚用什么方法使小车在进入不同的平面时具有相同的速度:
③实验表明:表面越光滑,小车受到的 越小,小车运动的距离将会越 。
④推论:如果小车受到的摩擦阻力为零,小车将
相关知识点
推荐套卷
 粤公网安备 44130202000953号
粤公网安备 44130202000953号