在“验证碰撞中动量守恒”的实验中,所验证的是从斜槽某一位置滚下的小球A在斜槽的水平出口处与静止小球B发生对心碰撞时动量守恒.两球半径大小均为r,且已知.实验时,小球A的质量m1和小球B的质量m2的大小关系是m1_________m2.实验时,除实验装置外还需要的测量工具应有__________.实验时若球的落点分别为图中所示的M、P、N点,则A、B两小球碰撞中动量守恒的表达式是____________.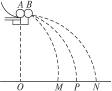
在“验证碰撞中动量守恒”的实验中,所验证的是从斜槽某一位置滚下的小球A在斜槽的水平出口处与静止小球B发生对心碰撞时动量守恒.两球半径大小均为r,且已知.实验时,小球A的质量m1和小球B的质量m2的大小关系是m1_________m2.实验时,除实验装置外还需要的测量工具应有__________.实验时若球的落点分别为图中所示的M、P、N点,则A、B两小球碰撞中动量守恒的表达式是____________.