江苏省南京市高三期初学情调研化学试卷
石墨烯是一种由碳原子组成六角形成蜂巢晶格的平面薄膜,其结构模型见右图。下列关于石墨烯的说法正确的是 ( )
| A.是一种新型化合物 | B.与石墨互为同位素 |
| C.晶体中碳原子键全部是碳碳单键 | D.是一种有发展前途的导电材料 |
下列有关化学用语表示正确的是 ( )
A.对硝基甲苯的结构简式: |
B.CH2F2的电子式: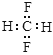 |
C.中子数为16的硫原子: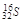 |
| D.乙炔的最简式:CH |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.1.0 mol·L-1KNO3溶液:H+、Fe2+、SCN-、SO42- |
B. 的溶液:K+、Ba2+、NO3-、Cl- 的溶液:K+、Ba2+、NO3-、Cl- |
| C.pH=0的溶液:Al3+、Cl-、SO42-、CO32- |
| D.c(ClO-) =" 1.0" mol·L-1的溶液:Na+、I-、S2-、SO42- |
下列关于物质性质与应用的说法正确的是 ( )
| A.碳具有还原性,高温条件下能将二氧化硅还原为硅 |
| B.二氧化硫有漂白、杀菌性能,可在食品加工中大量使用 |
| C.二氧化硅是半导体材料,可将太阳能直接转化为电能 |
| D.二氧化锰具有较强的的氧化性,可作H2O2分解的氧化剂 |
从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作。下列图示 对 应的装置合理、操作规范的是
| A.灼烧 | B.过滤 | C.分液 | D.蒸馏 |
设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
| A.标准状况下,2.24 L 水中所含的电子数为NA |
| B.常温常压下,16 g O3所含的电子数为8NA |
| C.0.1 mol Na2O2晶体中所含的离子数为0.4NA |
| D.1 mol Fe在氧气中充分燃烧失去的电子数为3NA |
下列指定反应的离子方程式正确的是
| A.氯化铝溶液中加入过量的氨水:Al3++4 NH3·H2O=AlO2-+4 NH4+ |
| B.稀硝酸中加入过量铁粉:Fe+4H++NO3-= Fe3++NO↑+2H2O |
| C.二氧化锰与浓盐酸混合加热:MnO2+4H++2Cl-△Mn2++ Cl2↑+2H2O |
| D.石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
下列各组物质之间通过一步就能实现如图所示转化的是
| 物质编号 |
物质转化关系 |
a |
b |
c |
d |
| ① |
 |
Na2O |
Na2O2 |
Na |
NaOH |
| ② |
Al2O3 |
NaAlO2 |
Al |
Al(OH)3 |
|
| ③ |
FeCl2 |
FeCl3 |
Fe |
CuCl2 |
|
| ④ |
NO |
NO2 |
N2 |
HNO3 |
A.①② B.②③. C.②④ D.①③
下列图示与对应的叙述相符的是 ( )

| A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 |
| B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
| C.图丙表示催化剂能改变化学反应的焓变 |
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 |
短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的颜色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z元素的核电荷数是W的2倍,Y是地壳中含量最多的金属元素。下列说法不正确的是 ( )
| A.工业上常用电解的方法制备X、Y的单质 |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.原子半径的大小顺序:r(X)> r(Y)> r(W)> r(Q) |
| D.元素X、Y的最高价氧化物对应的水化物之间能发生反应 |
下列说法中正确的是 ( )
| A.常温下,某难溶物的Ksp为2.5×105 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.NH3·H2O溶液加水稀释后,溶液中 的值增大 的值增大 |
| D.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 |
葛根素具有降血压等作用,其结构简式如下图,下列有关说法正确的是
| A.该物质在一定条件下能发生消去反应、加成反应、取代反应 |
| B.葛根素的分子式为C21H22O9 |
| C.该物质一个分子中含有5个手性碳原子 |
| D.一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
用铂丝蘸取少量某无色溶液进行焰色反应 |
火焰呈黄色 |
该溶液一定是钠盐溶液 |
| B |
向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液 |
出现黄色沉淀 |
Ksp(AgCl)>Ksp(AgI) |
| C |
向溶液X中滴加稀盐酸 |
有气体产生 |
溶液X 中一定含有CO32- |
| D |
向含H2SO4的淀粉水解液中加入新制的Cu(OH)2,煮沸 |
没有砖红色沉淀 |
淀粉未水解 |
有人曾建议用AG表示溶液的酸度,AG的定义为:AG=lg ,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
,室温下实验室用0.01 mol·L-1的氢氧化钠溶液滴定20 mL相同浓度的醋酸溶液,滴定曲线如右图所示。下列有关叙述正确的是( )
| A.A点时加入氢氧化钠溶液体积为20 mL |
| B.室温时0.01 mol·L-1的醋酸溶液pH=4 |
| C.OA段溶液中:c(CH3COO-)> c(CH3COOH) |
| D.若B点时加入NaOH溶液40 mL,所得溶液中:c(CH3COO-)+2 c(CH3COOH) = c(OH-) - c(H+) |
2SO2(g)+O2(g) 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙、丁四个容器体积均为2 L的恒容密闭容器中投料,其起始物质的量及含硫反应物的平衡转化率如下表所示:
| |
|
甲 |
乙 |
丙 |
丁 |
| 起始物质的量 |
n(SO2)/mol |
0.40 |
0 |
0.80 |
0.02 |
| n(O2)/mol |
0.24 |
0 |
0.48 |
0.04 |
|
| n(SO3)/mol |
0 |
0.40 |
0 |
0.40 |
|
| 含硫反应物的平衡转化率% |
80 |
 1 1 |
 2 2 |
 3 3 |
下列判断中,正确的是
A.乙中SO3的平衡转化率为 1=20%
1=20%
B.平衡时,丙中c(SO3)是甲中的2倍
C.平衡时, 3<
3< 1
1
D.该温度下,平衡常数的值为400
一水草酸钙(CaC2O4·H2O)可用作分离稀有金属的载体。其制备方法如下:
步骤I:用精制氯化钙稀溶液与草酸溶液共热反应,过滤,将固体溶于热盐酸中。
步骤Ⅱ:加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在105℃干燥得产品。
(1)写出步骤Ⅱ发生反应的化学方程式 。
(2)已知CaC2O4·H2O的Ksp = 2.34×10-9,为使步骤Ⅱ溶液中c(C2O42-)≤1×10-5 mol·L-1,c(Ca2+)的范围为 。
(3)为研究一水草酸钙的热分解性质,进行如下实验:准确称取36.50g样品加热,样品的固体残留率( )随温度的变化如下图所示。
)随温度的变化如下图所示。
①300℃时残留固体的成分为 ,900℃时残留固体的成分为 。
②通过计算求出500℃时固体的成分及质量。(写出计算过程)
聚合氯化铝是一种新型净水剂,其中铝的总浓度(用AlT表示)包括三类‘“主要为Al3+的单体形态铝总浓度(用Ala表示);主要为[AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝总浓度(用A1c表示)。
(1)一定条件下,向1.0 mol/LAlCl3溶液中加入0.6 mol/L的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液。写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:_____________________。
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如下表:
| AlT/(mol·L-1) |
Ala/% |
Alb/% |
A1c/% |
| 0.208 |
1.4 |
86.6 |
12.0 |
| 0.489 |
2.3 |
86.2 |
11.5 |
| 0.884 |
2.3 |
88.1 |
9.6 |
| 1.613 |
3.1 |
87.0 |
9.9 |
| 2.520 |
4.5 |
88.2 |
7.3 |
①在一定温度下,AlT越大,pH (填“越大”、“越小”或“不变”)。
②如将AlT =" 2.520" mol·L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式: 。
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1。当T>80℃时,AlT显著下降的原因是 。
(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s) = 3AlCl(g)+3CO(g) △H1 =" a" kJ·mol-1
②3AlCl(g) =" 2Al(l)+" AlCl3(g) △H2 =" b" kJ·mol-1
则反应Al2O3(s)+ 3C(s) =" 2Al(l)+" +3CO(g) △H = kJ·mol-1(用含a、b的代数式表示)。反应①常压下在1900℃的高温下才能进行,说明△H 0(填“>”“=”或“<”)。
(4)一种铝空气电池结构如图2所示,写出该电池正极的电极反应式 。
硫铁矿烧渣的主要成分为Fe2O3、Fe3O4,以及少量SiO2、Al2O3等。由硫铁矿烧渣制备铁红(Fe2O3)的一种工艺流程如下:
已知:还原焙烧时,大部分Fe2O3、Fe3O4转化为FeO。
几种离子开始沉淀和完全沉淀时的pH如下表所示:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
7.6 |
9.7 |
| Fe3+ |
2.7 |
3.7 |
| Al3+ |
3.8 |
4.7 |
(1)“酸浸、过滤”步骤中所得滤液中的金属阳离子有(填离子符号) 。
(2)Fe粉除调pH外,另一个作用是 ;Fe粉调节溶液的pH为 。
(3)“沉淀、过滤”步骤中生成FeCO3的离子方程式为 ;
所得滤液的主要溶质是(填化学式) 。
(4)高温条件下,“氧化”步骤中发生反应的化学方程式为 。
溴化钙在医药上用作中枢神经抑制药,实验室用“尿素法”制备溴化钙的主要流程如下:
溴化钙的部分溶解度数值如下:
| 温度 |
0℃ |
10℃ |
20℃ |
40℃ |
60℃ |
80℃ |
100℃ |
| 溶解度(g) |
125 |
132 |
143 |
213 |
278 |
295 |
312 |
(1)6Ca(OH)2+6Br2 50~70℃ 5CaBr2+6H2O+Ca(BrO3)2,每生成1 mol Ca(BrO3)2转移电子的物质的量为 ;50~70℃时,尿素[CO(NH2)2]将生成的Ca(BrO3)2还原为CaBr2,尿素被氧化为N2,该反应的化学方程式为 。
(2)过滤所需的玻璃仪器有玻璃棒、 , 。
(3)加入氢溴酸调pH的作用是 。
(4)操作I包括 、 、过滤、 、干燥。
(5)“二氧化硫法”制备的氢溴酸粗品中常含有少量的溴和硫酸;请选用所提供的试剂,补充完整检验氢溴酸粗品中是否含有Br2相SO42-的实验方案。
限选下列试剂:氯水、淀粉KI溶液、CCl4、BaCl2溶液、稀盐酸、植物油。
苯亚甲基苯乙酮俗称查尔酮,淡黄色梭状晶体,熔点58℃,沸点208℃(3.3kp),易溶于醚、氯仿和苯,微溶于醇。制备原理如下:

(1)制备过程中。需在搅拌下滴加苯甲酸,并控制滴加速度使反应温度维持在25~30℃,说明该反应是 (填“放热”或“吸热”)反应。如温度过高时,则可采用 措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是 。
(3)结晶完全后,需抽滤收集产物。’抽滤装置所包含的仪器除减压系统外还有 、 (填仪器名称)。
(4)获得的深色粗产品加入活性炭,用95%乙醇重结晶即得查尔酮晶体,可通过 法判断原料是否反应完全以及反应的转化率和选择性。
美托洛尔是一种治疗高血压的药物的中间体,可以通过以下方法合成:

请回答下列问题:
(1)美托洛尔中的含氧官能团为 和 (填名称)。
(2)反应③中加入的试剂X的分子式为C2H5OCl,X的结构简式为 。
(3)在上述①②③三步反应中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应 Ⅱ.能与FeCl3溶液发生显色反应
Ⅲ.分子中有4种不同化学环境的氢,且1 mol该物质与金属钠反应产生 1 mol H2。
写出一种该同分异构体的结构简式: 。
(5)根据已有知识并结合题目所给相关信息,写出以CH3OH和 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
 粤公网安备 44130202000953号
粤公网安备 44130202000953号