四川省成都市2012级临诊考试化学试卷
下列化学用语表达正确的是
A.乙酸分子比例模型: |
B.原于核内有18个中子的原子: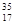 Cl Cl |
C.铬原于价电子层排布图: |
D.过氧化氢电子式: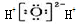 |
从分类角度,下列说法正确的是
| A.水玻璃与硅胶均属于酸 |
| B.漂白液与漂粉精的主要成分均为钠盐 |
| C.NO2、SO3均属于酸性氧化物 |
| D.醋酸、一水合氨均属于弱电解质 |
下列比较正确的是
| A.电负性:As>S>P | B.第一电离能F>N>O |
| C.熔点.BN> CCl4> MgBr2 | D.溶解性:乙醛>苯酚>乙醇 |
金属M和N可构成如图所示的装置.下列分析正确的是 
| A.金属活泼性N>M |
| B.M逐渐溶解 |
| C.负极反应为2H++2e- =H2↑ |
| D.SO42-向M极定向移动 |
某学习小组设计如下实验方案,相关推测不合理的是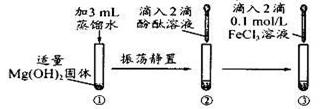
| A.试管②滴入酚酞后溶液可能变浅红 |
| B.试管③滴入FeCl3溶液后有红褐色沉淀生成 |
| C.试管④中的变化是物理变化 |
| D.上述反应说明Fe(OH)3溶解性小于Mg(OH)2 |
若NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2 .24 L NH3溶干1 L水中得到OH-数约为0.1NA |
| B.l 4 g N2与CO的混合气体含有的原于数目为NA |
| C.25℃时pH=13的NaOH溶液中含有OH-的数目为0 .l NA |
| D.含l mol H2 SO4的浓硫酸与足量铜反应转移的电子为NA |
下列说法正确的是
| A.丁烷的沸点高于丙醇 |
B.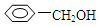 与苯酚是同系物 与苯酚是同系物 |
| C.淀粉、纤维素互为同分异构体 |
| D.葡萄糖、果糖均能发生银镜反应 |
下图是某盐酸试剂标签部分内容,据此判断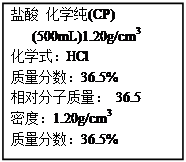
| A.该盐酸与钠可存放在同一药品橱柜中 |
| B.该盐酸含HCI质量为600 g |
| C.配制1OO mLO.2 mol/L盐酸需用到玻璃仪器为量筒、烧杯、玻璃棒 |
| D.该盐酸的物质的量浓度为12. 0 mol/L |
已知反应KClO3+6HCl = KCl+3Cl2↑+3 H2O,下列判断正确的是
| A.KClO3被氧化 |
| B.氧化剂与还原剂之比为1:6 |
| C.氧化产物是Cl2 |
| D.HCl在化学反应中只能作还原剂 |
用下列实验装置进行相应实验,能达到实验目的的是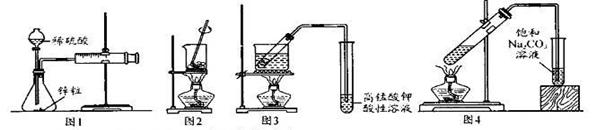
| A.图1--测量锌与硫酸反应的速率 |
| B.图2——灼烧海带成海带灰 |
| C.图3——验证溴乙烷与NaOH乙醇溶液反应生成乙烯 |
| D.图4——实骑室制备收集己酸乙酯 |
某软质隐形眼镜材料为如下图所币的聚合物。下列有关说法错误的是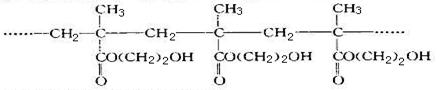
| A.生成该聚合物的反应属加聚反应 |
| B.该聚合物的单体是丙酸乙酯 |
| C.i聚合物分子中存在大量的—OH,所以具有较好的亲水性 |
D.该聚合物的结构筒式为 |
化学与生活宙哪相关,下列用选、性质或变化对应正确的是
| A.利用粮食酿酒的化学过程包含:淀粉一→葡萄糖一→己醇 |
| B.在月饼包装袋中放人生石灰:防止食物氧化变质 |
| C.焰火的绚丽:说明只有金属单质能发生焰色反应 |
| D.氢氧化铝用于清疗胃酸过多:氢氧化锯碱性强 |
常温下,下列各组离子一定能大量共存的是
| A.c(Fe3+) =0.1mol·L-1的溶液中:K+、NH4+、SCN-、SO42- |
| B.水电离出的(OH-)=1。0×10-3 mol·L-1的溶液:Na+ 、K+、MnO4-、C2O42- |
| C.能与铝反应生成氢气的溶液中:K+、Cl- 、Na+、SiO32- |
| D.0 1 mol·L-1NaOH溶液K+、Na+、SiO32-、CO32- |
某有机物的结构为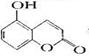 , ,下列有关说法正确的是
, ,下列有关说法正确的是
| A.1 mol该物质与足量淮溴水反应,最多消耗2 molBr2 |
| B.1mol该物质最多能与2mol NaOH反应 |
| C.l mol该物质晟多能与3 mol H2加成 |
| D.该物质的核磁共振氢谱共有6个吸收峰 |
能正确表示下列反应的离子方程式是
| A.钠与水反应:Na+2H2O=Na++OH-+H2↑ |
| B.Kl溶液中滴入稀硫酸,空气中振荡:4H+ +41-+O2=2I2+2H2O |
| C.CuCl2溶液中加入氨水:Cu2+ +20H- = Cu(OH)2:↓ |
D.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
下列实验操作与现象均正确的是
| 选项 |
操作 |
现象 |
| A |
将铝片置于试管中,加入5mL浓硫酸 |
铝片无明显溶解 |
| B |
两试管各加入5mL 0.1 mol·L-1Na2S2O3溶液,同时分别滴入55mL 0.1 mol·L-1硫酸和盐酸 |
两只试管同时变浑浊 |
| C |
试管中加入2mL饱和Na2CO3溶液,滴入两滴酚酞,加热 |
溶液先变红,后红色变浅 |
| D |
向盛有1mL硫酸铜溶液的试管中逐滴加入氨水得到深蓝色溶液,然后加入乙醇 |
最终只能形成深蓝色透明溶液 |
t℃时,在体积不变的容器中发生反应X(g)+3Y(g) 2Z(g)△H<O各组分浓度如下表
2Z(g)△H<O各组分浓度如下表
| 物质 |
X |
Y |
Z |
| 初始浓度/ mol·L-1 |
0.1 |
0.3 |
0 |
| 2min末浓度/mol·L-1 |
0.08 |
|
|
| 平衡浓度/mol·L-1 |
|
|
0.1 |
下列说法不正确的是
A .0~2min的平均速率v(x) ="0." 01 mol·L-1·min-1
B.达平衡时Y的转化率为50%
C.其它条件不变,升高温度,平衡逆向移动
D.其它条件不变,增加X的浓度,ν正增大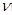 逆碱小,平衡正向移动
逆碱小,平衡正向移动
25C时,用浓度为0.1000 mol/L的NaOH溶液滴定20. 00 mL 0 .1000 mol·L-1的
CH3COOH.。滴定曲线如图所示。下列分析错误的是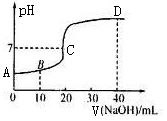
| A.C点的溶液:c(CH3COO一)+c(CH.3COOH)>c(Na+) |
| B.B点的溶液c (CH3COO一)>c(Na+)>c(H+)> c(OH-) |
| C.A点的纵坐标值为l |
| D.D点溶液2c(CH3COOH)十c(H+) =c(OH—)—c(CH3COO—) |
将等物质的量的铁和铜的混台物24 g与600mL稀硝酸恰好完全反应,生成NO6 .72 L(标准状况)向反应后的溶液中加入l mol·L-1 NaOH溶液使金属离于恰好沉淀,过滤。下列有关说法错误的是
| A.混合物溶解后的溶液中 c(Fe3+): c(Fe2+) =1:1 |
| B.需加入NaOH溶液1000mL |
| C.稀硝酸的物质的量浓度是2 mol·L-1 |
| D.最后所得沉淀在空气中充分加热可得固体32 g |
W、X、Y、Z为原于序数依次增大的前四周期元素,其中W、X、Y为主族元素。用X的氧化物漂白的草帽日久又变成黄色;基态W原子有两个单电子,且与X不同周期不同族,X、Y同周期,基态Z原于电子分属7个能级,且各能级均为全充满。
(1)X基态原子的价电子排布式是 。
(2)WX2中W原子的杂化轨道地 类型是 ;WX2分子的立体构性为 。
(3)WX2属于 (填“极性”或“非极性”“)分子;若X2Y2的结构简式为Y—X—X—Y,1molX2Y2含有的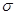 键数目为 NA。
键数目为 NA。
(4)X与Z所形成的化合物晶体的晶胞如下图所示,X的配位数是 ;该 晶体的化学式为 。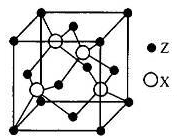
(12分)某工业废水肿含有一定量的Cr2O72-和CrO42-,现
取样该工业废水,检测其中铬的含量。
步骤I:取25. 00 mL废水,加入适后稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液,滴人几滴指示剂。
步骤Ⅲ: 用o .1000 mol·L-1Na2S2O3溶液滴定(I2+2Na2 S2O3= 2NaI+Na2S4O6)
达到终点时消耗溶液24. 00 mL。
步骤Ⅳ:将上述反应后的溶液进行如下处理:反应后废液
回答下列问题
(1)步骤I加入稀硫酸酸化的目的是 ;
(2)步骤Ⅱ中发生如下反应,请完善并配平离子方程式
该步骤中所加指示剂是 ;
(3)步骤Ⅲ判断滴定达到终点的现象是__ __。
(4)步骤Ⅳ在生产生活中的意义是____ (任答一条);
(5)计算工业废水中铬元素的含量是 mg/L.
以苯酚为原料合成某药物中间体M的合成路线如下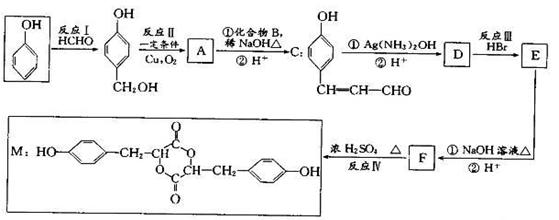
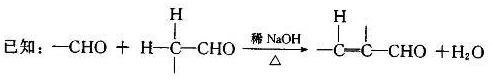
(1)C中含氧官能团的名称为___ _。
(2)反应I的反应类型是 。
(3)反应Ⅱ的化学方程式为 。
(4)化台物B的名称是 ;E的结构简式为__ __。
(5)写出同时满足下列条件的F的同分异构体的结构简式 (任写两种)。
①苯环上有三个取代基且苯环上的一氯取代物只有两种
②能与FeCl3溶液反应显紫色
③红外光谱显示有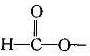
甲醇(CH3OH)被称为21世纪的新型燃料,以煤为原料制备甲醇的流程如下: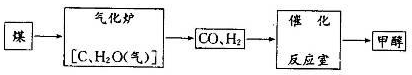
(1) 气化炉中主要反应的化学方程式为 。
(2)已知CO、H2、甲醇(l)的燃烧热分别为:—285.8 kJ/mol、—283 kJ/mol、—726.5 kJ/mol;
则CO和H2合成甲醇的热化学方程式为__ __
(3) -定条件下,在催化反应室中发生反应.CO(g)+2H2(g) =CH3OH(g)△H<0;
CO 的平衡转化率与温度、压强的关系如图所示。回答下列问题: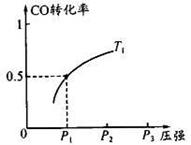
①工业上,上述反应温度不宜过高,原因是_ ___;
②若反应是1 mol CO与2 mol H2在2L容积中进行,则
T1、P1下,该反应的平衡常数为__ __;
维持温度、容积不变,催化反应室再增加l mol CO与2 mol
H2,达到新平衡时,CO的转化率____(填“增大”、“减小”或“不变”)。
硝矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O及少量氧化铁。
利用明矾石制备K2SO4的工艺流程如下所示: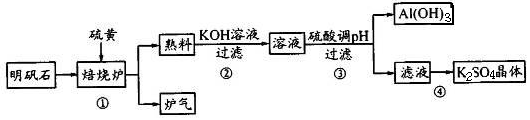
(1)焙烧炉中发生如下反应,请在方程式中表示出电子转移的方向和数目
2Al2(SO4)3+3S 2Al2O3+9SO2↑
2Al2O3+9SO2↑
(2)步骤②涉及Al2O3的离子方程式为____。
(3)步骤③调pH生成AI{OH)。的离子方程式为____;不能用CO2来调pH,理由是
.
(4)步骤④的主要操作步骤是___ _,过滤、洗涤和干燥
(5)炉气回收可做多种用途,请举一例:__ _。
某小组进行铝热反应实验,装置如图所示。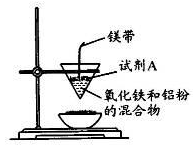
(1)铝热反应原理____(写化学方程式);试剂A为____(写化学式).实验现象____、有黑色固体生成。
(2)对黑色固体物质的组成,小组进行了如下探究
假设I该黑色物质为铁
假设Ⅱ该黑色物质为铁与四氧化三铁的混合物
【设计方案并实验】
| 实 验 步 骤 |
现 象 |
结 论 |
| ①取少量黑色固体于试管中加稀盐酸 |
固体全部溶解,有气泡产生 |
假设I成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mol/LKSCN溶液 |
溶液不变色 |
【交流评价】
你认为上述结论是否合理,__ __理由是__ __。
(3)取上述实验所得溶液,滴人适量氯水溶液变红色。此时涉及的离子反应方程式为
__ __、__ __;
利用反应体系中存在的平衡,小组再将溶液均分置于两支试管中并分别编号l、2.进行
如下探究:
| 实验编号 |
实验步骤 |
| 1 |
①滴加饱和FeCl3溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 |
|
| |
①滴加4滴1mol/LKSCN溶液 |
| ②滴加几滴NaOH溶液 |
该实验中,小组
主要探究的问题是__ __;
应重点观察的现象是__ __
预计得出的结论是__ __。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号