山东省泰安市高一年级考试化学试卷
化学与人类生活、社会可持续发展密切相关。下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用 ②研发易降解的生物农药
③应用高效洁净的能源转换技术 ④田间焚烧秸秆
⑤推广使用节能环保材料 ⑥废电池进行集中回收处理
| A.①③⑤⑥ | B.②③⑤⑥ | C.①②④ | D.②④⑤ |
下列化学用语表示正确的是
| A.原子核中有6个中子的硼原子:6B | B.HCl的电子式: |
C.K+结构示意图: |
D.HClO的结构式:H—O—Cl |
下列说法中正确的是
| A.只含有非金属元素的化合物可能是离子化合物 |
| B.第ⅠA族元素都比第ⅡA族元素金属性强 |
| C.只含有共价键的物质一定是共价化合物 |
| D.同主族元素原子半径越小越容易失去电子 |
下列说法正确的是
| A.14C和14N质量数相同,互为同位素 |
| B.12C和14N含有相同的中子数 |
| C.12C和 13N中子数相同,质子数不同,互为同位素 |
| D.12CO和14CO物理性质不同,化学性质基本相同 |
下列反应既是氧化还原反应,又是吸热反应的是
| A.锌粒与稀H2SO4反应 | B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.灼热的碳与CO2反应 | D.葡萄糖在人体内氧化 |
化学变化的实质是旧的化学键断裂、新的化学键形成。据此判断下列变化是化学变化的是
| A.固体氯化钠溶于水 | B.冰经加热变成水蒸气 |
| C.氯化铵受热分解生成氯化氢和氨气 | D.氯化氢溶于水 |
下列关于有机化合物的说法正确的是
| A.甲烷和乙烯都可以使溴水褪色 |
| B.乙醇和乙酸都能发生取代反应 |
| C.酸性高锰酸钾可以氧化苯和乙烯 |
| D.苯主要是以石油分馏获得的一种重要化工原料 |
下列说法不能证明氯的非金属性比硫强的是
| A.HCl比H2S稳定 |
| B.HClO4的酸性比H2SO4的酸性强 |
| C.向Na2S溶液中通入Cl2,溶液变浑浊 |
| D.向新制氯水中滴加Na2SO3溶液,氯水褪色 |
对于反应2SO2+O2 2SO3,下列判断正确的是
2SO3,下列判断正确的是
| A.2 mol SO2和足量的O2反应,一定生成2mol SO3 |
| B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2 |
| C.平衡时SO2的消耗速率等于O2的生成速率的2倍 |
| D.平衡时SO2的浓度为O2浓度的2倍 |
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的7/10。则下列说法中不正确的是
| A.原子半径由大到小排列顺序Z>Y>X |
| B.Y元素的两种同素异形体在常温下都是气体 |
| C.最高价氧化物对应水化物的酸性W>Z |
| D.阴离子半径由大到小排列顺序Z>W>Y |
对于300mL 1 mol·L-1盐酸与铁片的反应,采取下列措施:
①升高温度 ②改用100mL 3 mol·L-1盐酸
③再加300mL 1 mol·L-1盐酸 ④用等量铁粉代替铁片 ⑤改用100mL 98%的硫酸
其中能使反应速率加快的是
| A.①②④ | B.①③④ | C.①②③④ | D.①②③⑤ |
下列关于有机物的叙述不正确的是
| A.淀粉水解最终生成葡萄糖 |
| B.煤中含有苯、甲苯等芳香烃,可通过干馏制取 |
| C.医用酒精杀菌消毒原理是利用了蛋白质的变性 |
| D.除去乙酸乙酯中混有的乙酸,可加入饱和碳酸钠溶液后分液 |
某烃的结构简式为 ,它可能具有的性质是
,它可能具有的性质是
| A.易溶于水,也易溶于有机溶剂 |
| B.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 |
| C.在一定条件下它能通过加聚反应生成高分子化合物 |
| D.一定条件下1mol该物质最多可与3mol H2发生加成反应 |
下列叙述中正确的是
| A.离子化合物熔融状态下一定导电 |
| B.金属元素跟非金属元素化合时都能形成离子键 |
| C.离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 |
| D.离子化合物中不一定含有离子键,含共价键的化合物不一定是共价化合物 |
X、Y、Z是原子序数依次增大的短周期主族元素,X2-、Z+都与Mg2+具有相同的核外电子层结构。则下列说法中正确的是
| A.Y元素位于第二周期第ⅦA族或0族 |
| B.X、Y、Z三种元素中非金属性最强的是X元素 |
| C.X、Y、Z三种元素形成的简单离子的半径都比Mg2+半径小 |
| D.Z分别与X、Y形成的化合物都是离子化合物 |
参照反应Br+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是
| A.正反应为吸热反应 |
| B.该反应的逆反应是吸热过程 |
| C.HBr的能量一定高于H2的能量 |
| D.反应物具有的总能量大于生成物具有的总能量 |
有M、N、P、Q四块金属片,进行如下实验:
①M、N用导线相连后,同时插入稀H2SO4中,M极为负极
②P、Q用导线相连后,同时浸入稀H2SO4中,电子由P→导线→Q
③M、P相连后,同时浸入稀H2SO4,P极产生大量气泡
④N、Q相连后,同时浸入稀H2SO4中,Q极发生氧化反应
则四种金属的活动性顺序为
| A.M>N>P>Q | B.M>P>Q>N | C.N>Q>P>M | D.P>M>N>Q |
为探究锌与稀盐酸反应速率[以v(H2)表示],向反应混合液中加入某些物质,下列判断正确的是
| A.加入铜粉,v(H2)增大 |
| B.加入NaHSO4固体,v(H2)不变 |
| C.加入水,锌不与水反应,v(H2)不变 |
| D.加入NaCl固体,会增大Cl-浓度,使v(H2)增大 |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是
①Zn是负极
②电子由Zn经外电路流向Cu
③Zn极发生氧化反应生成Zn2+
④H+在溶液中由Cu极向Zn极迁移
| A.①②④ | B.②③④ |
| C.①②③ | D.①②③④ |
下图是一套实验室制气装置,用于制取、干燥和收集气体。下列各组物质中能利用这套装置进行实验的是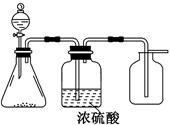
| A.碱石灰和浓氨水 |
| B.二氧化锰和浓盐酸 |
| C.铜和稀硝酸 |
| D.碳酸钙和稀盐酸 |
(7分)现有下列八种物质: HCl、NH4Cl、N2、Na2O2、CaCl2、Cl2、NaF、CO2
回答下列问题:
(1)只含有离子键的物质是 (填化学式,下同)。
(2)既含有离子键,又含有共价键的物质是 。
(3)属于共价化合物的是 ,其中所有原子都满足8电子结构的是 。
下表是元素周期表的一部分:
针对表中的①~⑩号元素,用元素符号或化学式填空:
(1)在这些元素中,最易失电子的元素是 ,非金属性最强的元素是 。
(2)化学性质最不活泼的元素是 ,其原子结构示意图为 。
(3)元素的最高价氧化物对应的水化物中呈两性的氢氧化物与氢氧化钠溶液反应的离子方程式是 。
(4)在②⑤⑦⑨四种元素中,原子半径由大到小的顺序是 。
(5)元素⑥、⑩的最高价氧化物对应的水化物中,酸性较强的是 。
短周期元素X、Y、Z、W核电荷数依次增大,X、Z同主族,Z、W同周期,四种元素的原子序数之和为37,在周期表中X是原子半径最小的元素,Y的最外层电子数是内层电子数的3倍。
(1)W在周期表中的位置是 。
(2)X与Y 能形成具有18个电子的化合物,此化合物的电子式为 。
(3)X、Y、Z三种元素组成的化合物中存在的化学键类型为 。
(4)Z、W两种元素的最高价氧化物对应水化物溶液之间反应的离子方程式为 。
来自石油的有机化工原料A,其产量已作为衡量一个国家石油化工发展水平的标志,A可以发生如下转化:
已知:E是具有果香味的有机物,其分子式为C4H8O2,F是一种高分子化合物。
(1)A的分子式是 ,C的名称是 。
(2)D分子中的官能团名称是 ,证明该官能团具有酸性的方法是 。
(3)反应③的化学方程式是 ;反应④的类型是 反应。
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验:
| 编号 |
操作 |
实验现象 |
| ① |
分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol·L-1 FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡 |
试管A中无明显气泡产生; 试管B中产生的气泡量增加 |
| ② |
另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 |
试管A、B中均未明显见到有气泡产生 |
请回答下列问题:
(1)过氧化氢分解的化学方程式为 。
(2)实验①的目的是___________________________________________________;实验中滴加FeCl3溶液的目的是________________________________________。
(3)实验②未观察到预期的实验现象。为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_________________________(用实验中所提供的试剂或条件)。
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,分析判断OE、EF、FG三段中,___________段化学反应速率最快。
目前,我国石油资源紧张,大多数城市使用“乙醇汽油”。
(1)乙醇燃烧时,如果氧气不足会有CO生成。用下图所示装置连接后验证乙醇燃烧产物中有CO、CO2和H2O。则按气流从左到右,连接装置的编号顺序为 。
(2)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是 ;B瓶溶液的作用是 。
(3)装置①中所盛的是 溶液,证明燃烧产物中含有CO的实验现象是 。
(4)装置④中所盛的固体药品是 ,它验证的产物是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号