全国普通高等学校招生统一考试理科综合能力测试化学
的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用捕获生成重要化工产品三聚氰胺的反应:→ +下列有关三聚氰胺的说法正确的是()
+下列有关三聚氰胺的说法正确的是()
| A. | 分子式为 | B. | 分子中既含极性键,又含非极性键 |
| C. | 属于共价化合物 | D. | 生成该物质的上述反应为中和反应 |
下列有关溶液的叙述正确的是()
| A. | 该溶液中 、 、 、 可以大量共存 |
| B. | 和 溶液反应的离子方程式: |
| C. | 和 溶液反应的离子方程式: |
| D. | 1 L0.1 该溶液和足量的 充分反应,生成11.2 |
为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
| 选项 |
实验目的 |
主要仪器 |
试剂 |
| A |
分离和混合物 |
分液漏斗、烧杯 |
和混合物、蒸馏水 |
| B |
鉴别葡萄糖和蔗糖 |
试管、烧杯、酒精灯 |
葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C |
实验室制取 | 试管、带导管的橡皮塞 |
锌粒、稀 |
| D |
测定溶液浓度 |
滴定管、锥形瓶、烧杯 |
溶液,0.1000盐酸 |
臭氧是理想的烟气脱硝剂,其脱硝反应为: ,反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
,反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是

中学化学中很多"规律"都有适用范围,下列根据有关"规律"推出的结论正确的是()
选项 规律 结论
| A. |
A 较强酸可以制取较弱酸 次氯酸溶液无法制取盐酸 |
| B. |
B 反应物浓度越大,反应速率越快 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C. |
C 结构和组成相似的物质,沸点随 NH3沸点低于PH3 相对分子质量增大而升高 |
| D. |
D 溶解度小的沉淀易向溶解度更小 ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 的沉淀转化 |
室温下,在0.2mol/L溶液中,逐滴加入1.0mol/L溶液,实验测得溶液pH随溶液体积变化曲线如下图,下列有关说法正确的是

是常见的六种元素。
(1)位于元素周期表第周期第族;的基态原子核外有个未成对电子;的基态原子核外电子排布式为。
(2)用">"或"<"填空:
| 第一电离能 |
离子半径 |
熔点 |
酸性 |
(3)与反应生成和一种黑色固体。在25 ℃、101下,已知该反应每消耗1,放热44.4,该反应的热化学方程式是。
(4)是常用于水的净化,工业上可用氧化溶液制取。写出该反应的离子方程式,并标出电子转移的方向和数目。
酯()是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):

(1)为加成反应,则的结构简式是;的反应类型是。
(2)中含有的官能团名称是;的名称(系统命名)是。
(3)的化学方程式是。
(4)是的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;②存在甲氧基()。的结构简式是。
(5)下列说法正确的是。
a.能和反应得到聚氯乙烯的单体
b.和中均含有2个键
c.1完全燃烧生成7
d.能发生加成、取代反应
是锂离子电池中广泛应用的电解质。某工厂用、为原料,低温反应制备,其流程如下:

已知:的沸点是-85.0 ℃,的沸点是19.5 ℃。
(1)第①步反应中无水的作用是、。反应设备不能用玻璃材质的原因是(用化学方程式表示)。无水有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中极易水解,其产物为两种酸,写出水解的化学方程式:。
(3)第④步分离采用的方法是;第⑤步分离尾气中HF、HCl采用的方法是。
(4)产品中通常混有少量。取样品。测得的物质的量为,则该样品中的物质的量为(用含有、的代数式表示)。
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
| 编号 |
实验目的 |
碳粉/ | 铁粉/ | 醋酸/% |
| ① |
为以下实验作参照 |
0.5 |
2.0 |
90.0 |
| ② |
醋酸浓度的影响 |
0.5 |
|
36.0 |
| ③ |
|
0.2 |
2.0 |
90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。时,容器中压强明显小于起始压强,其原因是铁发生了
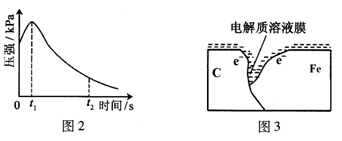
(3)该小组对图2中0~时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有的方案。请你再设计一个实验方案验证假设一,写出实验步骤和结论。
| 实验步骤和结论(不要求写具体操作过程): |
 粤公网安备 44130202000953号
粤公网安备 44130202000953号