江西省抚州五校高三5月联考理综化学试卷
下列说法不正确的是( )
| A.煤经过气化和液化等物理变化可以转化为清洁燃料 |
| B.侯氏制碱法的工艺过程,应用了物质溶解度的差异 |
| C.食品包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同 |
| D.甘氨酸和丙氨酸发生脱水反应,最多可生成4种二肽 |
已知在比较酸的强弱时,必须考虑两方面:一是电离出氢离子的能力,二是溶剂接受氢离子的能力。比如HCl在水中是强酸,在冰醋酸中就是弱酸;而HAc在水中是弱酸,在液氨中却是强酸,就是因为接受氢离子的能力:NH3>H2O>HAc。下列关于酸性强弱的说法正确的是( )
| A.在A溶剂中,甲的酸性大于乙;在B的溶剂中,甲的酸性可能小于乙 |
| B.比较HCl、H2SO4、HClO4、HNO3酸性的强弱,用水肯定不可以,用冰醋酸可能可以 |
| C.HNO3在HClO4中是酸,在H2SO4中可能是碱 |
| D.比较HCN与HAc酸性的强弱,用水肯定可以,用液氨肯定也可以 |
下列说法正确的是( )
| A.根据反应5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可检验绿矾(FeSO4·7H2O)是否变质 |
| B.根据反应H3PO3+2NaOH(足量)===Na2HPO3+2H2O可知:H3PO3属于三元酸 |
| C.根据反应3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O可知:反应中HNO3表现酸性和氧化性 |
| D.根据反应CuSO4+H2S===CuS↓+H2SO4可知:H2S的酸性比H2SO4强 |
已知X、M都是中学教材常见元素,下列对甲、乙两个离子反应通式的推断中,(甲)XO3n-+Xn-+H+→X单质+H2O(未配平);(乙)Mm++mOH-=M(OH)m↓,其中正确的是( )
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
③若m=2,则在空气中蒸干MSO4溶液并灼烧一定能得到MSO4
④若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
⑤若m=3,则MCl3与足量的碱溶液反应一定生成M(OH)m
⑥若n=2、m=3,则Xn-和Mm+发生的反应是水解反应
| A.①③ | B.②④ | C.①②③④ | D.其它组合 |
苯的同系物C12H18有多种同分异构体,其中二取代苯的同分异构体(不考虑立体异构)有( )
| A.48种 | B.45种 | C.42种 | D.以上都不是 |
乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素 的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示。下列说法不正确的是( )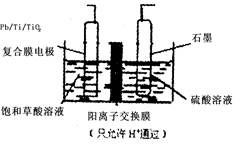
| A.电解时石墨电极应与直流电的正极相连 |
| B.阴极反应式为:HOOCCOOH+2H++2e-=OHCCOOH+H2O |
| C.电解时石墨电极上有O2放出 |
| D.电解一段时间后,硫酸溶液的pH不变化 |
T℃时,A气体与B气体反 应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。现向一体积可变的密闭容器中通入等物质的量的A气体和B气体,在恒温条件下发生反应达到平衡状态Ⅰ后,再升高到某温度,继续反应一段时间后达到平衡状态Ⅱ。下列叙述中正确的是( )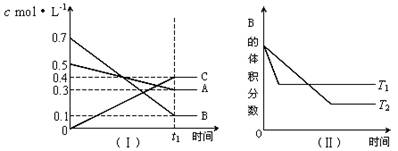
A.该反应在高温时才能自发进行
B.反应从开始到平衡状态Ⅰ的过程中,反应向正向进行,A的体积分数一直在减少
C.平衡状态Ⅰ到平衡状态Ⅱ的过程中,平衡向逆向移动,A的体积分数一直没有变化
D.反应从开始到平衡状态Ⅱ的过程中,平衡常数K和A的转化率都是先增大后减少
(Ⅰ)、A、B、C、D、E、五种元素均是短周期元素,且原子序数依次增大。B、E原子的最外层电子数均为其电子层数的2倍。D、E元素原子的最外层电子数相等。X、Y、Z、W、G、甲、乙七种物质均由上述中的两种或三种元素组成。元素B形成的单质M与甲、乙(相对分子质量:甲<乙)浓溶液的反应分别是:甲与M反应生成X、Y、Z,乙与M反应生成Y、Z、W,反应条件均省略。回答下列有关问题:
⑴X、Y、W均能与Z反应,若将标准状况下的X和D2按4:1充满试管后将其倒立于水槽中,待水不在上升时,试管内溶质的物质的量浓度是 (假设溶质不扩散)
⑵若将X、W、D2按4:4:3通入Z中充分反应,写出总的离子方程式
⑶G是一种既能与强酸又能与强碱反应的酸式盐,则G的电子式 ,取0.2mol/L的NaOH溶液与0.1mol/L的G溶液等体积混合后,加热至充分反应后,待恢复至室温剩余溶液中离子浓度的由大到小顺序是 ,此时测得溶液的PH=12,则此条件下G中阴离子的电离平衡常数Ka =
(Ⅱ)⑷某温度时,向AgNO3溶液中加入K2CrO4溶液会生成
Ag2CrO4沉淀,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。
该温度下,下列说法正确的是_________。
A. Ag2CrO4的溶度积常数(Ksp)为1×10-8
B. 含有大量CrO 的溶液中一定不存在Ag+
的溶液中一定不存在Ag+
C. a点表示Ag2CrO4的不饱和溶液,蒸发可以使溶液由a点变到b点
D. 0.02mol·L-1的AgNO3溶液与0.02mol·L-1的Na2CrO4溶液等体积混合会生成沉淀
⑸若常温下Ksp[Cr(OH)3]=10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至_______。
2013年10月我市因台风菲特遭受到重大损失,市疾控中心紧急采购消毒药品,以满足灾后需要。复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2是一种无色粘稠液体,请回答下列问题:
⑴火箭发射常以液态肼(N2H4)为燃料,液态H2O2为助燃剂。已知:
N2H4(1)+O2(g)=N2(g)+2H2O(g) △H="-" 534 kJ·mol-1 ①
H2O2(1)=H2O(1)+1/2O2(g) △H="-" 98.64 kJ·mol-1 ②
H2O(1)=H2O(g) △H=+44kJ·mol-l ③
则反应N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)的△H= ,
⑵据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作 原料的燃 料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电,其工作原理如图所示。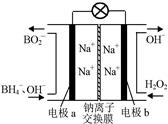
则该电池的正极反应____ ___
⑶H2O2是一种不稳定易分解的物质。右图是H2O2在没有催化剂时反应进程与能量变化图,请在图上画出使用催化剂加快分解速率时能量与进程图 。
⑷某化学兴趣小组欲测定H2O2的分解速率,取溶液0.5L进行分析,数据如表格所示:
| t(S) |
0 |
2 |
4 |
6 |
8 |
10 |
| n(H2O2) (moL) |
0.8 |
0.7 |
0.62 |
0.55 |
0.27 |
0.03 |
在上述表格中已知某一时刻向H2O2溶液中加入催化剂,则加入催化剂后整段时间内H2O2的平均分解速率___________。
⑸H2O2还是一种药物化学分析的氧化剂,能用于药物的分析。

①此检验过程中加过量H2O2反应的离子方程式为______________。
②从红褐色的悬浊液到最后的称量,其过程中所需的基本操作有___________(按操作的顺序填写)。
A.过滤 B.洗涤 C.萃取 D.分液 E.冷却 F.灼烧
③最后称量红棕色固体的质量为0.8960g,那么该药片中硫酸亚铁的质量分数为
_________(小数点后面保留一位有效数字)。
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
| 物质 |
甲醇 |
苯甲酸 |
苯甲酸甲酯 |
| 沸点/℃ |
64.7 |
249 |
199.6 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2 g苯甲酸和20 mL甲醇(密度约为0.79 g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
⑴浓硫酸的作用是________________________________________ _________;
若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式
___________________________________________________。
⑵甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲 酯的装置 (夹持仪器和加热仪器均已略去)。
根据有机物的沸点,最好采用______(填“甲”或“乙”)装置。
理由是______________________________________________。
⑶若要提高苯甲酸甲酯的产率,可采取的措施_
______ _。(任写一条)
Ⅱ.粗产品的精制
⑷苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称。
⑸通过计算,苯甲酸甲酯的产率为__________________________________。
【化学选修-化学与技术】(15分)
电石浆是氯碱工业中的一种废弃物,其大致组成如下表所示:
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程:
已知氯化钙晶体的化学式是:CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
⑴反应器中加入的酸应选用___________________。
⑵脱色槽中应加入的物质X是_______________;设备A的作用是______________;设备B的名称为________________;设备C的作用是____________________。
⑶为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是____________ _。反应的化学方程式为_________________。
| A.水 | B.浓硫酸 | C.石灰乳 | D.硝酸 |
⑷将设备B中产生的母液重新引入反应器的目的是______________________。
⑸氯碱工业离子方程式_____________________。
【化学选修-物质结构与性质】(15分)
已知前四周期六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大。B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成A2C型离子化和物,其中的阴、阳离子相差一个电子层,E4+离子和氩原子的核外电子排布相同。
请回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序是____________(填元素符号)
⑵化合物BD3的分子空间构型可描述为_________,B的原子轨道杂化类型为________。
⑶已知F元素在人体内含量偏低时,会影响O2在体内的正常运输。已知F2+与KCN
溶液反应得F(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物。则F的基态原子价电子排布式为________________。CN-与___________(一种分子)互为等电子体,则1个CN-中π键数目为___________。
⑷EO2与碳酸钡在熔融状态下反应,所得晶体的晶
胞结构如图所示,则该反应的化学方程式为________
在该晶体中,E4+的氧配为数为____________。若该
晶胞边长为a nm可计算该晶体的密度为__________
g/cm3(阿伏加德罗常数为NA)
【化学选修-有机化学基础】以烯烃为原料,合成某些高聚物的路线如下:
已知: (或写成
(或写成 )
)
⑴CH3CH=CHCH3的名称是____________。⑵X中含有的官能团是______________。
⑶A→B的化学方程式是_____________。⑷D→E的反应类型是_______________。
⑸甲为烃,F能与NaHCO3反应产生CO2。
①下列有关说法正确的是_______________。
a.有机物Z能发生银镜反应 b.有机物Y与HOCH2CH2OH互为同系物
c.有机物Y的沸点比B低 d.有机物F能与己二胺缩聚成聚合物
②Y的同分异构体有多种,写出分子结构中含有酯基的所有同分异构体的种类数__ ___。
③Z→W的化学方程式是__________________。
⑹高聚物H的结构简式是_________________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号