题客网高考押题卷 第三期(浙江版)化学
下列说法正确的是
| A.质谱法和核磁共振法不仅可用于有机小分子结构的分析,还可用于蛋白质结构的研究 |
| B.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5比胶体粒子小,因其比表面积大,故可吸附重金属离子,入肺后对人体产生很大的危害 |
| C.气化、液化和干馏是煤综合利用的主要方法,这三者中只有干馏是化学变化 |
| D.蛋白质遇双缩脲试剂时会呈现紫玫瑰色,凡含有肽键的化合物均能发生该反应 |
下列说法不正确的是
| A.制阿司匹林时用水洗涤产品,而在制摩尔盐时用酒精洗涤产品 |
| B.纸层析法通常把不与水混溶的有机溶剂作为固定相 |
| C.中和滴定实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,必须干燥或润洗后方可使用 |
| D.减压过滤装置中,布氏漏斗的颈口斜面应与吸滤瓶的支管口相对,以便于吸滤 |
已知X、Y、Z、W四种元素是元素周期表中三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的气态氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。下列说法正确的是
| A.X、Y、Z三种元素既能形成共价化合物也能形成离子化合物 |
| B.Y、Z、W三种元素形成的物质水溶液一定呈中性 |
| C.上述四种元素原子半径大小关系是W>Z>Y>X |
| D.W与Z形成的化合物一定是碱性氧化物 |
下列说法正确的是
A.按系统命名法,化合物 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 |
B.月桂烯( )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 |
| C.取卤代烃,加入氢氧化钠的乙醇溶液加热一段时间后冷却,再加稀硝酸酸化的硝酸银溶液,一定会产生沉淀,并根据沉淀颜色判断卤代烃中卤原子的种类 |
D.通常条件下,1mol的 分别与H2和浓溴水完全反应时,消耗H2和Br2的物质的量分别是4mol、3mol 分别与H2和浓溴水完全反应时,消耗H2和Br2的物质的量分别是4mol、3mol |
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯分析仪(图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。
下列有关叙述正确的是
| A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| B.电极b是正极,O2-由电极a流向电极b |
| C.电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| D.当固体电解质中有1molO2-通过时,电子转移4mol |
下列说法正确的是
| A.在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| B.pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
C.室温下向10 mL pH=3的醋酸溶液中加水稀释,溶液中 不变 不变 |
| D.在0.1 mol·L-1的硫化钠溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
有一无色溶液,仅含有K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,无沉淀产生。下列推断正确的是
| A.肯定有Al3+、Mg2+、Cl-,可能有NH4+ |
| B.肯定有Al3+、Mg2+、 HCO3-,肯定没有 MnO4- |
| C.肯定有Al3+、Mg2+、Cl-,可能有K+ |
| D.肯定有K+、Al3+、MnO4-,可能有HCO3- |
(14分)甲、乙、丙三种化合物均由氢、氮、氧、铜四种元素中的两种组成。常温下,甲是一种含氮质量分数为87.5%的液态化合物,其相对分子质量与空气中某种主要成分的相对分子质量相等;乙和丙是铜的两种常见氧化物,乙是新制氢氧化铜与乙醛反应的还原产物。试回答下列问题:
(1)甲的结构式 。
(2)甲是一种二元弱碱,则甲与过量硫酸反应的产物为 (写化学式)。16g甲在空气中充分燃烧,生成一种常见液态物质和氮气,放出311kJ热量,则其热化学方程式为 。
(3)甲和丙反应的产物中含有乙和一种气态单质,写出其化学方程式 。
(4)向乙的固体中加入过量硫酸酸化的硫酸铁溶液,乙固体完全溶解,得到透明溶液。
①写出其离子方程式 。
②若所得溶液中阳离子浓度均约为0.1mol/L,再向所得混合溶液中加丙,最先得到 沉淀(不同浓度的阳离子开始和完全以氢氧化物沉淀的pH如下图)。
③向上述混合液中加入有机萃取剂(RH)发生反应:2RH(有机相)+Cu2+(水相) R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。请设计实验方案,验证有机相中含有铜元素。
R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。请设计实验方案,验证有机相中含有铜元素。
(15分)甲醇(CH3OH)是用来制备汽油添加剂和许多普通塑料的原料,低温液相合成甲醇的方法如下。
反应原理:2H2+ CO→CH3OH;反应条件:以三乙二醇二甲醚作为溶剂,以Raney-Ni和CH3ONa为催化剂。
(1)氢碳比[γ = ]:当γ=2时,甲醇的选择性[λ =
]:当γ=2时,甲醇的选择性[λ = ]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
(2)干燥除水:为防止CH3ONa的水解,必须干燥除水,下表是不同干燥方法时对CO转化率的影响。
| 序号 |
干燥方法 |
CO转化率/% |
| ① |
不处理 |
40.2 |
| ② |
无水乙醇洗 |
56.3 |
| ③ |
以四氢呋喃洗 |
62.4 |
| ④ |
无水乙醇洗并真空干燥 |
70.1 |
| ⑤ |
|
77.2 |
从实验设计完整性思考,请补充实验⑤中的干燥方法。
(3)反应温度:下图是 = 2时甲醇合成过程中压力和温度随时间变化的图像。
= 2时甲醇合成过程中压力和温度随时间变化的图像。
在反应CO(g)+2H2(g)→CH3OH(g) △H中,△H 0(填“>”或“<”);0~t2时间段内,随反应的进行体系的压力先增大后减小,原因是 ;能判断该反应基本结束的时刻为 ;若t3时刻,测得平衡后CO的转化率为75%,若起始反应时的CO的物质的量为a mol,假设反应容器的体积为1L,则t3时的平衡常数的值为 。
(4)催化剂:在保持其它条件不变,只改变催化剂的用量,分别在1L恒容密闭容器中反应,测定10min时的CO转化率。下图是Raney-Ni为0.05g时,CO转化率与时间关系图,请画出Raney-Ni为1g时,CO转化率与时间变化图。
(15分)阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
主要试剂和产品的物理常数
| 名称 |
相对分子质量 |
熔点或沸点(℃) |
水 |
| 水杨酸 |
138 |
158(熔点) |
微溶 |
| 醋酸酐 |
102 |
139.4(沸点) |
反应 |
| 乙酰水杨酸 |
180 |
135(熔点) |
微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是________________。
(2)①合成阿司匹林时,最合适的加热方法是__________________________。
②加热后冷却,未发现被冷却容器中有晶体析出,此时应采取的措施是_________________。
③抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是____________________。
(3)另一种改进的提纯方法,称为重结晶提纯法。方法如下: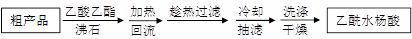
改进的提纯方法中加热回流的装置如图所示。
①使用温度计的目的是________________;
②此种提纯方法中乙酸乙酯的作用是________________,所得产品的有机杂质要比原方案少,原因是___________________________________。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号