高考化学一轮复习课后规范训练3-4练习卷
下列关于金属元素的叙述正确的是( )
| A.金属元素的单质只有还原性,其离子只有氧化性 |
| B.金属元素的单质在常温下均为固体 |
| C.金属元素在不同化合物中化合价均相同 |
| D.大多数金属元素的单质为电的良导体 |
金属材料在日常生活以及生产中有着广泛应用。下列关于金
属的一些说法不正确的是( )
| A.合金的性质与其成分金属的性质不完全相同 |
| B.工业上金属Mg、Cu都是用热还原法制得的 |
| C.金属冶炼的本质是金属阳离子得到电子变成金属原子 |
| D.越活泼的金属越难冶炼 |
下列关于生铁和钢的叙述,正确的是( )
| A.由铁矿石炼成铁是化学变化,由生铁炼成钢是物理变化 |
| B.用铁制容器盛放硫酸铜溶液,容器易被腐蚀 |
| C.生铁和钢都是铁、碳合金,它们在性能和用途上差别不大 |
| D.它们都能完全溶解在盐酸中 |
下列说法中,正确的是( )
| A.铁是人类在生产、生活中最早使用的金属 |
| B.金、银、铜是应用最广泛的金属材料 |
| C.钛被誉为“21世纪的金属”,应用前景很广阔 |
| D.铜是导电性、导热性最好的有色金属 |
下列有关金属的说法中,不正确的是( )
| A.青铜、不锈钢、硬铝都是合金 |
| B.铜表面易形成致密的氧化膜 |
| C.工业上用电解熔融MgCl2的方法制取金属镁 |
| D.铝是活泼金属,但在空气中耐腐蚀 |
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,下表为四种金属的熔、沸点:
| |
Na |
Cu |
Al |
Fe |
| 熔点(℃) |
97.5 |
1 083 |
660 |
1 535 |
| 沸点(℃) |
883 |
2 595 |
2 200 |
3 000 |
根据以上数据判断其中不能形成合金的是( )
A.Cu和Na B.Fe和Cu
C.Fe和Al D.Al和Na
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存
在,下列判断不正确的是( )
| A.加入KSCN溶液一定不变红色 |
| B.溶液中一定含Fe2+ |
| C.溶液中一定含Cu2+ |
| D.剩余固体中一定含铜 |
稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。
已知:①铈常见的化合价为+3和+4;②氧化性:Ce4+>Fe3+。下列说法正确的是( )
A. Ce、 Ce、 Ce、 Ce、 Ce、 Ce、 Ce它们互称为同素异形体 Ce它们互称为同素异形体 |
| B.工业上可以采用电解氯化铈水溶液来获得铈单质 |
| C.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI=2CeI3+3H2↑ |
| D.工业上金属铈一般保存在敞口容器中 |
铅的冶炼大致过程如下:
①富集:将方铅矿(PbS)进行浮选;②焙烧:2PbS+3O2 2PbO+2SO2;③制粗铅:PbO+C
2PbO+2SO2;③制粗铅:PbO+C Pb+CO↑;PbO+CO
Pb+CO↑;PbO+CO Pb+CO2。
Pb+CO2。
下列说法正确的是( )
| A.浮选法富集方铅矿的过程属于化学变化 |
| B.方铅矿焙烧反应中,PbS是还原剂,还原产物只有PbO |
| C.整个冶炼过程中,制取1 mol Pb共转移2 mol电子 |
| D.将l mol PbS完全冶炼成Pb理论上至少需要6 g碳 |
常温下,向含有H2SO4的CuSO4溶液中逐滴加入含a mol
溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述错误的是( )
| A.反应后溶液中c(Na+)=2c(SO42—) |
| B.a/2 mol>沉淀的物质的量>0 |
| C.沉淀的质量为49 a g |
| D.溶液中n(SO42—)=a/2 mol |
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,熔点422
℃,沸点1366 ℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO42—等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下: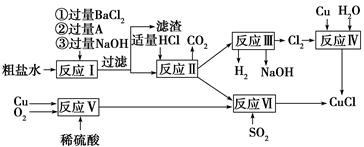
(1)A的化学式为________。
(2)写出反应Ⅴ的化学方程式______________________________________
(3)写出反应Ⅵ的离子方程式______________________________________
(4)本工艺中可以循环利用的物质是(用化学式表示)___________________________
(5)反应Ⅵ后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70 ℃ 燥2小时,冷却,密封包装即得产品。于70 ℃真空干燥的目的是_________________________
利用废铁丝、硫酸铜废液(含硫酸亚铁)和被有机物污染的废
铜粉制备硫酸铜晶体。生产过程如下:
试回答下列问题:
(1)铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,可能发生反应的离子方程式有______________________________________________
(2)废铜粉与还原所得铜粉混合灼烧,检验发现灼烧后得到的是CuO和少量Cu的混合物。原因可能是:
①灼烧不充分Cu未被完全氧化。
②CuO被还原。还原剂可能是________,该反应的化学方程式是___________________
(3)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)____________________。
(4)直接向氧化铜混合物中加入浓硫酸并加热进行酸溶,也可达到充分酸溶的目的,但实际操作中较少使用,原因可能是__________________________________________
已知常温下D、E、F、H、L、N均为气体;A的焰色反应呈黄色;向B的溶液中滴加KSCN溶液,无明显现象;1 mol B隔绝空气分解得到F、G、H三种氧化物,其物质的量均为1 mol;F是易与血红蛋白结合的物质;J是现代社会中应用最广泛的金属单质。
请回答下列题:
(1)B的化学式为________;H的结构式为________
(2)电解A溶液的离子方程式为______________________________________
(3)D与E反应可制得一种重要的化工原料,其反应的现象是____________________________
(4)F与G反应的化学方程式为________________________________
碱式碳酸铜可表示为:xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种(Cu
的相对原子质量按63.5计)。
(1)现采用氢气还原法,请回答下列问题:
已知xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式为xCuCO3·yCu(OH)2·zH2O+(x+y)H2 (x+y)Cu+xCO2+(x+2y+z)H2O
(x+y)Cu+xCO2+(x+2y+z)H2O
①实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l);
②称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为________g,化学式为________。
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由_________________________________________________________
 粤公网安备 44130202000953号
粤公网安备 44130202000953号