高考化学苏教版总复习 10-2 物质的检验、分离和提纯练习卷
下列叙述中正确的是( )
| A.液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
下列叙述错误的是( )
| A.用金属钠可区分乙醇和乙醚 |
| B.用高锰酸钾酸性溶液可区分己烷和3-己烯 |
| C.用水可区分苯和溴苯 |
| D.用新制的银氨溶液可区分甲酸甲酯和乙醛 |
下列实验操作正确的是( )
| A.中和滴定实验时,用待测液润洗锥形瓶 |
| B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶 |
| C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| D.NaCl溶液热发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
不能鉴别AgNO3、BaCl2、K2SO3和Mg(NO3)四种溶液(不考虑它们间的相互反应)的试剂组是( )
| A.盐酸、硫酸 | B.盐酸、氢氧化钠溶液 |
| C.氨水、硫酸 | D.氨水、氢氧化钠溶液 |
用下列实验装置进行相应实验,能达到实验目的的是( )
| A.用图①所示装置除去Cl2中含有的少量HCl |
| B.用图②所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图③所示装置制取少量纯净的CO2气体 |
| D.用图④所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
下列有关分离和提纯的说法正确的是( )
| A.用浓溴水除去苯中混有的苯酚 |
| B.用蒸馏的方法从海水中得到淡水 |
| C.用分液的方法分离乙酸和乙酸乙酯 |
| D.用浓硫酸除去氨气中混有的水蒸气 |
下列关于离子检验的说法中正确的是( )
| A.向某溶液中加入澄清石灰水,溶液变浑浊,则该溶液一定含有CO32- |
| B.向某溶液中加入AgNO3溶液,生成白色沉淀,该溶液中一定含有Cl- |
| C.向某溶液中加入盐酸化的BaCl2溶液,有白色沉淀生成,该溶液中一定含有SO42- |
| D.向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
取少量无机盐溶液,对其中的离子进行检验。下列判断正确的是( )
| A.加入盐酸,产生白色沉淀,则试样中一定有Ag+ |
| B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- |
| C.加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+ |
| D.加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42- |
下列除去杂质的方法正确的是( )
| A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气 |
| B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤 |
为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是( )
| A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.取少量硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
| C.取少量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取少量硫酸亚铁铵晶体放入试管中,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
下列有关物质检验的实验结论正确的是( )
| |
实验操作 |
现象 |
实验结论 |
| A |
向某溶液中加入盐酸酸化的氯化钡溶液 |
有白色沉淀生成 |
溶液中一定含有SO42- |
| B |
将某气体通入澄清石灰水中 |
变浑浊 |
该气体一定是CO2 |
| C |
向某溶液中加入2滴KSCN溶液 |
溶液不显红色 |
溶液中一定含有Fe2 |
| 另取样,先滴入氯水,再滴入KSCN溶液 |
溶液变为红色 |
||
| D |
将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热 |
有银镜生成 |
该物质一定是葡萄糖 |
某同学为检验溶液中是否含有常见的几种无机离子,进行了如下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
| A.原溶液中一定含有SO42- |
| B.原溶液中一定含有NH4+ |
| C.原溶液中一定含有Cl- |
| D.原溶液中一定含有Fe3+ |
有一无色透明溶液,欲确定是否含有下列离子: Fe2+、Mg2+、Al3+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液进行实验:
| 实验步骤 |
实验现象 |
| (1)取少量该溶液,加几滴紫色石蕊试液 |
溶液变红 |
| (2)取少量该溶液加热,加Cu片和浓H2SO4,加热 |
有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加BaCl2溶液 |
有白色沉淀 |
| (4)取(3)中上层清液,加AgNO3溶液 |
有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 |
有白色沉淀,NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定不存在的离子有________,溶液中肯定存在的离子是____。
(2)请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论)_____。
有一瓶澄清的溶液,其中可能有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Cl-、I-、NO3-、CO32-、S2-、SO42-、AlO2-、MnO4-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性,可以排除________离子的存在;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫色,可以排除________离子的存在;
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除________离子的存在;
(4)取出部分上述碱性溶液滴加Na2CO3溶液后,有白色沉淀生成,证明________离子存在,又可排除________离子的存在;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确定:该溶液中肯定存在的离子是________,还不能确定是否存在的离子是________。
请你利用下列装置来证明浓硫酸与足量锌反应时可得到SO2、H2两种气体,所需试剂自选。
(1)在下面的方框中,画出实现上述实验目的的装置示意图(仪器选自于下图,夹持装置、连接胶管、橡皮塞及尾气处理装置不必画出,也不必标出装置内试剂,需要加热的仪器下方用△标出),按气流流向在每件仪器下方标出字母A、B、C……其他可选用的仪器(数量不限)简易表示如下: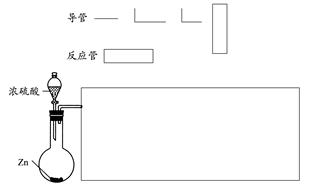
(2)根据方框中的装置图,填写下表:
| 仪器符号 |
仪器中所加物质 |
作用 |
| |
|
|
| 最后一种装置(作图时请对其编号) |
浓硫酸 |
防止空气中水蒸气进入E中干扰实验 |
下表是实验室制备气体的有关内容:
| 编号 |
实验内容 |
实验原理 |
气体发生装置 |
| ① |
制氧气 |
H2O2―→O2 |
|
| ② |
制氨气 |
NH4Cl―→NH3 |
|
| ③ |
是氯气 |
HCl―→Cl2 |
|
(1)上表气体中:从制备过程看,必须选择合适的氧化剂才能实现的是________(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是________。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。
(3)若用上述制备O2的装置制备NH3,则选择的试剂为________________。
(4)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
①为提高配制的精确度,量取浓盐酸的仪器可选用下列中的________(填序号):
②配制过程中,除上图所列仪器外,还需要的仪器有________、________、________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号