高一化学人教版必修二 4-1-2海水资源的开发利用练习卷
下列说法正确的是( )
| A.海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约 |
| B.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法 |
| C.海水淡化的各种方法中,蒸馏法的成本比较低 |
| D.以上说法都正确 |
下列关于海水知识的叙述中不正确的是( )
| A.海水资源的利用包括海水水资源的利用和海水化学资源的利用 |
| B.海水既苦又涩,不能直接利用 |
| C.海水中某些金属元素总储量大,但富集程度却很低 |
| D.海水淡化应同化工生产、能源技术结合 |
下列从海水中提取镁正确的方法是( )
(提示:熔点:MgO 2 850℃ MgCl2 714℃)
A.海水 Mg(OH)2 Mg(OH)2 Mg Mg |
B.海水 MgCl2溶液→MgCl2晶体 MgCl2溶液→MgCl2晶体 Mg Mg |
C.海水 Mg(OH)2 Mg(OH)2 MgO MgO Mg Mg |
D.海水 Mg(OH)2 Mg(OH)2 MgCl2溶液→MgCl2晶体 MgCl2溶液→MgCl2晶体 Mg Mg |
海水中含有氯化镁,是镁的重要来源之一。从海水中提取镁,可按照以下步骤进行:
①把贝壳制成石灰乳
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤、干燥产物
④将所得的产物熔融后电解。
关于提取镁,下列说法不正确的是( )
| A.此法的优点之一是原料来源丰富 |
| B.进行①、②、③步操作的目的是从海水中提取氯化镁 |
| C.第④步电解时会产生氯气 |
| D.以上提取镁的过程中涉及的反应有分解反应、化合反应、复分解反应和置换反应 |
海水是镁的主要来源之一,从海水中提取镁可按如下步骤进行:①把贝壳(主要成分是碳酸钙)煅烧成石灰;②在引有海水的渠中加入石灰,经过沉降,然后过滤得沉淀物;③将沉淀物与稀盐酸反应,然后结晶、过滤、干燥;④电解得产品。以上提取镁的全过程中,没有涉及的反应类型有( )
| A.分解反应 | B.化合反应 |
| C.置换反应 | D.复分解反应 |
从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法是( )
| A.加入适量的Na2CO3溶液 |
| B.通入溴蒸气 |
| C.加入适量的NaOH溶液 |
| D.加入适量的NaBr溶液 |
从海带中提取碘单质的过程涉及氧化还原反应
B.往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输
C.赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的
D.海洋经济专属区的资源开发可获得Fe、Co、K、Au、Mg、B等金属
下列说法正确的是( )
| A.海水中含量最高的元素是氯 |
| B.海水中含量最高的物质是氯化钠 |
| C.加碘食盐溶液遇淀粉溶液显蓝色 |
| D.加碘食盐中的碘是含碘元素的化合物 |
下列元素①Cl、②Na、③Br、④I、⑤Mg、⑥U,属于海水中的微量元素的是( )
| A.①②⑤ | B.④⑥ |
| C.①②③④ | D.③④⑤⑥ |
某同学设计实验从海带中提取碘:①滴加稀硫酸和双氧水;②在海带中加入少量酒精,点燃使其燃烧为灰烬,在灰烬中加水搅拌;③加四氯化碳并振荡;④过滤;⑤分液。该实验的合理操作顺序是( )
| A.①③⑤②④ | B.②①③④⑤ |
| C.②④①③⑤ | D.③①②⑤④ |
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下: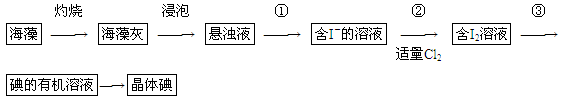 (1)实验操作③的名称是________,所用主要仪器名称为________。
(1)实验操作③的名称是________,所用主要仪器名称为________。
(2)提取碘的过程中,可供选择的有机试剂是________(填序号)。
A.酒精(沸点78℃) B.四氯化碳(沸点77℃)
C.甘油(沸点290℃) D.苯(沸点80℃)
(3)在操作②中,溶液中生成少量ICl(ICl的性质类似于氯气),为消除此杂质,使碘全部游离出来,应加入适量(填序号)________溶液,反应的离子方程式______________________。
A.KIO3 B.HClO C.KI D.Br2
(4)利用碘的有机溶液得到单质I2的方法是_______________________________________。
目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是________,写出在沉淀池中发生反应的离子方程式:_________________________________________________。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度考虑,生产生石灰的主要原料来源于海洋中的________。
(3)操作A是________,操作B是________。
(4)加入的足量试剂a是________(填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为________,从考虑成本和废物循环利用的角度,副产物氯气可以用于________。
海水占地球总储水量的97%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。也可以电解熔融氯化钠制得钠和氯气,该反应方程式为________________________。
(2)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
试写出反应的化学方程式:
②__________,③__________,④__________。
目前世界上60%的镁是从海水中提取的。已知海水提取镁的主要步骤如下:
(1)关于加入试剂①作沉淀剂,有以下几种不同方法,请完成下列问题。
| 方法 |
是否正确 |
简述理由 |
| 方法1:直接往海水中加入沉淀剂 |
不正确 |
(一) |
| 方法2:高温加热蒸发海水后,再加入沉淀剂 |
(二) |
(三) |
| 你认为最合理的其他方法是: (四) |
(一)_______________________________________________;
(二)_______________________________________________;
(三)______________________________________________;
(四)______________________________________________。
(2)框图中加入的试剂①应该是________(填化学式);加入的试剂②是________(填化学式);工业上由无水MgCl2制取镁的化学方程式为________________________________________。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号