2014高考化学二轮复习限时集训 专题9电化学原理练习卷A
钢铁防腐方法有许多种,如图是其中的一种方法,描述正确的是( )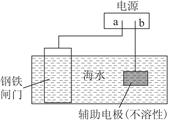
| A.图中所示是牺牲阳极的阴极保护法 |
| B.铁闸门作阴极,发生还原反应 |
| C.电子流向:a→铁闸门→辅助电极→b |
| D.辅助电极上的反应:O2+2H2O+4e-=4OH- |
根据图所示装置,下列说法不正确的是( )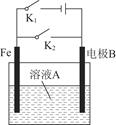
| 选项 |
开关状态 |
溶液A |
电极B |
说明 |
| A |
打开K1,闭合K2 |
NaCl |
石墨 |
正极反应:O2+2H2O+4e-=4OH- |
| B |
打开K1,闭合K2 |
NaCl |
Zn |
铁制品保护:牺牲阳极的阴极保护法 |
| C |
打开K2,闭合K1 |
CuSO4 |
Cu |
铁表面镀铜 |
| D |
打开K2,闭合K1 |
CuSO4 |
粗铜 |
电解法精炼铜 |
肼(N2H4)—空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O。下列关于该电池工作时说法中正确的是( )
| A.正极的电极反应式:O2+4H++4e-=2H2O |
| B.溶液中的阴离子向正极移动 |
| C.负极的电极反应式:N2H4+4OH--4e-=4H2O+N2 |
| D.溶液的pH保持不变 |
保护埋在地下的钢管常用如图所示方法。关于此方法,下列说法正确的是( )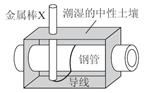
| A.金属棒X的材料可能为铜 |
| B.金属棒X的材料可能为钠 |
| C.钢管附近土壤的pH可能会上升 |
| D.这种方法称为外加电流的阴极保护法 |
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体。Fe(OH)3有吸附性,可吸附污物使之沉积下来,具有净化水的作用。模拟处理装置如图所示,下列说法错误的是( )
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O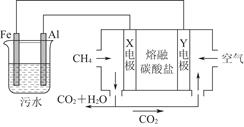 |
| B.铁作阳极,失去电子生成Fe2+ |
| C.工作时熔融盐中的碳酸根移向Y电极 |
| D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ |
科学家们在研制一种吸气式的锂—空气电池,工作时吸收空气中的氧气在多孔金制成的正极表面上反应。总反应可表示为2Li+O2 Li2O2,下列有关说法正确的是( )
Li2O2,下列有关说法正确的是( )
| A.充电时,多孔金制成的电极外接电源负极 |
| B.放电时,吸收空气中22.4 L的O2,就有2 mol e-从电池负极流出 |
| C.放电时,Li+从负极向正极移动 |
| D.该电池可使用含Li+的水溶液作电解质溶液 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOClCl)中形成的,其电池总反应方程式为8Li+3SOCl2=6LiCl+Li2SO3+2S。下列叙述中正确的是( )
| A.电解质溶液可以用水,也可以用饱和食盐水 |
| B.电池工作过程中,亚硫酰氯(SOCl2)被还原成Li2SO3 |
| C.电池工作时,锂电极为正极,石墨电极为负极 |
| D.电池工作过程中,金属锂提供的电子与正极区析出的硫的物质的量之比为4∶1 |
图甲中电极均为石墨电极,下列叙述中正确的是( )
| A.电子沿a→d→c→d路径流动 |
| B.b极的电极反应为O2+4e-+4H+=2H2O |
C.通电初期乙中的总反应为Cu+H2SO4 CuSO4+H2↑ CuSO4+H2↑ |
| D.反应过程中,甲、乙装置中溶液的pH都逐渐减小 |
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。图为RFC工作原理示意图,下列有关说法正确的是( )
| A.图(a)把化学能转化为电能,图(b)把电能转化为化学能,水得到了循环使用 |
| B.当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下) |
| C.c极上发生的电极反应是:O2+4H++4e-=2H2O |
| D.图(b)中电子从c极流向d极,提供电能 |
如图所示,通电一段时间后,Cu电极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为100 mL,则通电前A池中原混合溶液Cu2+的浓度为( )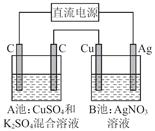
| A.0.05 mol/L | B.0.035 mol/L |
| C.0.025 mol/L | D.0.020 mol/L |
化学能与电能之间的相互转化与人类的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池,如图9-8工作原理示意图,反应原理为2Na+FeCl2 Fe+2NaCl,该电池放电时,正极反应式为________________________________________________________________________;
Fe+2NaCl,该电池放电时,正极反应式为________________________________________________________________________;
充电时,____________(写物质名称)电极接电源的负极;该电池的电解质为________。
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液,工作原理示意图如图所示,一段时间停止通电取出电极。若在电解后的溶液中加入0.98 g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
①Y电极材料是________,发生________(填“氧化”或“还原”)反应。
②电解过程中X电极上发生的电极反应式是_______________________________________________________________________。
③如在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是__________。
电化学原理在工业生产中有着重要的作用,请利用所学知识回答有关问题。
(1)用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容。如图,是电解产生多硫化物的实验装置:
①已知阳极的反应为(x+1)S2-=Sx+S2-+2xe-,则阴极的电极反应式是________________________________________________________________________。
当反应转移x mol电子时,产生的气体体积为____________(标准状况下)。
②将Na2S·9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解。其原因是(用离子反应方程式表示):___________________________________________________。
(2)MnO2是一种重要的无机功能材料,制备MnO2的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为______________________。现以铅蓄电池为电源电解酸化的MnSO4溶液,如图所示,铅蓄电池的总反应方程式为_______________________________________________,当蓄电池中有4 mol H+被消耗时,则电路中通过的电子的物质的量为________,MnO2的理论产量为________g。
(3)用图电解装置可制得具有净水作用的FeO42-。实验过程中,两极均有气体产生,Y极区溶液逐渐生成FeO42-。
①电解过程中,X极区溶液的pH________(填“增大”“减小”或“不变”)。
②电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O和________________________________________________________________________,
若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号