[广东]2014届广东省茂名市高三第一次高考模拟考试理综化学试卷
下列关于常见有机物的说法正确的是
| A.乙炔的化学性质与乙烯相似,也能形成高分子化合物 |
| B.甲烷是水煤气的主要成分 |
C.不粘锅的原料 为烃类化合物 为烃类化合物 |
| D.葡萄糖、鸡蛋清均能与NaOH溶液反应 |
下列化学应用中不涉及氧化还原反应的是
| A.Na2S水溶液在空气中变浑浊 |
| B.生活中使用明矾净水,除去水中的悬浮颗粒 |
| C.溶有二氧化氮的浓硝酸做火箭的助燃剂 |
| D.漂白粉漂白有色布条 |
下列陈述Ⅰ、Ⅱ都正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
非金属性:Cl>S |
酸性:HClO> H2SO3 |
| B |
SO2有氧化性 |
SO2能使酸性KMnO4溶液褪色 |
| C |
NH3.H2O为一元弱碱 |
含有NH4+的水溶液均显弱碱性 |
| D |
锌的金属性比铁强 |
海轮外壳上装锌块可减缓腐蚀 |
下列各组离子在溶液中能够大量共存的是
| A.NH4+、NO3-、Na+、SO42- | B.H+、Fe2+、Na+、NO3- |
| C.Ba2+、K+、Al3+、HCO3- | D.NH4+、Li+、OH-、SO42- |
下列实验方法正确且能达到目的的是
| A.用装置I除去CO2中的SO2 | B.实验室用装置II制备NH3 |
| C.用装置III制备乙烯 | D.装置IV比较酸性H2CO3>苯酚 |
设nA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4L O2与O3混合物含有3nA个氧原子 |
| B.0.1mol/L NH4Cl 溶液中含有NH4+ 数目为0.1nA |
| C.标准状况下,22.4LBr2与足量铁粉反应转移电子数目为2nA |
| D.17g H2O2含有 O-H键数目为nA |
常温下,100ml 蒸馏水中加入0.1mol CH3COONa ,下列说法正确的是
| A.该溶液中存在: c(Na+) + c(H+)=c(OH—)+c(CH3COO—) |
| B.加入酚酞后加热,溶液颜色变浅 |
| C.若在该溶液再通入0.1mol HCl,存在: c(Na+)>c(CH3COO—)> c(H+) |
| D.若在该溶液中再投入0.1mol NaCl,存在: c(Na+)=c(Cl—)+c(CH3COO—)+c(CH3COOH) |
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y: 154pm Z:125pm W: 117pm,X Y W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是
| |
|
|
|
X |
| Y |
|
|
W |
|
A、元素Z处于周期表的阴影位置
B、非金属性:X>W
C、X与W形成化合物熔点很高,为离子化合物
D、Y、W的最高价氧化物对应的水化物能反应
芳香醛与活性亚甲基化合物的缩合反应在有机合成中有重要应用,化合物III是医药中间体,其合成方法如下:
反应①: 
化合物Ⅱ也可以由化合物IV(C3H6Cl2)经以下途经合成: 
(1)化合物II的分子式为 ,1mol化合物III最多与 mol H2发生加成反应。
(2)化合物IV转化为化合物V的反应类型是 ,化合物V和化合物VII能形成一种高分子聚合物,写出该聚酯的结构简式 。
(3)由化合物VI转变成化合物VII分两步进行,其中第一步是由化合物VI与足量的银氨溶液共热反应,写出其化学反应方程式 。
(4)E是化合物II的同分异构体,且E是一种链状结构,在核磁共振氢谱中有3种氢, 1mol E能与2 molNaHCO3反应,写出化合物E的结构简式 。(任写一种;不考虑顺反异构。)
(5)化合物I与化合物 ( )在催化剂条件下也能发生类似反应①的反应得到另一医药中间体,写出该反应化学方程式 。
)在催化剂条件下也能发生类似反应①的反应得到另一医药中间体,写出该反应化学方程式 。
甲醇是一种重要的化工原料。甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。现有如下实验,在体积为1 L的密闭容器中,充入1mol CH3OH和1molH2O,一定条件下发生反应:CH3OH (g)+ H2O (g) CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
| 时间 物质 |
0 min |
10 min |
30 min |
60 min |
70 min |
| CO2(mol/L) |
0 |
0.2 |
0.6 |
0.8 |
0.8 |
| CH3OH(mol/L) |
1.0 |
0.8 |
0.4 |
0.2 |
0.2 |
①已知:CH3OH (g)+ 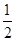 O2 (g)
O2 (g) CO2(g) + 2H2 (g) H1= —192.9kJ/mol
CO2(g) + 2H2 (g) H1= —192.9kJ/mol
H2(g)+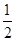 O2 (g)
O2 (g) H2 O(g) H2= —120.9kJ/mol
H2 O(g) H2= —120.9kJ/mol
则甲醇与水蒸气催化重整反应的焓变△H3=_____ 。
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。
③该反应的平衡常数表达式为K=__________________。
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.再充入1molH2O
(2)甲醇在催化剂条件下可以直接氧化成甲酸。
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL) 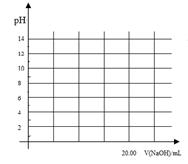
工业上利用含有一定浓度的I2和CuSO4溶液的工业废水制备饲料添加剂Ca(IO3)2,其生产流程如下: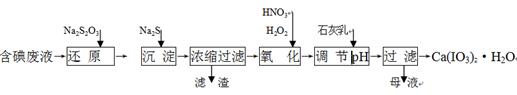
已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3—>H2O2
(1)“还原”过程中主要反应的化学方程式为:2Na2S2O3+I2 = + 2NaI。
(2)在还原过程还伴随有CuI生成,写出加入Na2S的离子反应方程式 。
(3)在氧化过程中先加入H2O2再加入浓硝酸,而不直接加入浓硝酸的目的是 。
(4)加入的石灰乳在溶液中反应而得到Ca(IO3)2,则要调节pH至 (填“酸性” 或“中性”或“碱性”),原因是 。
(5)Ca(IO3)2也可用电化学氧化法制取:先充分电解KI溶液,然后在电解后的溶液中加入CaCl2,最后过滤得到Ca(IO3)2。写出电解时阳极发生的电极反应方程式 ,用该方法制取Ca(IO3)2,每1kg碘化钾理论上可生产纯度为97.8%Ca(IO3)2的质量为 ____kg(计算结果保留3位有效数字)。
某同学利用如图装置制NO并进行相关实验探究。
(1)写出制备NO的反应方程式
(2)收集的气体与空气混合后变红色,这说明NO具有_____性。
(3)制备NO的步骤如下:
1按图所示连接好装置;
2取下注射器,通过U型长管加入稀硝酸至接近U型短管的铜丝
3在针头上安装好注射器,抽出U型短管中的所有空气;然后拔出注射器,并排尽注射器中的空气。
4待硝酸与铜丝分离后,用已排除空气的注射器抽出生成NO,将注射器针头插入橡皮塞中以封口。
在上述操作中遗漏的一个步骤是 ,在步骤3中可以观察到的现象为 。
(4)在铜丝上绑上石墨的作用是 。
(5)若将稀硝酸换成浓硝酸,则可制取NO2气体。请你用注射器收集NO2气体并完成“外界因素对化学平衡移动影响”实验探究,相关内容填在下面表格。(只完成一个影响因素的探究,其他实验用品自选)已知
2NO2(g)  N2O4(g) △H <0;N2O4为无色气体。
N2O4(g) △H <0;N2O4为无色气体。
| 实验步骤 |
实验现象 |
实验结论 |
| ①分别用两支注射器收集NO2,并将注射器针头插入橡皮塞中以封口。 ②_____________________ _______________________ ________________________ _______________________ ________________________ |
_______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ |
_______________________ ________________________ _______________________ ________________________ _______________________ _______________________ ________________________ _______________________ |
 粤公网安备 44130202000953号
粤公网安备 44130202000953号