[北京]2014届北京市房山区高三上学期期末考试化学试卷
下列说法不正确的是
| A.维生素都易溶于水 |
| B.NO2和SO2都是可形成酸雨气体 |
| C.加碘食盐不能使淀粉液变蓝 |
| D.青霉素使用者一定要做皮肤敏感实验 |
下列说法正确的是
| A.光导纤维、石英、硅胶分别属于单质、酸性氧化物、酸 |
| B.Na、Al、Cu可以分别用热还原法、热分解法和电解法冶炼得到 |
| C.氯化钠、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 |
| D.天然气、沼气和液化石油气分别属于化石能源、不可再生能源和二次能源 |
下列化学表达方式不正确的是
| A.中子数为20的氯原子:37Cl |
B.S2-的结构示意图: |
C.CCl4的电子式: |
D.2-甲基丁烷的结构简式: |
下列实验装置、试剂选用或操作正确的是
| A.实验室制乙烯 | B.用水吸收氨气 | C.稀释浓硫酸 | D.海带灼烧成灰 |
下列说法不正确的是
| A.Al2O3、SiC等是耐高温材料 |
| B.将Cl2通入冷的消石灰中可制得漂白粉 |
| C.浓硫酸可用于干燥NH3、SO2、NO2等气体 |
| D.硅酸钠的水溶液是制备硅胶和木材防火剂的原料 |
利用下列各组中的物质制备并收集相应的气体,能采用如图所示装置的是
| A.浓氨水和固体NaOH制NH3 |
| B.过氧化氢溶液和二氧化锰制O2 |
| C.稀硝酸和铜片制NO |
| D.电石和饱和食盐水制乙炔 |
在pH=1的无色溶液中,可以大量共存的一组离子是
| A.NH4+、NO3- 、K+、SO42- | B.Cl-、NO3-、HCO3-、Na+ |
| C.Na+、ClO-、S2-、NO3- | D.MnO4-、K+、Na+、SO42- |
下列说法正确的是
| A.NH4Cl为共价化合物 |
| B.N2分子中含有一对共用电子对 |
| C.Na2O2既含有离子键又含有非极性键 |
| D.电解水与电解熔融NaCl时破坏的化学键类型相同 |
用石墨电极电解CuCl2溶液(见图)。下列分析正确的是
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2+ + 2e- = Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
下列涉及的有机物及有机反应类型正确的是
| A.苯与甲苯均可以使酸性高锰酸钾褪色 |
| B.葡萄糖、蛋白质、纤维素都能发生水解反应 |
| C.甲醛,氯乙烯,乙二醇均可做加聚反应的单体 |
| D.乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
NA表示阿伏加德罗常数,下列说法正确的是
| A.常温常压下,32g O2含有的原子数为2NA |
| B.100mL 1mol·L-1氨水中,含有OH- 离子数是0.1 NA |
| C.100mL 2 mol·L-1碳酸钠溶液中,CO2-3离子数为0.2NA |
| D.标准状况下,22.4LCl2通入足量NaOH溶液,转移的电子数为2NA |
将下表中的Y物质加入或通入X物质中,在反应所得溶液中一定只含一种溶质的是
| 选项 |
X物质 |
Y物质 |
| A |
蒸馏水 |
Na |
| B |
NaOH溶液 |
CO2 |
| C |
NaOH溶液 |
Cl2 |
| D |
稀硝酸 |
Fe |
下列反应中,离子方程式正确的是
| A.大理石溶于盐酸中:CO32-+2H+= CO2↑+H2O |
| B.AlCl3溶液中加入过量氨水:Al3++3NH3•H2O =Al(OH)3↓+ 3NH4+ |
| C.硫酸镁溶液与氢氧化钡溶液混合:SO42- + Ba2+ =BaSO4↓ |
| D.氯化铁溶液中加入铜片:Fe3++Cu = Fe2++Cu2+ |
下列说法正确的是
| A.直接加热蒸干FeCl3溶液,可得FeCl3固体 |
| B.加入催化剂可加快反应速率,并提高反应物的转化率 |
| C.pH值相同的CH3COOH溶液和NH4Cl溶液中,水的电离程度相同 |
| D.可用Na2CO3溶液处理水垢中的CaSO4,转化为易于除去的CaCO3 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
R |
W |
| 原子半径/pm |
160 |
143 |
89 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+2 |
+5、-3 |
-2 |
下列叙述正确的是
A.X、Z元素的金属性:X < Z
B.气态氢化物的稳定性:R > W
C.Y的最高价氧化物既能溶于H2SO4又能溶于NaOH
D.一定条件下,R单质与常见的W单质能直接生成RW2
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
下图所示的实验,能达到实验目的的是
| A |
B |
C |
D |
 |
 |
 |
 |
| 验证化学能转化为电能 |
验证温度对平衡移动的影响 |
验证铁发生析氢腐蚀 |
验证非金属性Cl> C > Si |
绿原酸是咖啡的热水提取液的成分之一,绿原酸结构简式如下:
下列关于绿原酸判断不正确的是
| A.分子中所有的碳原子不可能在同一平面内 |
| B.1mol绿原酸与足量溴水反应,最多消耗4molBr2 |
| C.绿原酸既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
| D.1mol绿原酸与足量NaOH溶液反应,最多消耗8mol NaOH |
对四支分别盛有无色溶液的试管,进行如下操作,结论正确的是
| |
操作 |
现象 |
结论 |
| A. |
滴加氯水和CCl4,振荡、静置 |
下层溶液显紫色 |
原溶液中有I- |
| B. |
滴加BaCl2溶液 |
生成白色沉淀 |
原溶液中一定有SO42- |
| C. |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
原溶液中有Na+、无K+ |
| D. |
滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中一定无NH4+ |
用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是
| A.c(NH4+) > c(Cl-),c(OH-) > c(H+) |
| B.c(Cl-) > c(NH4+),c(OH-) > c(H+) |
| C.c(NH4+) = c(Cl-),c(OH-) = c(H+) |
| D.c(Cl-) > c(NH4+),c(H+) > c(OH-) |
肼(N2H4)是一种可用于火箭或原电池的燃料。已知:
N2(g) + 2O2(g) =2 NO2(g) ΔH =" +67.7kJ/mol" ①
N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH = -534 kJ/mol ②
下列说法正确的是
| A.反应①中反应物所具有的总能量大于生成物所具有的总能量 |
| B.2N2H4(g) + 2NO2(g) = 3N2(g)+ 4H2O (g) ΔH = -1000.3kJ/mol |
| C.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料电池其负极反应式:N2H4-4e-+4OH-=N2+4H2O |
| D.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料,工作一段时间后,KOH溶液的pH将增大 |
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H="-49.0" kJ/mol。一定条件下,向体积为1L的密闭容器中充入1 mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如下图所示。下列叙述中,正确的是
CH3OH(g)+H2O(g) △H="-49.0" kJ/mol。一定条件下,向体积为1L的密闭容器中充入1 mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如下图所示。下列叙述中,正确的是
| A.升高温度能使平衡向正反应方向移动 |
| B.从反应开始到平衡,v(H2)=0.075mol·L-1·min-1 |
| C.3 min时,V(CO2)正 = V(CH3OH)逆 |
| D.反应达到平衡状态时,CO2的平衡转化率为75% |
对羟基苯甲酸乙酯又称尼泊金乙酯,是一种常见的食品添加剂及防腐剂,其生产过程如下:(反应条件未全部注明)
回答下列问题:
(1)D所含官能团的名称 。
(2)有机物G的结构简式 。
(3)反应④的反应类型是 。
(4)反应⑥的试剂和条件是 。
a.乙醇、浓H2SO4 b.乙酸、浓H2SO4
c.乙醇、稀H2SO4 d.乙酸、稀H2SO4
(5)下列四种物质不与H反应的是 。
a.FeCl3溶液 b.NaOH溶液 c.NaHCO3溶液 d.浓Br2水
(6)反应②的化学方程式是
(7)D有多种同分异构体,写出一个与D不同类且含苯环的结构简式: 。
在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+O2 2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。SO2转化为SO3的热化学方程式是 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速度 。该反应K值将 。压强将 。(填“增大”或“减小”或“不变”)
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.缩小容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
如下图装置所示,是用氢氧燃料电池B进行的某电解实验:
(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:
Li2NH+H2=LiNH2+LiH ,则下列说法中正确的是 。
| A.Li2NH中N的化合价是-1 |
| B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 |
| D.此法储氢和钢瓶储氢的原理相同 |
(2)在电池B工作时:
① 若用固体Ca(HSO4)2为电解质传递H+,则电子由 极流出,H+向 极移动。(填“a”或“b ”)
② b极上的电极反应式为:
③ 外电路中,每转移0.1 mol电子,在a极消耗 L的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCl溶液,则B工作时:
① 电解池中X极上的电极反应式是 。在X极这边观察到的现象是 。
② 检验Y电极上反应产物的方法是 。
③ 若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是 。
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B反应的化学方程式为 。
(2)若D是金属,C溶液在贮存时应加入少量D,其理由是(用必要的文字和离子方程式说明) 。
(3)若D是一种常见的温室气体,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,固体C受热分解可得固体B,该反应的化学方程式是 。
(4)若D为氯碱工业的主要产品,B具有两性,则B转化为C的离子方程式为 。
(5)若A、B、C均为氧化物,D是一种黑色固态非金属单质,则元素D在周期表中的位
置是 ,B分子的结构式为 。
以聚甲基丙烯酸羟乙基酯(HEMA)为材料,可制成软性隐形眼镜。其合成路线图如下:
已知:
回答以下问题:
(1)A的官能团的名称是
(2)反应①的反应类型是
(3)写出下列反应的化学方程式
反应②
反应③
(4)下列说法正确的是(选填字母)
a.I具有顺反异构现象
b.G可以使酸性高锰酸钾褪色
c.F的核磁共振氢谱有三种峰,其峰面积之比为1:2:3
d.D可以发生银镜反应
(5)F可以与氢气发生加成反应,加成后的产物有多种同分异构体,其中含-COO-的有
种,写出其中一种的结构简式 。
利用含锰废水(主要含Mn2+、SO42-、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工业流程如下: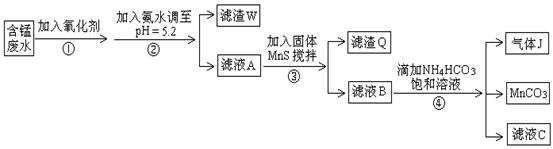
已知某些物质完全沉淀的pH值如下表:
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
Mn(OH)2 |
CuS |
MnS |
MnCO3 |
| 沉淀完全时的PH |
3.7 |
5.2 |
6.4 |
9.8 |
≥0 |
≥7 |
≥7 |
回答下列问题:
(1)若下列物质均能把Fe2+氧化为Fe3+,则过程①中可选择加入的氧化剂是 。
a.Cl2 b.MnO2 c.浓HNO3 d.H2O2
(2)过程②中,所得滤渣的成分是 。
(3)过程③中,搅拌的目的是 ,发生反应的离子方程式是 。
(4)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3反应的离子方程式是___________。
(5)由MnCO3可制得重要的催化剂MnO2,MnCO3 +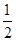 O2 → MnO2 + CO2。
O2 → MnO2 + CO2。
现在空气中加热 460.0 g的MnCO3,得到332.0 g产品,若产品中杂质只有MnO,则该产品中MnO2的质量分数是 。(摩尔质量/g·:MnCO3 115 MnO2 87 MnO 71)
如图是某研究性学习小组设计的SO2与Na2O2反应的探究装置.
(1)实验开始时,打开旋塞K,通入N2排尽整套装置中的空气,关闭旋塞K。点燃酒精灯,A中反应的化学方程式是 。
(2)B装置的作用是 。
(3)反应过程中,观察到:A中出现黑色不溶物;C中固体由淡黄色逐渐至完全转化为白色;若将带火星木条伸入D试管口内,火星显得更明亮。
①停止加热后,再通入N2至整套装置冷却,其目的是 。
②取少量C中白色固体,溶于蒸馏水得无色溶液W 。若向W中滴加几滴酸性KMnO4溶液,振荡,紫色褪去;若向W中加入用盐酸酸化的BaCl2溶液,出现大量白色沉淀;则说明C中白色固体有 。
③D装置中发生反应的离子方程式是 。
④过滤出A装置中的黑色不溶物,洗涤后将其溶于浓硝酸,得到蓝色溶液并产生红棕色气体;向蓝色溶液中滴加BaCl2溶液,产生白色沉淀;则黑色物质可能是___________。
a.Cu b. CuO c.CuS d.Cu2S
 粤公网安备 44130202000953号
粤公网安备 44130202000953号