[上海]2014届上海市普陀区中考期末(一模)考试化学试卷
下图依次是金刚石、石墨、C60的结构示意图,它们是同素异形体,化学性质相似,物理性质却有很大差异。其原因是
| A.构成的原子种类不同 |
| B.构成的原子大小不同 |
| C.不同种原子空间排列不同 |
| D.同种原子的空间排列不同 |
小明在探究蔗糖的性质实验前,所做的假设属于化学变化范畴的是
| A.能否溶于酒精 | B.能否磨碎变成糖粉 |
| C.能否变成酒精 | D.能否通过结晶方法变成大晶体 |
在加压条件下,25m3的天然气可以装入0.024m3的钢瓶中,由此可以说明
| A.分子的大小可以改变 | B.分子之间有间隔 |
| C.分子在不断地运动 | D.分子由原子构成 |
打开汽水瓶盖,有大量CO2气体逸出,下列说法错误的是
| A.溶质减少 | B.浓度减小 |
| C.溶解度减小 | D.变为CO2的不饱和溶液 |
某学校化学课外活动小组的同学,取刚降到地面的雨水的水样,用pH计(测pH的仪器)每隔10分钟测一次pH,其数据如下表所示,其中雨水酸性最强的时刻是:
| 测定时间 |
16:00 |
16:10 |
16:20 |
16:30 |
| pH |
4.95 |
4.93 |
4.86 |
4.84 |
A.16:00 B.16:10 C.16:20 D.16:30
下列四组物质,能用酚酞区别的是
| A.氯化铵溶液与氯化钠溶液 | B.纯碱溶液与氨水 |
| C.生石灰与熟石灰 | D.氨水与硝酸溶液 |
对于甲烷燃烧的方程式CH4+2O2 CO2+2H2O,下列理解错误的是
CO2+2H2O,下列理解错误的是
| A.16g甲烷和32g氧气反应生成44g二氧化碳和18g水 |
| B.1mol甲烷和2mol氧气反应生成1mol二氧化碳和2mol水 |
| C.1个甲烷分子和2个氧气分子反应生成1个二氧化碳分子和2个水分子 |
| D.甲烷和氧气在点燃的条件下生成二氧化碳和水 |
实验室中将新制得的还原铁粉(颗粒极细)撒落到空气中,可以见到铁粉在空气中燃烧发出火星,对此现象认识错误的是
| A.燃烧需要助燃剂,比如氧气 |
| B.燃烧物由于状态不同,着火点可以发生变化 |
| C.该反应一定是氧化反应 |
| D.铁的燃烧是放热反应 |
将100g质量分数为0.05%的食盐溶液改变成质量分数为0.10%,则下列操作可行的是
| A.加入5g食盐 | B.蒸发掉50g水 |
| C.加入50g食盐 | D.取出50g溶液即可 |
实验室利用H2+CuO Cu+H2O反应原理(实验装置见下图),测定水分子中氢氧原子的“相对原子质量”比值,实验室中制得的氢气中有少量水蒸气。则有关实验操作说法正确的是
Cu+H2O反应原理(实验装置见下图),测定水分子中氢氧原子的“相对原子质量”比值,实验室中制得的氢气中有少量水蒸气。则有关实验操作说法正确的是
| A.只需要获得氧化铜粉前后的质量差 |
| B.只需要获得无水硫酸铜前后的质量差 |
| C.若没有“甲”装置,所得比值偏大 |
| D.实验中一定要通入足量的氢气将氧化铜完全反应 |
氧气是我们身边常见的物质,请回答以下问题:
(1)写出实验室利用双氧水分解制取氧气的化学方程式 ;
(2)将硫粉在空气中燃烧,除见到淡蓝色火焰外,还具有的现象是 ,并写出该反应的化学方程式 ;
(3)我们生活离不开氧气,但是某些方面氧气也给生活、生产造成不利的一面,请写出一条有关氧气不利的一面 。
(4)实验室制取氧气,利用的化学反应常常是分解反应,而不会是化合反应,理由是 。
“达菲”是目前世界上治疗H1N1流感病毒的良药。生产“达菲”的主要原料是莽草酸,可从茴香中提取。如图为莽草酸理化性质的描述。回答下列问题:
(1)莽草酸物质中,共有 种元素,其中氢、氧两种元素的质量比为 ,碳、氧原子的个数之比为 。
(2)其中属于化学性质的是 (填图中序号)。
(3)莽草酸的摩尔质量是 g/mol。
水是非常良好的溶剂,是生活、生产中最重要的物质,请回答下列问题:
(1)KNO3溶于水后得到的溶液,具有稳定性和 性。根据如图所示的KNO3和NaCl的溶解度曲线回答下列问题。
(2)50℃时,KNO3的溶解度 (填“大于”、“等于”或“小于”)NaCl的溶解度;
(3)10℃时,KNO3的溶解度约为 ;
(4)在温度不变的情况下,将NaCl的不饱和溶液变成饱和溶液,可采用恒温蒸发水和 的方法。
(5)在40℃时,将质量分数相等的KNO3和NaCl溶液,冷却到20℃,此时有关它们质量分数的关系,下列说法错误的是 (选填编号)
A.可能KNO3溶液质量分数大
B.可能NaCl溶液质量分数大
C.两者可能仍旧相等
为控制大气中“温室效应”(CO2、CH4)气体的排放量,“低碳”正成为人们的共识。
(1)近几十年来大气中二氧化碳含量不断上升的主要原因是 。
(2)生活中燃烧等物质的量的碳、一氧化碳、甲烷,最终排放出的二氧化碳的量 (选填编号)
| A.一样多 | B.碳多 | C.一氧化碳多 | D.甲烷多 |
(3)CO2常用来做灭火剂,但是遇到特殊物质时,CO2也能支持燃烧,写出镁条在CO2中燃烧的化学方程式 ,该反应中做还原剂的是 。
(4)实验室制取二氧化碳,采用的实验原理用化学方程式表示为 ;
若用左图制取CO2则碳酸钙固体应该放置的位置是 ,若用右图收集CO2则气体进入的导管口应该是 (以上均用图中英文编号填写)。
(5)实验室利用澄清石灰水检验CO2时发生的化学方程式为 。
测定溶解度有多种方法,下列是测定30℃时硫酸铜溶解度的实验方法。经查找资料,30℃时硫酸铜的溶解度为25g/100gH2O。
一、配置30℃时的硫酸铜饱和溶液:
(1)配置的步骤如图:
取用100mL水,图中称量得到22.2g硫酸铜用于实验,是否合理,请说出理由 ;并在30℃的水浴中加热硫酸铜溶液一段时间,保证硫酸铜完全溶解,得到饱和溶液。
二、测量一定质量饱和硫酸铜溶液中硫酸铜的质量:
(2)在已配得的30℃时饱和溶液中,迅速取出饱和溶液50g,采用蒸发的方法求得硫酸铜的质量。从饱和溶液中析出蓝色晶体的化学式为(10) ,得到晶体后还要继续加热,直至固体颜色变为(11) 色为止。此操作过程中,用到的仪器除铁架台、酒精灯外,还需(12) 。
(3)最后称量得到固体质量为9.8g,经计算得到此时硫酸铜的溶解度为(13) g/100gH2O(精确到0.1g)。实验反思:实验数值比资料中的数据偏小,可能的原因是(14) (写出一条即可);
(4)测量50g饱和硫酸铜溶液中硫酸铜的质量,还可以使用重量法。
实验原理:CuSO4+BaCl2 →CuCl2+BaSO4↓
该实验方法中一定还要用到的实验操作是(15) (填写操作名称)。若最终得到硫酸钡14.5g,计算溶液中硫酸铜的质量为多少克?(提示:硫酸铜式量为160,硫酸钡式量为233。写出计算过程,精确到0.1g)
实验探究氢气遇到氧气发生爆炸的条件:
(1)甲装置中仪器“A”的名称是 ;在实验室中利用氯酸钾和二氧化锰制取氧气,发生的化学方程式是 ;利用锌粒和稀硫酸制取氢气,可以利用下列 (选填“甲”或“乙”)装置;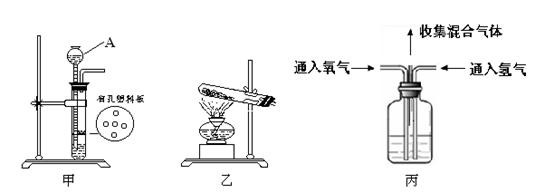
(2)利用丙装置将氢气、氧气混合气体收集起来,可以观察 数量,通过活塞控制两者气体的比例关系,利用一次性保鲜袋收集混合气体,然后直接点燃保鲜袋。
(3)实验共四次,实验数据及现象记录在下表:
| 实验次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 氢气与氧气的体积比 |
1︰2 |
1︰4 |
1︰19 |
1︰39 |
| 氢气的体积百分数 |
33% |
20% |
5% |
3.3% |
| 点燃后现象 |
爆炸 |
爆炸 |
爆炸 |
保鲜袋燃烧,没有爆炸 |
由此可见氢气与氧气混合发生爆炸,除要达到燃烧的三个条件外,还和 有关。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号