[北京]2013-2014学年北京市西城区高一上学期期末考试化学试卷
目前,很多自来水厂用氯气杀菌、消毒。下列关于氯气的性质描述正确的是
| A.无味 | B.无毒 | C.黄绿色 | D.不溶于水 |
当光束通过下列分散系时,可观察到丁达尔效应的是
| A.乙醇溶液 | B.氯化钠溶液 | C.硫酸铜溶液 | D.氢氧化铁胶体 |
在水溶液里或熔融状态下能导电的化合物是电解质。下列物质不属于电解质的是
| A.Fe | B.NaOH | C.H2SO4 | D.Na2SO4 |
下列物质与危险化学品标志的对应关系不正确的是
| A |
B |
C |
D |
| 乙醇 |
天然气 |
浓硫酸 |
氢氧化钠 |
 |
 |
 |
 |
合金具有许多优良的物理、化学或机械性能。下列物质属于合金的是
| A.水银 | B.不锈钢 | C.陶瓷 | D.玻璃 |
下列试剂可以用带磨口玻璃瓶塞的试剂瓶保存的是
| A.氢氟酸 | B.水玻璃 | C.氢氧化钠 | D.浓盐酸 |
下列物质中,既能与盐酸又能与氢氧化钠溶液反应,且有气体生成的是
| A.Si | B.SO2 | C.Al | D.Al2O3 |
下列变化中,需加入适当的氧化剂才能完成的是
| A.Fe → FeCl3 | B.CuO → Cu | C.HNO3 → NO | D.SO3 → H2SO4 |
某些补铁剂的成分中含有硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是
| A.稀盐酸 | B.KSCN溶液 | C.氯水 | D.铁粉 |
下列有关氧化还原反应的叙述中,正确的是
| A.一定有氧气参加 | B.还原剂本身被还原 |
| C.氧化反应先于还原反应发生 | D.一定有电子转移(得失或偏移) |
下列电离方程式书写不正确的是
| A.CuCl2== Cu2+ +2Cl- | B.Ba(OH)2="=" Ba2++(OH)2- |
| C.Al2(SO4)3="=" 2A13++3SO42- | D.HNO3="=" H++NO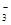 |
下列图示的四种实验操作是常用的分离提纯的方法,其名称从左到右依次是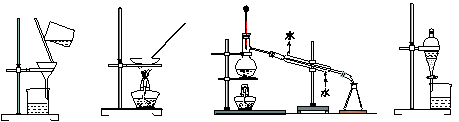
| A.蒸发、蒸馏、过滤、萃取 |
| B.过滤、蒸馏、蒸发、萃取 |
| C.过滤、蒸发、蒸馏、分液 |
| D.萃取、蒸馏、蒸发、过滤 |
下列变化不属于氧化还原反应的是
| A.加热氢氧化铁固体 | B.金属钠露置于空气中 |
| C.铜丝放入浓硫酸中并加热 | D.将氯气通入冷的消石灰浊液中 |
下列关于SO2性质的说法中,不正确的是
| A.能使品红溶液褪色 | B.能与水反应生成硫酸 |
| C.能与NaOH溶液反应 | D.能使酸性KMnO4溶液褪色 |
下列有关硅及其化合物用途的说法中,不正确的是
| A.硅单质是制造光电池的主要原料 | B.二氧化硅是制造光导纤维的材料 |
| C.可用石英坩埚加热氢氧化钠固体 | D.玻璃、水泥、陶瓷都是硅酸盐产品 |
下列化学反应中,能用离子方程式 H+ + OH-== H2O 表示的是
A.2H2 + O2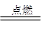 2H2O 2H2O |
| B.HCl + NaOH == NaCl + H2O |
| C.2HCl + Cu(OH)2== CuCl2 + 2H2O |
| D.Ba(OH)2 + H2SO4== BaSO4↓+ 2H2O |
已知某溶液中存在较多的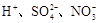 ,该溶液中还可能大量存在的离子组是
,该溶液中还可能大量存在的离子组是
A.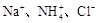 |
B.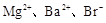 |
| C.Mg2+、Cl-、Fe2+ | D.K+、SiO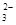 、Cl- 、Cl- |
下列除杂过程中,所选用的试剂或方法不正确的是
| A.NaCl固体中有NH4Cl固体:加热 |
| B.自来水中含有Cl-等可溶性杂质:蒸馏 |
| C.Na2CO3固体中有少量NaHCO3固体:加热 |
| D.CO2气体中混有SO2气体:将混合气体通过盛有NaOH溶液的洗气瓶 |
下列化学反应的离子方程式书写正确的是
| A.氯气通入氯化亚铁溶液中:Fe2++Cl2="=" 2Cl-+Fe3+ |
| B.氯气与氢氧化钠溶液反应:Cl2 + 2OH-="=" Cl-+ ClO- + H2O |
C.大理石与稀盐酸反应:CO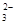 + 2H+== CO2 ↑ + H2O + 2H+== CO2 ↑ + H2O |
D.铜与稀硝酸反应:Cu + H+ + NO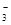 == Cu2+ + NO↑ + H2O == Cu2+ + NO↑ + H2O |
下列关于钠及其化合物性质的叙述,正确的是
| A.钠能与硫酸铜稀溶液反应,置换出红色的铜 |
| B.氧化钠和过氧化钠都能与水反应,生成物完全相同 |
| C.过氧化钠是淡黄色固体,可用作呼吸面具的氧气来源 |
| D.质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,产生气体的质量相同 |
若NA表示阿伏加德罗常数,下列说法正确的是
| A.1 mol Na2O2与水反应时,转移电子的数目为2 NA |
| B.标准状况下,22.4 L水中含有水分子的数目为NA |
| C.14 g N2中含有电子的数目为7 NA |
| D.数目为NA的一氧化碳分子和0.5 mol甲烷的质量比为7︰4 |
将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的 和
和 浓度相等。则已反应的
浓度相等。则已反应的 和未反应的
和未反应的 的物质的量之比是
的物质的量之比是
| A.2︰3 | B.3︰2 | C.1︰2 | D.1︰1 |
木炭与浓硫酸反应可表示为:C +2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)该反应的反应物和生成物中,属于氧化物的是 。
(2)木炭作 (填“氧化剂”或“还原剂”),硫酸 (填“被氧化”或“被还原”)。
(3)若消耗了2mol H2SO4,则生成 mol SO2。
部分金属可以与水在一定条件下发生反应。
(1)将一小块金属钠投入盛有水的烧杯中,待完全反应后,向其中滴加酚酞溶液。①钠与水反应的化学方程式是 。
②上述实验过程中,可观察到的实验现象有 (填选项序号),
产生现象b的原因是 。
a.钠浮在水面 b.钠熔成小球
c.钠球在水面上四处游动,发出嘶嘶声,逐渐消失
d.反应后向烧杯中滴加酚酞溶液,溶液呈红色
(2)铁粉可以与水蒸气在高温下反应,生成 (填化学式)和氢气。
氨气具有广泛的用途。
(1)工业上合成氨反应的化学方程式是 。
(2)实验室常用如下图所示装置制取并收集氨气。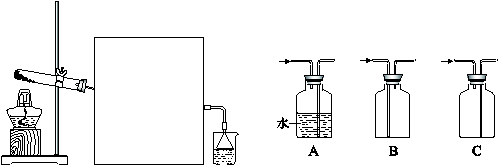
①实验室制取氨气反应的化学方程式是 。
②图中方框内收集氨气的装置可选用 (填字母序号)。
③尾气处理装置中使用倒扣漏斗的作用是 。
(3)工业上用NH3制取NO反应的化学方程式是 。
为了检验市场上常见两种金属饮料瓶的主要成分,某小组取甲、乙两种饮料瓶,将其剪碎作为样品,分别按下述步骤进行实验:
I.取少量样品于试管中,加入盐酸,充分反应后过滤。
II.取少量滤液于试管中,向其中滴加氢氧化钠溶液。
步骤II的实验现象如下:
| 样品甲 |
生成白色沉淀,继续滴加氢氧化钠溶液,沉淀消失 |
| 样品乙 |
生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色 |
(1)样品甲中金属的主要成分是 ,生成白色沉淀反应的离子方程式是 。
(2)样品乙进行步骤I后所得滤液中一定含有的金属离子是 ,白色沉淀变为红褐色反应的化学方程式是 。
现有含有少量NaCl、Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。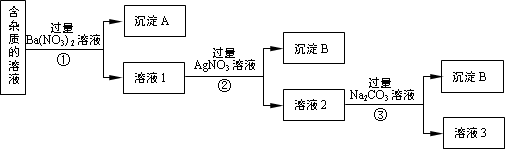
(1)沉淀A的主要成分是 、 (填化学式)。
(2)②中反应的离子方程式是 。
(3)①②③中均进行的分离操作是 。
(4)③中加入过量的Na2CO3溶液的目的是 。
(5)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是 ,为了除去杂质,可向溶液3中加入适量的 。
(6)实验室用上述实验获得的NaNO3固体配制500 mL 0.40 mol/L NaNO3溶液。
①配制溶液时,进行如下操作:a.定容;b.计算;c.溶解;d.摇匀;e.转移;f.洗涤;j.称量。称取NaNO3固体的质量是 g。按照操作顺序,第4步是 (填序号)。
②某同学转移溶液的操作如图所示,图中仪器的名称是烧杯和 ,该同学操作中的错误是 。
某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验。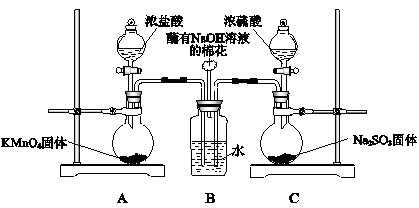
(1)装置A中的反应为2KMnO4+16HCl(浓) ="=" 2KCl+2MnCl2+5Cl2↑+8H2O,反应中的氧化剂是 ,生成71 g Cl2转移的电子是 mol。
装置C中生成SO2,反应的化学方程式是 。
(2)装置B中蘸有NaOH溶液的棉花的作用是 。
(3)打开A、C中分液漏斗的活塞,一段时间后关闭活塞。待反应完全后,小组同学又继续如下实验。
①甲同学取适量B中溶液于试管中,向其中滴加少量AgNO3溶液,有白色沉淀生成。甲同学由此认为SO2和Cl2发生了反应,理由是该反应中生成了 (填离子符号)。
②乙同学认为甲同学的结论不合理,认为A中生成的Cl2中混有杂质,应该在装置A、B间增加一个然后再按甲同学的方法即可得到正确结论。
乙同学认为Cl2中混有的杂质是 ,洗气瓶中盛有试剂的名称是 。
③ 丙同学则认为甲、乙两位同学的结论均不合理。丙同学取适量B中溶液于试管中,向其中滴加少量溶液X,有白色沉淀生成,则可得出结论,即SO2与Cl2同时通入水中,可以发生反应。溶液X是 (填选项序号)。
A.BaCl2溶液 B.Ba (OH)2溶液 C.Ba (NO3)2溶液 D.品红溶液
SO2与Cl2同时通入水中反应的化学方程式是 。
某小组用铜屑制取硫酸铜溶液。将铜屑放入一定浓度的硫酸中,加热并不断鼓入空气其反应原理为2Cu+O2+2H2SO4 2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
2CuSO4+2H2O。现欲将6.4 g铜完全溶解,加水后得200 mL溶液。计算:
(1)参加反应的氧气在标准状况下的体积是 。
(2)所得硫酸铜溶液的物质的量浓度是 。
(3)取100 mL上述硫酸铜溶液,加水稀释至0.1 mol/L,稀释后硫酸铜溶液的体积是 。
为探究某抗酸药X的组成,进行如下实验:
查阅资料:
①抗酸药X可能的组成可以表示为:MgmAln(OH)p(CO3)q(SiO3)r(m、n、p、q、r为≥0的整数)。
② 在pH=5.0时沉淀完全;
在pH=5.0时沉淀完全; 在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
在pH=8.8时开始沉淀,pH=11.4时沉淀完全。
实验过程:
| 步骤 |
实验操作 |
实验现象 |
| I |
向X的粉末中加入过量盐酸 |
产生气体A,得到无色溶液 |
| II |
向Ⅰ所得的溶液中滴加氨水,调节pH至5~ 6,过滤 |
生成白色沉淀B |
| III |
向沉淀B中加过量NaOH溶液 |
沉淀全部溶解 |
| IV |
向II得到的滤液中滴加NaOH溶液,调节pH至12 |
生成白色沉淀C |
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是 。
(2)II中生成B反应的离子方程式是 。
(3)III中B溶解反应的离子方程式是 。
(4)沉淀C的化学式是 。
(5)若上述n(A)︰n(B)︰n(C)=1︰2︰3,则X的化学式是 。
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。
可选药品:稀硝酸、浓硝酸、浓硫酸、NaOH溶液、蒸馏水
查阅资料:
A.浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
B.氢氧化钠溶液不与NO反应,能与NO2反应2NO2 + 2NaOH = NaNO3 + NaNO2 +H2O
| 实验过程 |
实验现象 |
| I.检验装置的气密性 |
|
| II.…… |
|
| III.打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 |
①中产生大量的红棕色气体,红棕色气体在②中变为无色,气体通过③后依然为无色,通过④后变为红棕色 |
(1)①中发生反应的离子方程式是 。
(2)②中发生反应的化学方程式是 。
(3)装置②~⑤中盛放的药品分别是② 、③ 、④ 、⑤ 。
(4)II的操作是 ,目的是 。
(5)该同学得出结论所依据的实验现象是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号