[河南]2014届河南省许昌平顶山新乡三市高三第一次调研理综化学试卷
下列有关物质性质的应用不正确的是
| A.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| B.浓硫酸具有强氧化性,不能用浓硫酸干燥SO2 |
| C.熟石灰具有碱性,可用来改良酸性土壤 |
| D.铝热反应能放出大量的热,常用于焊接钢轨 |
下列叙述中,错误的是
| A.乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
| B.分子式为C5H12的烃有三种可能的结构 |
| C.苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
| D.淀粉、纤维素和蛋白质都是高分子化合物,它们在一定条件下都能水解 |
W、X、Y、Z四种元素均为短周期元素且原子序数依次增大,其简单离子都能促进水的电离的是
| A.W2-、X+ | B.X+、Y3+ | C.X+、Z2- | D.Y3+、Z2- |
某有机物的结构如图,下列有关说法不正确的是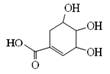
A.分子中C、H、O原子个数比为7∶6∶5
B.分子中不只含有两种官能团
C.可发生加成和取代反应
D.在水溶液中羧基容易电离出氢离子而羟基不能
下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是
| 选项 |
X |
Y |
| A |
MgSO4 |
CuSO4 |
| B |
AgNO3 |
Pb(NO3)2 |
| C |
FeSO4 |
Al2 (SO4)3 |
| D |
CuSO4 |
AgNO3 |
已知CO(g)+H2O(g) H2(g)+CO2(g)△H<0,若其他条件不变,以下说法中正确的是
H2(g)+CO2(g)△H<0,若其他条件不变,以下说法中正确的是
| A.加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B.升高温度,反应速率加快,反应放出的热量不变 |
| C.改变压强,平衡不发生移动,反应放出的热量不变 |
| D.若在原电池中进行,反应放出的热量不变 |
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度(纵坐标)和加入铁粉的物质的量(横坐标)之间的关系如图所示,则原溶液中Fe(NO3)3、 Cu(NO3)2、HNO3物质的量浓度之比为
| A.1∶1∶1 | B.3∶3∶8 | C.1∶3∶1 | D.1∶1∶4 |
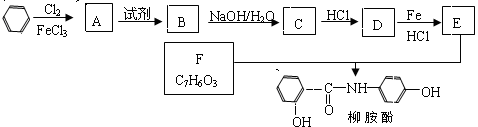
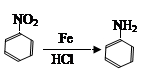
下图是一些重要工业生产的转化关系(反应条件略去):
请完成下列问题:
(1)若D是单质,且与A属于同一主族,反应在高温下进行,则:
①此反应的化学方程式是 。
②D单质的一种重要用途是 。
(2)若B为黄色固体,D为固体化合物,则该反应为4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
①当有1molC生成时,该反应转移电子的总数是 。
②将C通入足量的酸性KMnO4溶液中,发生反应的离子方程式为 。
(3)若B是一种碱性气体,D为化合物,则:
①该反应的化学方程式是 。
②B在加热条件下与CuO反应有Cu生成,该反应的化学方程式为 ;有人提出产物Cu中可能还含有Cu2O。已知Cu+在酸性溶液中不能稳定存在,为验证Cu2O是否存在,可取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,则证明含有Cu2O。请写出发生反应的化学方程式:_________。
Ⅰ.甲醇是一种新型的能源。
(1)合成气(组成为H2和CO)是生产甲醇的重要原料,请写出由焦炭和水在高温下制取合成气的化学方程式 。
(2)已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ;
(3)在容积为l L的密闭容器中,由CO和H2合成甲醇。在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);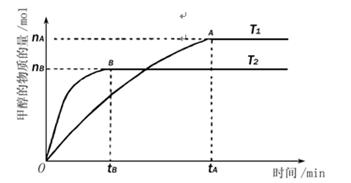
下列说法正确的是 (填序号)
A.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=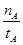 (mol·L-1·min-1) (mol·L-1·min-1) |
| B.该反应在T1时的平衡常数比T2时的大 |
| C.该反应为吸热反应 |
D.处于A点的反应体系从T1变到T2,达到平衡时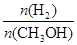 减小 减小 |
(4)在T1温度时,将1 mol CO和2mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO转化率为a,则容器内的压强与起始压强之比为 ;
(5)在直接以甲醇为燃料的电池中,电解质溶液为碱性,负极的反应式为 ;假设原电解质为NaOH,且电池工作一段时间后溶质只有Na2CO3,此时溶液中各离子浓度大小关系为
Ⅱ.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9×10-11。某溶液中含有C1-, Br-和CrO42-,浓度均为0.010mo1·L-1,向该溶液中逐滴加入0.010mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为 。
测定有机物中碳和氢等元素的含量,最常用的方法是燃烧分析法。即把已知量的样品置于氧气流中,用氧化铜作催化剂,在760℃左右,样品全部被氧化为二氧化碳和水。实验装置如下图所示: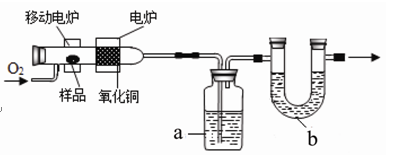
(1)实验时,装置a、b中通常装入的物质分别是 、 。
(2)开始加热之前,要通一段时间的氧气,目的是 ;停止加热后,也要通一段时间的氧气,目的是 。
(3)某次实验中,取用样品烃的含氧衍生物A的质量为2.3g,经测定a装置增重2.7g,b装置增重4.4g。请推算出A物质的实验式: (要求写出计算过程)
(4)经进一步测定得知A的相对分子质量为46,则A的分子式为 。
(5)实验发现A物质遇金属钠可以放出氢气,则A物质中具有的官能团为 。同样取2.3g的A,与足量的钠反应,用如图所示装置量取放出的氢气。量取气体时操作水准管的注意事项为 。将量取的气体换算成标准状况体积为cmL,则一个A分子中有 个氢原子被置换了(用含c的表达式表示)。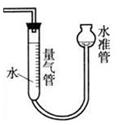
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下: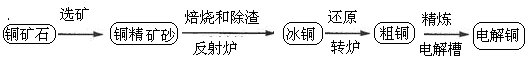
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转化为低价氧化物。该过程中两个主要反应的化学方程式是 、 ,反射炉内生成炉渣的主要成分是 ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式是 、 ;
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板是图中电极 (填图中的字母);在电极d上发生的电极反应式为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为 。
前四周期原子序数依次增大的元素A,B,C,D中, A是电负性最大的元素,并且A-和B+的电子数相差为8;C和D原子序数相差为2,且都与B位于同一周期,C元素的次外层电子数是最外层电子数的7倍。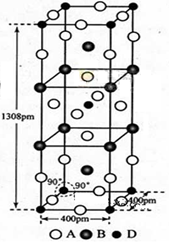
回答下列问题:
(1)D的价层电子排布式为_______。
(2)请用电子式表示A、B两元素形成化合物的过程。 。
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________;D的配位数为_______;
②列式计算该晶体的密度___ ____g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_ ____;该化合物中存在一个复杂离子,该离子的化学式为___ ____,配位数是_ __。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号