[北京]2013届北京市丰台区第一次模拟理综化学试题试卷
下列说法不正确的是
| A.用电解法精炼粗铜的时候纯铜做阳极 |
| B.将镁块与钢铁输水管相连,可以防止钢铁腐蚀 |
| C.熔融烧碱的时候,不能使用石英坩埚 |
| D.可以用硫酸或者CO2中和碱性废水 |
下列化学反应得出的结论不正确的是
| |
化学反应 |
结 论 |
| A |
2Na + 2H2 O=2NaOH + H2↑ 4Na + O2= 2Na2O |
Na应隔绝空气,密封保存 |
| B |
CO32- + 2H+=CO2 ↑+ H2O |
遇强酸产生大量CO2的溶液中一定含有大量CO32- |
| C |
Al2O3+ 6H+=2Al3+ + 3H2O Al2O3+ 2OH-=2AlO2-+ H2O |
Al2O3是两性氧化物 |
| D |
CO2(少量) +H2O+ C6H5O-→HCO3-+C6H5OH |
相同温度时,电离出H+的能力: H2CO3 > C6H5OH> HCO3- |
下列说法正确的是
| A.1mol葡萄糖可与5mol乙醇发生酯化反应 |
| B.油脂氢化、氨基酸形成多肽、蛋白质水解都属于取代反应 |
| C.可用碘水和银氨溶液鉴别葡萄糖、麦芽糖和淀粉三种物质 |
D.乙二醇、甲醛、α-羟基丙酸(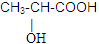 )都可发生缩聚反应 )都可发生缩聚反应 |
已知:氢氧化镁能溶于浓度均为3mol/L的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是
| A.c(NH4+):③ > ② |
| B.pH:① > ② > ③ |
C.Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s) Mg2+ (aq) + 2OH- (aq)向溶解方向移动 Mg2+ (aq) + 2OH- (aq)向溶解方向移动 |
| D.将等体积的①和③混合,所得溶液中c(Cl-) >c(NH4+) > c(H+) > c(CH3COO-) > c(OH-) |
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液下列说法不正确的是
| A.K+移向催化剂b |
| B.催化剂a表面发生的化学反应:Fe(CN)64--e- = Fe(CN)63- |
| C.Fe(CN)63-在催化剂b表面被氧化 |
| D.电解池溶液中的Fe(CN)64-和Fe(CN)63-浓度基本保持不变 |
某同学对Na2O2和CO2反应后的所得固体进行研究,下列实验方案中不能测得固体中Na2CO3的质量分数的是
| A.取a克混合物与足量的稀盐酸充分反应,将反应后的固体加热蒸干、灼烧得到b克固体 |
| B.取a克混合物与足量的稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| C.取a克混合物与足量的BaCl2溶液充分反应,过滤、洗涤、烘干得到b克固体 |
| D.取a克混合物与足量的水反应,加热,使气体完全逸出,冷却至室温测得气体体积为VL(标况) |
已知:(CH3COOH) 2(g) 2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
2CH3COOH(g)经试验测得在不同压强下体系的平均相对分子质量(M)随温度T的变化曲线如图所示,下列说法正确的是
| A.该过程的△H<0 |
| B.平衡常数: K(a)=K(b)<K(c) |
| C.气体压强:P(a)<P(b)= P(c) |
| D.当M=80时,(CH3COOH) 2和CH3COOH的物质的量之比为1:1 |
直接排放氮氧化物会形成酸雨、雾霾,催化还原法和氧化吸收法师常用的处理方法。
(1)用化学方程式表示NO2形成酸雨的过程____________________________
(2)利用NH3和CH4等气体除去烟气中的氮氧化物。
①NH3的电子式
②热稳定性 NH3 CH4(填“>”=“<”)
③已知:CH4(g)+2O2(g)=CO2(g)+2H20(l) △H1=akJ/mol; 欲计算反应CH4(g)+4NO(g)=CO2(g)+2H20(l)+2N2(g)的焓变 △H2则还需要查询某反应的焓变△H3,当反应中各物质的化学计量数之比为最简整数比时,△H3=bkJ/mol,该反应的热化学方程式是__________________________据此计算出△H2= kJ/mol (用含a、b的式子表示)。
(3)利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.写出氧化吸收法除去氮氧化物的化学方程式______________________________________现有标况下的O233.6ml,理论上可以处理该氮氧化物______ml(标准状况下)。
用芒硝(Na2SO4 °10H2O)制备纯碱、明矾铵[(NH4)2Al(SO4)2°12H2O]的生产工艺流程如下图:
(1)溶液C中的溶质主要是_____________
(2)明矾铵的溶液呈_____性,明矾铵可用于净水,用离子方程式说明其原理______________________
(3)过程Ⅰ中的反应温度不能超过40℃,其原因是______________________________
(4)运用化学平衡原理解释Na2SO4稍过量的原因
(5)若将Al2(SO4)3加入到A中会产生大量的沉淀和气体,导致明矾铵的产量降低,请用离子方程式解释产生该现象的原因是___________________________________________
(6)溶液E中的溶质离子为__________________
(7)已知明矾铵的溶解度随着温度的升高而增大,过程Ⅱ中得到明矾铵的系列实验操作是: 、 、过滤、洗涤、干燥。
为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)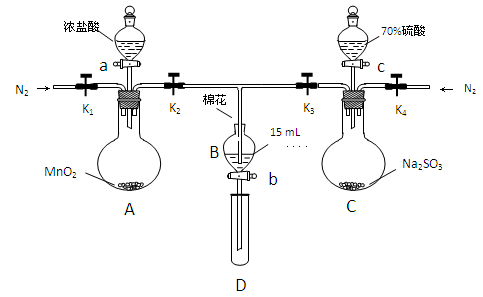
实验过程:
Ⅰ.打开弹簧夹K1-K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,单后关闭K1、K2、K3 .
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅵ,检验B溶液中的离子.
(1)过程Ⅰ的目的是___________________________
(2)棉花中浸润的溶液为_______________________
(3)A中发生反应的化学方程式为_____________________________________________
(4)用70%的硫酸支取SO2,反应速率比用98%的硫酸块,原因是___________________
(5)过程Ⅳ中检验B溶液中是否含有硫酸根的操作是______________________________
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化Cl2>Fe3+>SO2的是
| |
过程Ⅳ B溶液中含有的离子 |
过程Ⅵ B溶液中含有的离子 |
| 甲 |
有Fe3+无Fe2+ |
有SO42- |
| 乙 |
既有Fe3+又有Fe2+ |
有SO42- |
| 丙 |
有Fe3+无Fe2+ |
有Fe2+ |
(7)进行实验过程Ⅴ时,B中的溶液颜色由黄色变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。
查阅资料:Fe2+(aq)+SO32-(aq) 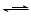 FeSO3(s)
FeSO3(s)
提出假设:FeCl3和SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合颜色。
某同学设计如下实验,正式该假设的成立: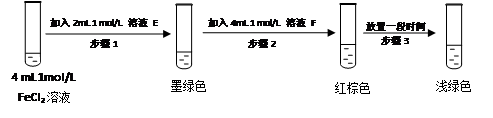
溶液E和F分别是___________、_______________
请用化学平衡原理解释步骤3红棕色溶液变为浅绿色的原因___________________________
共聚法可改进有机高分子化合物的性质,高分子聚合物P的合成路线如下:
(1)A的结构简式为________________
(2)C的名称为
(3)I由F经①~③合成,F可以使溴水褪色.
a.①的化学方程式是
b.②的反应试剂是
c.③的反应类型是
(4)下列说法正确的是
a.C可与水任意比例混合
b.A与1,3-丁二烯互为同系物
c.由I生成M时,1mol最多消耗3molNaOH
d.N不存在顺反异构体
(5)高聚物P的亲水性,比由E形成的聚合物__________(填“强、弱”).
(6)E与N按照物质的量之比为1:1发生共聚生成P,P的结构简式为
(7)E有多重同分异构体,符合下列条件的异构体由 种(不考虑顺反异构),写出其中的一种
a.分子中只含一种环状结构
b.苯环上有两个取代基
c.1mol该有机物与溴水反应时能消耗4molBr2
 粤公网安备 44130202000953号
粤公网安备 44130202000953号