[江苏]2013届江苏省扬州、南通、泰州、宿迁四市高三第二次调研测试化学试卷
今年两会期间,习近平勉励江苏代表为“让生态环境越来越好”做贡献。下列做法均正确的是
①合理开发利用可燃冰 ②全面关停化工企业
③研发易降解的生物农药 ④改进汽车尾气净化技术
| A.①②③ | B.①③④ | C.①②④ | D.②③④ |
下列有关化学用语表示正确的是
A.对硝基甲苯的结构简式: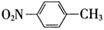 |
B.镁离子的结构示意图: |
C.次氯酸的电子式: |
D.亚硫酸钠水解的离子方程式: |
下列有关物质的性质与应用相对应的是
| A.NH3极易溶于水,可用作制冷剂 |
| B.A12O3熔点高,。可用作耐高温材料 |
| C.SO2具有氧化性,可用于漂白品红、织物等 |
| D.BaCO3能与盐酸反应,可用于治疗胃酸过多 |
在指定条件下,下列各组离子可能大量共存的是
A.无色澄清透明溶液中: |
B.与铝反应放出H2的溶液中: |
C.滴加酚酞显红色有溶液中: |
D.由水电离的 |
右下图为与水相关的部分转化关系(水作反应物或生成物,部分产物和反应条件未列出)。下列说法错误的是
| A.右图所示的反应均为氧化还原反应 |
| B.比较镁、铁与水的反应条件,可知铁的金属性比镁弱 |
| C.工业上常用NO2与水的反应原理制取硝酸 |
| D.实验室中可用铜与稀硝酸反应制取NO2 |
用下列实验装置进行相应实验.能达到实验目的的是
| A.用图1所示装置除去HCl气体中的少量C12 |
| B.用图2所示装置检验加热时产生的乙烯 |
| C.用图3所示装置在铁制品表面镀铜 |
| D.用图4所示装置分离溴的四氯化碳溶液 |
设NA为阿伏加德罗常数的值。下列叙述错误的是
| A.常温常压下,0.17g NH3中含有的共用电子对数为0.1NA |
| B.常温常压下,1 L pH=1的稀H2SO4中含有的氢离子数为0.1NA |
| C.标准状况下,2.24 L C12与足量稀NaOH反应转移电子数为0.1NA |
| D.10 g由CaCO3与KHCO3组成的混合物中含有的碳原子数为0.1NA |
下列有关说法正确的是
| A.催化剂通过降低化学反应的焓变加快化学反应速率 |
| B.铅蓄电池充电时.标有“一”的电极应与电源的负极相连 |
| C.温度保持不变.向水中加入钠盐对水的电离一定没有影响 |
| D.向醋酸钠溶液中加水稀释时.溶液中所有离子浓度都减小 |
下列图示与对应的叙述相符的是
A.图I可表示N2+3H2 2NH3的速率时间图像,t1时刻改变的条件是升高温度 2NH3的速率时间图像,t1时刻改变的条件是升高温度 |
| B.图Ⅱ可表示用0.1 000 mol/L醋酸滴定40.00 mL0.1000 mol/LNaOH溶液得到的滴定曲线 |
| C.图Ⅲ可表示NO2平衡转化率与温度、压强的变化关系,由图可知:△H<0、P1<P2 |
| D.图Ⅳ可表示pH相同的NaOH溶液与氨水稀释过程的pH变化.其中曲线a对应氨水 |
甲酸香叶酯是一种食品香料.可以由香叶醇与甲酸发生酯化反应制得。
下列说法中正确的是
| A.香叶醇的分子式为CllHl8O |
| B.香叶醇在浓硫酸、加热条件下可发生消去反应 |
| C.1 mol甲酸香叶酯可以与2 molH2发生加成反应 |
| D.甲酸香叶酯分子中所有碳原子均可能共平面 |
短周期元素T、X、Y、Z的原子序数依次增大,T与Z属于同一主族,X、Y、Z最高价氧化物对应的水化物两两之间都能反应,且X、Y、Z原子最外层电子数之和等于X的原子序数。则下列说法正确的是
| A.简单离子半径大小顺序:rT>rX>rY |
| B.T与Z的最高正化合价相等 |
| C.室温下,单质Y不能与浓硫酸反应 |
| D.用电解法可制得T、X、Y的单质 |
常温下,向20.00 mL 0.100 mol/LCH3COONa溶液中逐滴加入0.1 000 mol/L盐酸,溶液的pH与所加盐酸体积的关系如右下图所示(不考虑挥发)。下列说法正确的是

T℃,向5.0 L恒容密闭容器中充入1.0 molSO3气体,发生反应:2SO3(g)  2SO2(g)+O2(g)
2SO2(g)+O2(g)
△H="+196" kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6 kJ的热量。当温度度不变时,改变某一条件,下列结论正确的是
工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:
有关氢氧化物开始沉淀和沉淀完全的pH如下表: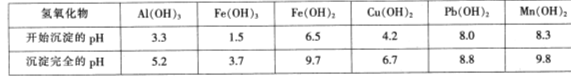
请问答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是 。
(2)酸浸后的溶液中含有Mn2+、 SO42-,另含有少量Fe2+、Fe3+.A13+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为 。
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是 。
③加入BaS,除去Cu2~、Pb2+后,再加入NaF溶液,除去 。
(3)从溶液A中回收的主要物质是 ,该物质常用作化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应韵化学方程式:
。
化合物F(匹伐他汀)用于高胆固醇血症的治疗,其合成路线如下: (1)化合物D中官能团的名称为 、 和酯基。
(1)化合物D中官能团的名称为 、 和酯基。
(2)A→B的反应类型是
(3)写出同时满足下列条件的A的一种同分异构体的结构简式:
I.分子中含有两个苯环;Ⅱ.分子中有3种不同化学环境的氢;Ⅲ.不含一O—O一。
(4)实现D→E的转化中,化合物X的分子式为C19H15NFBr,写出其结构简式: 。
(5)已知:化合物E在CF3COO H催化作用下先转化为 ,再转化为F。你认为合成路线中设计步骤②的目的是 .
,再转化为F。你认为合成路线中设计步骤②的目的是 .
(6)上述合成路线中,步骤③的产物除D外还生成 ,该反应原理在有机合成中具有广泛应用。试写出以
,该反应原理在有机合成中具有广泛应用。试写出以 为主要原料制备
为主要原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:CH3CH2OH CH2=CH2
CH2=CH2 CH3CH3
CH3CH3
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病,KI、K1O3曾先后用于加碘盐中。
(1)工业上可以通过铁屑法生产KI,其工艺流程如下: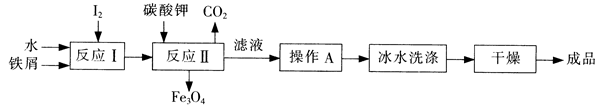
①反应I生成铁与碘的化合物,若该化合物中铁元素与碘元素的质量比为21:127,则加入足量碳酸钾时,反应Ⅱ的化学方程式为 。
②操作A包括 ;用冰水洗涤的目的是 。
(2)KIO3可以通过H2O2氧化I2先制得HIO3,然后再用KOH中和的方法进行生产。
①烹饪时,含KIO3的食盐常在出锅前加入,其原因是 ,
②若制得1284 kg KIO3固体,理论上至少需消耗质量分数为30%的双氧水 kg。
③KIO3还可通过下图所示原理进行制备。电解时总反应的离子方程式为 。若忽略溶液体积的变化,则电解结束后阴极区的pH与电解前相比 (选填“增大”、“减小”或“不变”)。
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等。过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量。 
(1)某研究小组拟用右图装置测定一定质量的样品中过氧化镁的含量。
①实验前需进行的操作是 .稀盐酸中加入少量FeCl3溶液的作用是 。
②用恒压分液漏斗的优点有:使分液漏斗中的溶液顺利滴下; 。
③实验终了时,待恢复至室温,先 ,再平视刻度线读数。
(2)实验室还可通过下列两种方案测定样品中过氧化镁的含量:
方案I:取a g样品,加入足量稀盐酸,充分反应后再加入 NaOH溶液至Mg2+沉淀完全,过滤、洗涤后,将滤渣充分灼烧,最终得到b g固体。
方案Ⅱ:称取0.1 g样品置于碘量瓶中,加入15 mL0.6 mol/LKI溶液和足量盐酸,摇匀后在暗处静置5 min,然后用0.1 mol/L Na2S2O3溶液滴定,滴定到终点时共消耗VmL Na2S2O3溶液。(已知:I2+2Na2S2O3= Na2S4O6+2NaI)
①已知常温下Ksp[Mg(OH)2]=l×10-11。为使方案I中Mg2+完全沉淀[即溶液中c(Mg2+)≤l ×10-5mol/L],溶液的pH至少应调至 。方案I中过氧化镁的质量分数为 (用含a、b的表达式表示)。
②方案Ⅱ中滴定前需加入少量 作指示剂;样品中过氧化镁的质量分数为 (用含V的表达式表示)。
在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应。
(1)若在恒温恒容的容器内进行反应C(s)+H2O(g) CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 。(填字母)
CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 。(填字母)
a.容器内的压强保持不变 b.容器中H2浓度与CO浓度相等
c.容器中混合气体的密度保持不变 d.CO的生成速率与H2的生成速率相等
(2)CO一空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2。该电池负极的电极反应式为 。
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g)  CH4(g)+ H2O (g)
CH4(g)+ H2O (g)
①一定条件下,该反应能够自发进行的原因是 。
②已知H2(g)、CO(g)和 CH4(g)的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1和890,0 kJ·mol-1。
写出CO与H2反应生成CH4和CO2的热化学方程式: 。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为: .
CH3OH(g)+CO(g) HCOOCH3(g) △H=-29.1 kJ·mol-1
HCOOCH3(g) △H=-29.1 kJ·mol-1
科研人员对该反应进行了研究.部分研究结果如下:
①从反应压强对甲醇转化率的影响“效率"看,工业制取甲酸甲酯应选择的压强是 。
②实际工业生产中采用的温度是80℃,其理由是 。
已知A、D、E、G、L、M是核电荷数依次增大的6种短周期主族元素,其中A的原子序数与周期序数相等,D、G、L、M基态原子的最外能层均有2个未成对电子。R+核外有28个电子。请回答下列问题:(答题时,A、D、E、G、L、M、R用所对应的元素符号表示)
(1)E、G、M的第一电离能由大到小的顺序为 。
(2)下图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价。基态R2+的核外电子排布式为 ;Q的化合价为 价。
(3)1 mol晶体L中含有δ键的数目为 。
(4)G与M可形成MG3与MG2,MG3分子的空间构型是 ,MG2中M原子的杂化方式是 。
(5)在(EA4)2R(MG4)2中存在的化学键除极性键外,还有 (填字母)。
a.离子键 b. 氢键 c.配位键 d.金属键
三苯甲醇是一种重要有机合成中间体,可以通过下列原理进行合成: 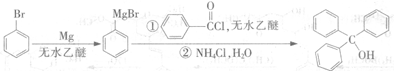
实验步骤如下:
①如图1所示,在三颈烧瓶中加入A,1.5 g镁屑,在滴液漏斗中加入,6.7 mL溴苯和无水乙醚,先加人1/3混合液于烧瓶中,待镁屑表面有气泡产生时,开始搅拌,并逐滴加入余下的混合液,使反应液保持微沸状态,至反应完全。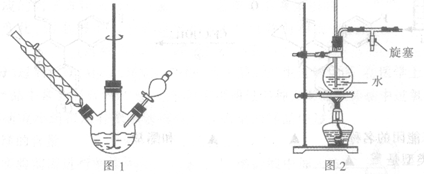
②继续加,A,3.7 g苯甲酰氯和无水乙醚,水浴回流l h 后,在冷水浴下慢慢滴加氯化铵的饱和溶液30.0 mL。
③将三颈烧瓶内的物质水浴加热蒸去乙醚,然后加,A,30.0 mL水进行水蒸气蒸馏(图2用作水蒸气发生装置),直至无油状物蒸出。
④冷却抽滤,将固体用80.0%的乙醇溶液重结晶,最终得到产品。
(1)步骤①中“逐滴加入余下的混合液”是为了防止 。
(2)若水蒸气蒸馏装置中出现堵塞现象,则图2玻璃管中水位会突然升高,此时应 ,待故障排除后再进行蒸馏。
(3)抽滤用到的主要仪器有气泵、 ,抽滤优于普通过滤的显著特点是 。
(4)步骤④中用80.0%的乙醇溶液重结晶的目的是 。
(5)用光谱法可检验所得产物是否纯净,其中用来获得分子中含有何种化学键和官能团信息的方法 。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号