[安徽]2013届安徽省合肥市高三第三次教学质量检测理综化学试卷
毒品可卡因又称古柯碱(分子结构如下图所示),是一种具有局部麻醉作用的天然生物碱,因其毒性大且易成瘾,现已被其他麻药所替代。下面有关叙述正确的是
| A.古柯碱是高分子化合物 |
| B.古柯碱分子结构中不存在非极性键 |
| C.古柯碱难溶于水和盐酸 |
| D.0. 01mol古柯碱分子中含甲基约1.204×1022个 |
下列离子在溶液中能大量共存,通入SO2气体后仍能大量共存的一组是
| A.NH4+、I-、Cl-、Ca2+ | B.K+、Na+、ClO-、SO42- |
| C.Fe3+、Na+、Cl-、SCN- | D.K+、Al3+、NO3-、AlO2- |
下列实验能够达到预期目的的是
| A.①可用于表示:0.1mol·L-1的NaOH溶液滴定盐酸的滴定曲线 |
| B.②可用于证明:氧化性 Cl2>Br2>I2 |
| C.③可用于证明:Ksp(AgCl)>Ksp(AgBr)>Ksp(Ag2S) |
| D.④可用于证明:非金属性 Cl>C>Si |
汽车尾气净化中的一个反应如下:2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-373.4kJ/mol
N2(g)+2CO2(g) △H=-373.4kJ/mol
反应达到平衡后,改变某一个条件,下列示意图曲线①〜⑧中正确的是
| A.①⑥⑧ | B.①⑤⑦ | C.②③④ | D.③⑥⑦ |
工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是
| A.阴极材料可以是Fe,含氧酸根杂质不参与电极上放电 |
| B.该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑ |
| C.通电后,该电解槽阴极附近溶液pH会减小 |
| D.除去杂质后氢氧化钾溶液从出口B导出 |
已知磷酸分子结构 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。由此可推断出H3PO2的分子结构是
某酸HX稀溶液和某碱YOH稀溶液的物质的量浓度相等,两溶液混合后,下表各组关系可能合理的是
| 编号 |
HX |
YOH |
溶液体积 |
粒子浓度 |
| ① |
强酸 |
强碱 |
V(HX)=" V" (YOH) |
c(HX) + c(X-) = c(Y+) |
| ② |
弱酸 |
弱碱 |
V(HX)<V(YOH) |
c(X-) < c(Y+) |
| ③ |
强酸 |
强碱 |
V(HX)= V(YOH) |
c(H+)>c(YOH) + c(OH-) |
| ④ |
弱酸 |
弱碱 |
V(HX)>V(YOH) |
c(Y+) + c(H+) = c(X-) + c(OH-) |
A.①② B.②③ C.②④ D.③④
X、Y、Z、T、W五种元素的性质或原子结构如下表:
| 元素 |
元素性质或原子结构 |
| X |
原子的最外层电子数是次外层电子数的2倍 |
| Y |
常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z |
基态原子最外层电子排布式为(n+1)sn(n+1)pn+2 |
| T |
与Z同周期,元素最高价是+7价 |
| W |
原子序数为Y、T元素之和,不锈钢中含有该元素 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_______;W元素基态原子电子排布式为________________________。
(2)元素Z与元素T相比,非金属性较强的是_______(用元素符号表示),下列表述中能证明这一事实的是______________。
A.常温下Z的单质和T的单质状态不同
B.T的氢化物比Z的氢化物稳定
C.一定条件下Z和T的单质都能与氢氧化钠溶液反应
D.T的电负性比Z大
(3)常见溶剂XZ2的分子中,含有的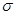 键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
键与π键个数比为_______,它所形成的晶体类型为_______;Y的常见氢化物易液化的主要原因是______________
(4)①自然界常见的X元素含氧酸的钙盐和适量T的氢化物溶液反应时,每产生4. 4g 气体(不考虑气体溶解)放热a kJ,则该反应的热化学方程式为______________。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得PH变化曲线如下图所示: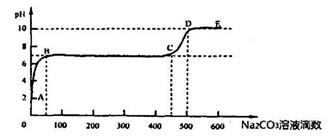
请用离子方程式表示BC段、CD段发生的反应:
BC段:__________________________________________;
CD段:__________________________________________。
某有机物G分子结构的球棍模型如下图所示(图中小球分别表示碳、氢、氧原子,球与球之间的连线“一”不一定是单键)。用芳香烃A为原料合成G的路线如下:
试回答:
(1)G的分子式为_______;G中环状基团被氢原子取代后的有机物名称为_______。
(2)A的结构简式为______;D中官能团的名称为_______。
(3)B→C反应的化学方程式是____________________________;
E→F反应的化学方程式是____________________________。
(4)E的同分异构体中可用通式 表示(其中X、Y均不为H),且能发生银镜反应的物质有_______种,其中核磁共振氢谱有6个峰的物质结构简式为 (写出一种即可) ________________。
表示(其中X、Y均不为H),且能发生银镜反应的物质有_______种,其中核磁共振氢谱有6个峰的物质结构简式为 (写出一种即可) ________________。
利用酸解法制钛白粉产生的废液[含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4 ],生产硫酸亚铁和补血剂乳酸亚铁。其生产步骤如下:
请回答:
(1)步骤①中分离操作的名称是_______;步骤⑥必须控制一定的真空度,原因是______________
(2)废液中的TiOSO4在步骤①能水解生成滤渣(主要成分为TiO2•xH2O)的化学方程式为_________
_ ;步骤④的离子方程式为____________________________________。
(3)用平衡移动原理解释步骤⑤中加乳酸能得到乳酸亚铁的原因______________________________。
(4)配平酸性高锰酸钾溶液与硫酸亚铁溶液反应的离子方程式:
_____ Fe2+ + _____ MnO4- + _____ H+ = _____Fe3+ +_____ Mn2+ +_____
取步骤②所得晶体样品a g,溶于稀硫酸配成100.00 mL溶液,取出20. 00 mL溶液,用KMnO4溶液滴定(杂质与KMnO4不反应)。若消耗0.1000 mol·L-1 KMnO4溶液20.00mL,则所得晶体中FeSO4• 7H2O的质量分数为(以含a的式子表示) _____________________。
向溴水中加入足量乙醛溶液,可以看到溴水褪色。据此对溴水与乙醛发生的有机反应类型进行如下探究,请你完成下列填空:
I.猜测:
(1)溴水与乙醛发生取代反应;
(2)溴水与乙醛发生加成反应;
(3)溴水与乙醛发生_______反应。
II.设计方案并论证:
为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:
方案l:检验褪色后溶液的酸碱性。
方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-离子的物质的量。
(1)方案1是否可行? _______,理由是__________________________________________
(2)假设测得反应前用于溴水制备的Br2的物质的量为a mol 。
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生加成反应;;
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生取代反应;
若测得反应后n(Br-) = _______mol,则说明猜测(3)正确。
III.实验验证:某同学在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀l.88 g(已知反应生成有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为__________________________________________。
IV.拓展
请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。
| 实验操作步骤 |
实验现象 |
结论 |
| |
|
|
 粤公网安备 44130202000953号
粤公网安备 44130202000953号