[广东]2012-2013学年广东省郁南县第一学期期末检测化学试卷
诗词是民族灿烂文化中的瑰宝。下列诗句中隐含有化学变化的是
| A.千里冰封,万里雪飘 | B.只要功夫深,铁柱磨成针 |
| C.野火烧不尽,春风吹又生 | D.夜来风雨声,花落知多少 |
把一根火柴梗平放在蜡烛火焰中,约1s后取出,可观察到火柴梗
| A.放置在外焰部分被烧黑最重 | B.均匀地被烧黑 |
| C.放置在内馅部分被烧黑最重 | D.放置在焰心部分被烧黑最重 |
实验是科学探究的重要手段,下列化学实验操作正确的是 
| A.滴加液体 | B.加热液体 | C.固体粉末取用 | D.倾注液体 |
化学与人体健康密切相关。市场上有“高钙牛奶”、“含氟牙膏”、“葡萄糖酸锌口服液”等商品,这里的“钙、氟、锌”应理解为
| A.原子 | B.元素 | C.分子 | D.单质 |
据火星探测器发回的数据分析,火星大气中95%是二氧化碳,其余为少量的氮气、氢气,还找到了有液态水存在的证据。根据以上信息,某同学做出如下推断:①火星大气是混合物②火星大气与地球大气成分相似③火星环境适宜人类生存④火星上温室效应更显著。你认为正确的是
| A.①④ | B.②③ | C.②④ | D.③④ |
已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则该原子核外电子数为
| A.2 | B.6 | C.8 | D.14 |
下列关于右图所示实验的说法中,正确的是
| A.该反应为化合反应 |
| B.试管1中的气体是氢气 |
| C.试管1和试管2中气体体积比为1:2 |
| D.该实验证明水是由氢气和氧气组成的 |
甲醛(CH2O)是室内污染的主要成分之一,它来源于室内装修所用的油漆、胶合板等材料。下列关于甲醛的说法错误的是
A、甲醛是由C、H、O三种元素组成 B、甲醛分子中C、H、O原子个数比是1:2:1
C、一个甲醛分子含有四个原子 D、甲醛分子是由一个碳原子和一个水分子构成
绿色化学又称环境友好化学,它的特点之一是:提高原子的利用率,使原料中所有的原子全部转化到产品中,实现“零排放”。下列反应符合绿色化学这一特点的是
| A.工业制取生石灰CaCO3高温 CaO+CO2↑ | B.实验室制取氢气Zn+H2SO4=ZnSO4+H2↑ |
| C.制熟石灰CaO+H2O=Ca(OH)2 | D.工业炼铁:Fe2O3+3CO高温 2Fe+3CO2 |
学习化学要善于从化学的视角认识世界。对下列事实的认识你认为错误的是
| 选项 |
事实 |
认识 |
| A |
水蒸发变成水蒸气 |
分子大小发生改变 |
| B |
50L水和50L酒精混合后的体积小于100L |
分子之间有间隔 |
| C |
墙内开花墙外香 |
分子在不断运动 |
| D |
N2的化学性质不活泼,O2的化学性质比较活泼 |
不同分子性质不同 |
下图表示治理汽车尾气所涉及反应的微观过程。下列说法错误的是
| A.图中单质的化学式为N2 | B.该反应使有毒气体转化为无毒气体 |
| C.反应物都属于氧化物 | D.反应中原子、分子个数都不变 |
下列各组物质,按单质、化合物、混合物顺序排列正确的是
| A.空气、氮气、稀有气体 | B.铁、氧化铁、铁矿石 |
| C.生石灰、熟石灰、石灰石 | D.氧气、一氧化碳、二氧化碳 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 |
X |
Y |
Z |
Q |
| 反应前质量/g |
2 |
2 |
84 |
5 |
| 反应后质量/g |
待测 |
24 |
0 |
14 |
下列推断正确的是
A、该反应是分解反应 B、反应后生成24gY
C、反应后X的质量为53g D、反应中X与Q发生改变的质量之比为55:14
实验桌上放着三瓶没有标签的CO、O2、CO2气体,鉴别它们最简便的方法是
| A.测定它们是否有毒 | B.闻气味 |
| C.用澄清的石灰水 | D.用一根燃着的木条 |
(5分)用化学符号填写下列空白:
(1)2个氢原子 ;
(2)地壳中含量最高的金属元素 ;
(3)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图。该元素的原子的核电荷数为 ,相对原子质量为 。图乙所示粒子的符号为 。
(5分)“化学就是你,化学就是我;你我的消化系统是化学过程的场所……”,它告诉我们化学就在我们的身边:
(1)在氮气、氧气、二氧化碳等物质中:①可用于人工降雨的物质 (写化学式,下同)。②空气中含量最多的气体 。
(2)电解水时在水中加入少量氢氧化钠或稀硫酸,其作用是 。
(3)不同的火灾所采取的灭火方式不同。如扑灭森林火灾时可以采取的方法或原理是
;扑灭因电线老化而引起的 火灾时应先 ,再进行灭火。
(4分)右图是某品牌补铁剂的标签。请回答:
(1)富马酸亚铁颗粒为人体补充 元素,
(2)富马酸亚铁中C、H、Fe、O原子个数比为 。
(3)富马酸亚铁的相对分子质量为 。
(4)若每次服用1包该补铁剂,则摄入铁元素的质量为 mg(计算结果取整数)。
(3分)下列物质都可用于自来水的净化。
(1)高铁酸钾(化学式K2FeO4)集氧化、吸附、凝聚、杀菌功能于一体,目前被广泛应用于自来水净化处理领域。高铁酸钾中铁元素的化合价为 。
(2)在自来水的净化过程中需要用到活性炭,它的作用是 。
(3)漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为[Ca(ClO)2]。次氯酸钙可发生如下反应:Ca(ClO)2 + CO2+ X=CaCO3↓+2HClO,则X的化学式为 。
(3分)根据元素周期表的部分信息,回答下列问题:
| 1 H 氢 |
|
|
|
|
|
|
|
2 He 氦 |
| 3 Li 锂 |
4 Be 铍 |
|
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
| 11 Na 钠 |
12 Mg 镁 |
|
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
(1)由原子序数为8和13的两种元素组成的化合物是 (写化学式)。
(2)元素周期表同一横行元素的排列规律是:从左至右
(3)表中不同种元素最本质的区别是 (填序号):
A、质子数不同 B、中子数不同 C、相对原子质量不同
(8分)已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z之间有如下转化关系。请回答下列问题。
(1)写出X的化学式 ;
(2)写出②和④反应的化学方程式:
② ;④ ;
(3)“物质的组成与结构决定物质的性质”是重要的化学思想。气体X、Y都含有 元素和 元素,但它们的物理性质、化学性质都不同。请举出X、Y性质不同的一个例子 。
(8分)物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙在高温高压加催化剂的条件下合成丙。甲、乙、丙的微观示意图见下表。
| 物质 |
甲 |
乙 |
丙 |
 |
| 微观示意图 |
 |
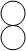 |
 |
(1)甲、乙、丙三种物质都是由(填“分子”、“原子”或“离子”) 构成的。
(2)甲、乙、丙中属于化合物的是(填序号) 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。
(4)写出甲和乙合成丙反应的化学方程式 。
(5)现用10g的甲和60g的乙混合反应制取丙,反应一段时间后,经测定剩余甲的质量为4g,则剩余乙的质量为 g。
(6)在生产丙的原料中,甲是用水与碳高温反应(将水蒸汽通过高温碳层,这种方法又称为水煤汽法)制得的,这个过程还生成另一种产物一氧化碳;请你根据信息写出该反应的化学方程式 。
(12分) 现有下列A、B、C、D、E五种实验装置,根据题意,将装置的序号填入下列空格中。
(1)写出指定仪器的名称:① ;② 。
(2)用高锰酸钾制取氧气,气体发生装置选用(填序号) ;用高锰酸钾制取氧气的化学方程式为 ;
(3)用C装置收集CO2时,检验CO2是否收集满的方法是 。
(4)用过氧化氢溶液制取氧气,气体发生装置选用(填序号) ;用过氧化氢溶液制取氧气的化学方程式为 。
(5)氨气(NH3)无色、有刺激性气味,极易溶于水,密度比空气小;实验室常用加热固体硫酸铵和固体氢氧化钙的混合物来制取氨气(在制得氨气的同时还生成了硫酸钙和水)。则氨气的制取和收集的装置是(填序号) ; 请你写出该反应的化学方程式 。
(10分)某校研究性学习小组用右图装置进行镁条在空气中燃烧的实验:将镁条燃烧、冷却后打开止水夹。
【发现问题】
进入集气瓶中水的体积约占集气瓶容积的30%。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积应不超过其容积的 %。可现进入集气瓶中水的体积约为其容积的30%,根据空气的组成,可推出减少的气体中一定有氮气,这种推测的理由是
。剩余约70%的气体主要成份是 。
【提出假设】镁条能与空气中的氮气发生化学反应。
【探究实验】
接着上述实验,先拿开装置中集气瓶的胶塞,然后迅速把点燃的镁条伸进含有剩余气体的集气瓶中。发现镁条能在余下的气体中剧烈燃烧。
【实验结论】根据上述探究实验,你得的结论是 。
【查阅资料】
①镁条在氮气中能燃烧并生成氮化镁(Mg3N2)固体。根据资料,氮化镁中氮元素的化合价 ,该反应的化学方程 。
②镁条除了能与氮气反应,还可以在二氧化碳气体中燃烧生成碳和氧化镁。请你写出该反应的化学方程式 。
【实验反思】通过以上探究,你对燃烧有了什么新的认识:
。(写出一点即可)。
(6分)肉毒碱又称维生素Bt,是一种类维生素,它的化学式为C7H15NO3,在哺乳动物的脂肪代谢和能量产生中起着重要作用,被认为是“最佳减肥营养素”。
请通过计算回答下列问题:
(1)肉毒碱是由 种元素组成,C、H、O元素的质量比为 。
(2)肉毒碱的相对分子质量为 。
(3)肉毒碱中氮元素质量分数为 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号