[湖北]2011-2012学年湖北省襄阳市高二下学期四校联考期中考试化学试卷
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A.SO2和SiO2 | B.CCl4和KCl | C.NaCl和HCl | D.CO2和H2O |
下列说法正确的是( )
| A.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| B.稀有气体形成的晶体属于分子晶体 |
| C.干冰升华时,分子内共价键会发生断裂 |
| D.金属晶体的熔点普遍都很高 |
关于晶体和非晶体的说法,正确的是( )
| A.晶体在三维空间里呈周期性有序排列,因此在各个不同的方向上具有相同的物理性质 |
| B.晶体在熔化过程中需要不断的吸热,温度不断地升高 |
| C.普通玻璃在各个不同的方向上力学、热学、电学、光学性质相同 |
| D.晶体和非晶体之间不可以相互转化 |
下列化合物,按其晶体的熔点由高到低排列正确的是( )
| A.SiO2 CaCl2 CBr4CF4 | B.SiO2CsCl CF4CBr4 |
| C.CsCl SiO2 CBr4CF4 | D.CF4CBr4CsCl SiO2 |
下列各项所述的数字不是6的是 ( )。
| A.在NaCl晶体中,与一个Na+ 最近的且距离相等的Cl- 的个数 |
| B.在金刚石晶体中,最小的环上的碳原子个数 |
| C.在二氧化硅晶体中,最小的环上的原子个数 |
| D.在石墨晶体的层状结构中,最小的环上的碳原子个数 |
下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤晶格能由大到小顺序:NaF> NaCl> NaBr>NaI
⑥ SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦分子晶体中分子间作用力越大,分子越稳定
A.①②③⑥ B.①②④ C.③⑤⑥⑦ D.③⑤
已知含氧酸可用通式XOm(OH)n来表示,如X是S,当m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸。下列各含氧酸中酸性最强的是( )
| A.HClO2 | B.H2SeO3 | C.H3BO3 | D.HMnO4 |
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120o,它能水解,有关叙述正确的是 ( )
| A.氯化硼液态时能导电而固态时不导电 | B.硼原子以sp杂化 |
| C.氯化硼遇水蒸气会产生白雾 | D.氯化硼分子属极性分子 |
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA |
B.1 mol甲基(—CH3)所含的电子总数为9NA |
C.0.5 摩1, 3-丁二烯分子中含有碳碳双键数为 NA |
D.1 mol碳正离子(CH3+ )所含的电子总数为8NA |
下列关于丙烯(CH3—CH=CH2)的说法错误的是( )
| A.丙烯分子有8个σ键,1个π键 | B.丙烯分子中3个碳原子都是sp3杂化 |
| C.丙烯分子存在非极性键 | D.丙烯分子中3个碳原子在同一平面上 |
手性分子是指在分子结构 中,当a、b、x、y为彼此互不相同的原子或原子团时,
中,当a、b、x、y为彼此互不相同的原子或原子团时,
称此分子为手性分子,中心碳原子为手性碳原子。下列分子中指定的碳原子(用*标记)
不属于手性碳原子的是( )
A.苹果酸  |
B.丙氨酸 |
C.葡萄糖 |
D.甘油醛 |
下列叙述正确的是( )
A.分子式为C3H6 的有机物最多存在3个碳碳单键,与C4H10 的碳碳单键数相同
B 和
和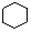 均是芳香烃,
均是芳香烃, 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
C. 和分子
和分子 组成相差一个—CH2—,因此是同系物关系
组成相差一个—CH2—,因此是同系物关系
D.分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推
测有机物结构简式为C2H5-OH
下列说法不正确的是( )
| A.用四氯化碳可以萃取乙酸水溶液中的乙酸 |
| B.元素分析可以鉴定有机物的实验式 |
| C.红外光谱分析可以鉴定有机物中含有的官能团或化学键 |
| D.核磁共振氢谱分析可以鉴定有机物中不同化学环境的氢原子及它们的数目比 |
有下列八种晶体:
| A.(水晶)SiO2 | B.冰醋酸 | C.氧化镁 | D.白磷 E.固体氩 |
F.氢氧化钠 G.铝 H.金刚石
用序号回答下列问题:
(1) 属于原子晶体的化合物是_________;晶体中含有氢键的是________。
(2) 由极性分子构成的晶体是_________;由正四面体形分子构成的晶体是____;
含有共价键的离子晶体是________。
(3) 在一定条件下能导电而不发生化学变化的是___________;晶体中只含有范德华
力一种作用的是___________;受热熔化需克服共价键的化合物是___________。
Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
| 元素 |
25Mn |
26Fe |
|
| 电离能/kJ·mol-1 |
I1 |
717 |
759 |
| I2 |
1509 |
1561 |
|
| I3 |
3248 |
2957 |
回答下列问题:
(1)Mn元素外围电子层的电子排布式为 ,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难。对此,你的解释是 。
(2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是 。
(3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为 晶体。
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为 。
(8分)⑴键线式 表示的分子式 ;名称是 。
表示的分子式 ;名称是 。
⑵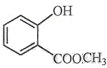 中含有的官能团的名称为 。
中含有的官能团的名称为 。
⑶用价层电子对互斥理论推测下列分子的空间构型:
SO2 ________; HCHO___________.
⑷重结晶的首要工作是选择适当的溶剂,要求该溶剂:
a.杂质在此溶剂中溶解度______________ 。
b.被提纯的物质在此溶剂中溶解度__________________。
乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全。有关物质的沸点见下:
| 物质 |
乙醛 |
乙酸 |
甘油 |
乙醇 |
水 |
| 沸点/℃ |
20.8 |
117.9 |
290 |
78.2 |
100 |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)
_________________________________________。
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温
度计水银球的位置应在________;当试管A内的主要反应完成后温度计水银球的位置应在_______。
(3)烧杯B内盛装的液体可以是_______。
(4)试管C中收集到的是粗产品,若想进一步提纯,可采用的方法是_____;
提纯后的产品若在质谱仪中进行测定,其质荷比最大是____(填数值);
若在核磁共振仪中进行测定,其核磁共振氢谱共有__种峰,峰面积之比为__。
已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如右图。 请回答:
请回答:
 (1)
(1) A与B形成的化合物在固态时的晶体类型是 ;A与B形成的化合物
A与B形成的化合物在固态时的晶体类型是 ;A与B形成的化合物
比A与C形成的化合物熔点要____(填高、低)
(2)
 写出C的单质与水反应的离子方程式 ;
写出C的单质与水反应的离子方程式 ;
(3)如图所示,D跟B形成的离子化合物的化学式为 ;鉴别该离子化合物是否为晶体,最可靠的科学方法是 ,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是 cm3(只要求列出算式)。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号