[北京]2012届北京市延庆县九年级上学期期末考试化学试卷
水是生命的基础,没有水就没有生命。下列有关水的说法正确的是
| A.水是由两个氢元素和一个氧元素组成 |
| B.无色、无嗅、清澈透明的水就是纯水 |
| C.婴幼儿、青少年长期饮用纯净水有益健康 |
| D.过滤可以将不溶于水的固体杂质与水分离 |
氢元素和氧元素的本质区别是其原子的
| A.质子数不同 | B.最外层电子数不同 |
| C.电子层数不同 | D.中子数不同 |
利用洗涤灵可以洗去餐具上的油污,这其中洗涤灵起到的作用是
| A.做乳化剂 | B.作溶剂 | C.作催化剂 | D.做溶质 |
下列化学方程式书写正确的是
| A.Na2CO3 + HCl="==" NaCl+H2O + CO2↑ | B.Mg + O2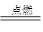 MgO2 MgO2 |
C.CH4 + 2O2 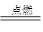 CO2 + 2H2O CO2 + 2H2O |
D.2Fe + 6HCl="==" 2FeCl3 |
有人通过闻茶的方法就能判断出茶的产地。人们能够闻到茶香的原因是
| A.分子在不断运动 | B.分子之间有间隔 |
| C.分子的质量和体积都很小 | D.分子是由原子构成的 |
化学知识中有很多的“相等”。请你判断下列说法中不正确的是
| A.溶液稀释前后,溶质的质量相等 |
| B.化合物中,元素正化合价数值等于负化合价数值 |
| C.50g水和50g酒精混合,所得溶液的质量等于100g |
| D.50mL的水和50mL的酒精混合,所得溶液的体积等于100mL |
打火机的主要燃料是丁烷(C4H10)。下列有关丁烷的说法不正确的是
| A.从性质上看:丁烷具有可燃性 |
| B.从变化上看:丁烷完全燃烧只生成水 |
| C.从组成上看:丁烷由碳、氢两种元素组成 |
| D.从结构上看:一个丁烷分子由4个碳原子和10个氢原子构成 |
实验室制取二氧化碳,下列做法可行的是
| A.用镊子夹取块状石灰石固体 |
| B.将鼻子凑到瓶口闻酸液的气味 |
| C.将用剩的酸液倒回原瓶 |
| D.用稀硫酸与块状石灰石反应制取二氧化碳 |
下列自救措施中不合理的是
| A.室内起火,不要急于打开所有门窗 |
| B.厨房燃气泄漏,不要立即打开抽油烟机 |
| C.在山林中遇到火灾时,向顺风方向奔跑,脱离火灾区 |
| D.火灾发生且烟雾较浓时,应用湿毛巾捂住口鼻,迅速逃离 |
为寻找常温下能加速过氧化氢分解的物质,并通过实验比较它们的效果,设计了下图所示的实验,在四组对比实验中,效果较差的是
| A.第一组同时实验,观察比较反应过程中两个气球体积的变化 |
| B.第二组同时实验,观察比较反应过程中两者产生气泡的快慢 |
| C.第三组分两次实验,看木条是否能复燃 |
| D.第四组分两次实验,比较收集一定体积的气体所需要的时间 |
在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 |
A |
B |
C |
D |
| 反应前质量/g |
4 |
6 |
111 |
4 |
| 反应后质量/g |
待测 |
15 |
0 |
84 |
下列说法正确的是
A.该反应的反应物为A和C B.容器中发生的化学反应属于化合反应
C.反应后,生成D的质量为84g D.反应后,待测A的质量为26g
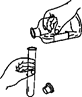
如图,小试管中盛放着固体乙(足量),滴管中有液体甲,广口瓶中有少量饱和的澄清石灰水(试管底部浸没在澄清石灰水中)。当把甲溶液滴加到乙中,过一会儿可看到石灰水变浑浊了,U形管中的a液面降低、b液面升高了。根据以上现象请你分析下列说法正确的是
| A.甲、乙一定分别是稀盐酸和大理石 |
| B.甲、乙有可能分别是水和硝酸铵 |
| C.石灰水变浑浊,一定是发生了化学变化 |
| D.石灰水变浑浊,有可能是发生了物理变化 |
关于“3CO2”的含义叙述正确的是
①表示二氧化碳这种物质 ②表示三个碳原子和六个氧原子
③表示三个二氧化碳分子 ④表示二氧化碳分子由一个碳原子和两个氧分子构成
⑤相对分子质量为132 ⑥碳原子与氧原子的质量比为3∶8
| A.③⑥ | B.②⑥ | C.①③④ | D.②⑤⑥ |
已知固体氯酸钾在加热条件下可以分解,生成氧气。如果用二氧化锰作催化剂则可以加快其分解速度。已知a为固体氯酸钾,b为混有少量二氧化锰的固体氯酸钾,且a和b的质量相等,当分别同时加热a和b至完全反应时,能正确表示生成氧气的质量随反应时间而变化的图像是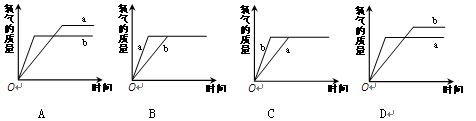
过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解。某100g30%的双氧水放置一段时间后,经实验测定其溶质质量分数变为25%,则分解掉的过氧化氢的质量是
A.5 g B.5.3 g C.5.67 g B.6.56g
水是人类生活中不可缺少的物质。
(1)下图①和②是两个简易净水装置。若对某河水水样进行初步净化:使用装置①时,应沿 慢慢向漏斗中倾倒河水,并注意液面始终要低于滤纸边缘;使用装置②时,活性炭的作用是 (填序号)。
A.沉淀 B.过滤 C.吸附 D.使硬水软化
(2)下图③是自然界水的循环示意。针对水蒸发过程的几点说法中,正确的是 (填序号)。
A.符合质量守恒定律 B.水的化学性质保持不变
C.水分子没有发生改变 D.水的物理性质保持不变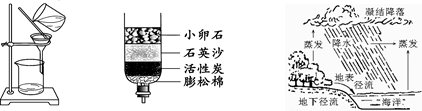
① ② ③
(3)水还有一个更广泛的应用,就是可以作溶剂,因为它可以溶解多种物质。常温下将25g食盐,放入100g水中,完全溶解,所得到的溶液中溶质质量分数是____________。若用该食盐溶液选种,将种子放入该食盐溶液中,则优良的种子应该处在溶液的________(填“上面”或“底部”)。
能源、环境问题是全球关注的热点问题。
(1)生活中经常使用的燃料有煤、 和天然气等化石燃料。
(2)化石燃料大量使用产生 、NO2等污染物,这些污染物在空气中反应后的生成物溶于雨水,会形成 ,破坏环境。
(3)“蜂窝煤”被加工成多孔形状的原因是 ,使其燃烧更充分。制作“蜂窝煤”时常加入生石灰(主要成分为氧化钙),其燃烧过程发生的部分化学反应如下:
①SO2 + CaO 高温 CaSO3, ②2CaSO3 + O2 高温 2CaSO4,
③2SO2 + O2 高温 2SO3, ④SO3 + CaO 高温 CaSO4。
从上述反应可知,在制作“蜂窝煤”时加入生石灰的作用是 。
(4)现阶段,人们大量利用燃料燃烧产生的能量。某校化学小组在研究燃烧的条件时,做了下图所示A、B、C三个实验。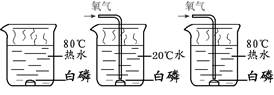

①上图所示白磷能够燃烧的实验是(填序号) , 反应的化学方程为 。
②对比实验B和C可以得到的结论是 。
右图是硝酸钾溶解度曲线。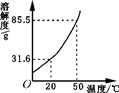
(1)硝酸钾溶液中的溶质是 。
(2)20℃时硝酸钾的溶解度比50℃时硝酸钾的溶解度________(填“大”或“小”)。
(3)欲将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采取的方法是 (写出一种即可)。
(4)小明在20℃时进行了如下实验,得到相应的溶液①~⑤,下列说法正确的是 。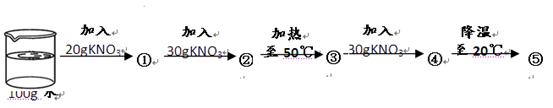
| A.④中溶质的质量分数最大 | B.②⑤中溶质的质量分数相等 |
| C.①③④中没有固体存在 | D.②④⑤的溶液为饱和溶液 |
物质丙是重要的化工产品,在国民经济中占有重要地位。工业上用甲和乙合成丙。甲、乙、丙的微观示意图见下表。
(1)直接构成甲的微粒是 。
(2)甲、乙、丙中属于化合物的是(填序号) 。
(3)已知物质丙中氢元素的化合价为+1,则另一种元素的化合价为 。
(4)甲和乙合成丙的反应中,甲、乙、丙的微粒个数比为 。该反应的基本反应类型为_______________________。
下列用字母表示的8种物质由H、C、O、Ca、Cl、Mn中的几种元素组成它们是初中化学常见的物质。
(1)A是大理石的主要成分,遇B溶液产生气泡,该反应的化学方程式为 。
(2)向D溶液中加入E会生成F和G,其中D、F组成元素相同。D的化学式为 ,G的化学式为 。
(3)向X中加入F,发生化合反应生成Y,X和Y含有相同的金属元素。该反应的化学方程式为 。
(4)从上述物质中任选2种为一组,按下图所示装置进行实验。将胶头滴管中的液体滴入瓶中,导管口处有气泡产生。写出符合要求的3组物质。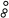 友情提示:填写物质的化学式、名称或俗称均可。
友情提示:填写物质的化学式、名称或俗称均可。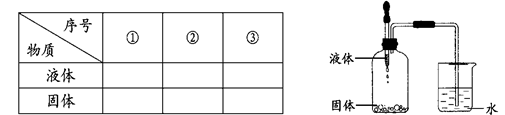
根据下图回答问题。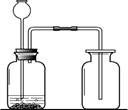

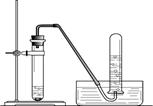
A B C
(1)仪器a的名称为 。
(2)加热高锰酸钾制取氧气的装置是 (填序号),反应的化学方程式为
。
(3)根据CO2的性质分析,制备二氧化碳气体的装置选用A而不选用C的原因是 、 。
(4)从上述制取气体的实验装置选择,我们得到的启发是,在选择制取气体的发生装置时,需要考虑的因素有 。
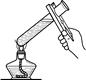
同学们在课外活动中设计了有关气体的实验。气体的发生装置如右图所示。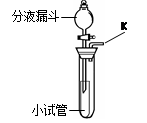
(1) 此装置可以用于制备气体气。若制备氧气,应在分液漏斗中盛放的药品是 ;该反应的化学方程式是 。
(2) 此装置还可以验证某气体的化学性质。若小试管中装有大理石,则分液漏斗中应放____________(填物质名称),大试管中应放的药品是________或_______,写出其中发生化合反应的化学方程式________________________。
(3) 在不改变此实验装置的基础上,同学们认为只要再增加一个操作,还可以验证该气体的其他化学性质。增加的操作是 。
同学在帮助老师整理实验室时,发现了半瓶久置的氢氧化钙粉末[Ca(OH)2],他们决定对这瓶氢氧化钙粉末的组成进行实验探究。
(1)提出问题:这瓶氢氧化钙是否已经变质?
(2)猜想与假设:该氢氧化钙粉末的成分为①氢氧化钙;②氢氧化钙、碳酸钙;③ 。
(3)设计方案、进行实验:请你参与探究,并填写下表。
| 实 验 步 骤 |
实验现象 |
实验结论 |
| ①取样品少量于小烧杯中,加入适量水,充分搅拌,过滤。 |
|
|
| ② 。 |
大量气泡产生 |
氢氧化钙已经变质。 |
| ③取少量滤液于试管中, 。 |
____________ |
氢氧化钙没有完全变质。 该反应的化学方程式为 。 |
(4)联想与启示:氢氧化钙变质是由于Ca(OH)2与空气中的 发生化学反应的缘故,因此氢氧化钙应 保存。
已知金属钠与水在常温下反应的化学方程式为:2Na + 2H2O="=2NaOH" + H2↑。
若要得到1 g氢气,需要金属钠多少克?
已知碳与氧化铜在高温时可同时发生两个反应且均生成红色固体。
(1)碳与氧化铜在高温时反应生成红色铜的化学方程式可表示为:
C + 2CuO 2Cu + CO2↑; 写出碳与氧化铜在高温时反应生成红色氧化亚铜(化学式为Cu2O)和二氧化碳的化学方程式__________________________________。
2Cu + CO2↑; 写出碳与氧化铜在高温时反应生成红色氧化亚铜(化学式为Cu2O)和二氧化碳的化学方程式__________________________________。
(2)现有碳和氧化铜组成的混合物3.12 g,在高温时充分反应。若反应后碳和氧化铜均无剩余且反应产生的气体全部被足量的澄清石灰水吸收,石灰水增重0.44 g。
① 反应前混合物中碳的质量为 g。
② 计算反应后固体混合物中氧化亚铜的质量。
(写出解题过程,计算结果保留两位小数)。



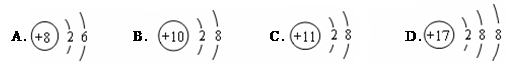
 粤公网安备 44130202000953号
粤公网安备 44130202000953号