[河南]2011-2012学年河南省偃师高中高一下学期第一次月考化学试卷
下列变化过程中,只破坏共价键的是 ( )
| A.I2升华 | B.NaCl颗粒被粉碎 |
| C.HCl溶于水得盐酸 | D.从NH4HCO3中闻到了刺激性气味 |
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为( )。
| A.HX | B.H2X | C.XH4 | D.XH3 |
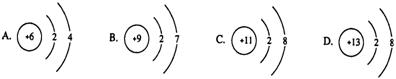
下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是 ( )。
| A.6和8 | B.11和13 | C.11和16 | D.12和17 |
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是( )。
A. |
B. |
C. |
D. |
下列各组顺序的排列不正确的是 ( )。
| A.离子半径:Na+ >Mg2+ >Al3+ >F- |
| B.热稳定性:HCl>H2S>PH3>AsH3 |
| C.酸性强弱: Al(OH)3<H4SiO4<H2CO3<H3PO4 |
| D.原子半径:K>Na>Mg |
下列离子中,所带电荷数与该离子的核外电子层数相等的是( )。
| A.Al3+ | B.Mg2+ | C.Be2+ | D.H+ |
下列事实,不能说明氯元素的非金属性比硫元素强的是( )。
| A.氯气与氢硫酸能发生置换反应 | B.HClO4酸性比H2SO4强 |
| C.盐酸是强酸,氢硫酸是弱酸 | D.受热时,氯化氢比硫化氢稳定 |
元素X的原子比元素Y的原子多一层电子,X、Y的单质都能与水激烈反应放出气体,所生成的两种气体混合点燃,会发生爆炸,X、Y形成的离子都与氖原子有相同的电子层结构,则X、Y可能是( )。
| A.Na和Cl | B.K和F | C.Na和F | D.Ca和Cl |
国际无机化学命名委员会在1989年作出决定,把长式周期表原先的主、副族及族号取消,从左到右改为第1~18列,碱金属族为第1列,稀有气体为第18列。按这个规定,下列说法不正确的是( )
| A.第15列元素的最高价氧化物为R2O5 |
| B.第2列元素中肯定没有非金属元素 |
| C.第17列元素的第一种元素无含氧酸 |
| D.第16、17列元素都是非金属元素 |
下列关于元素周期律的叙述正确的是
| A.随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 |
| B.随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 |
| C.随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 |
| D.元素性质的周期性变化是指原子核外电子排布、原子半径及元素主要化合价的周期性变化 |
居里夫人发现了放射性元素镭(Ra),因而获得诺贝尔化学奖,已知镭原子核内有88个质子,与Ca处于同一主族。下列说法不正确的是( )。
| A.镭位于周期表中第七周期IIA族 | B.镭的硫酸盐难溶于水 |
| C.镭的碳酸盐可溶于水 | D.镭的氢氧化物为强碱 |
Y元素最高正价与负价的绝对值之差是4;Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物( )。
| A.KCl | B.Na2S | C.Na2O | D.K2S |
下列说法中正确的是( )。
| A.在共价化合物中可能含有离子键,离子化合物中也可能存在共价键 |
| B.稀有气体分子是由稀有气体的原子组成的,故其中必含有共价键 |
| C.阳离子一定是金属离子, 阴离子一定只含有非金属元素 |
| D.在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀合金材料的元素 |
根据表1信息,判断以下叙述正确的是 ( )
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、—2 |
—2 |
A.氢化物的沸点为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
甲、乙两种非金属:①甲比乙容易与H2化合;②甲原子能与乙阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。能说明甲比乙的非金属性强的是( )。
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |
24.已知自然界氧的同位素有16O、17O、18O,氢的同位素有 H、D,从水分子的原子组成来看,自然界的水一共有 ( )
A 3种 B 6种 C 9种 D 12种
右图为短周期的一部分,推断关于Y、Z、M的说法正确的是 ( )
| |
X |
|
| |
Y |
|
| Z |
M |
|
A.非金属性:Y> Z
B.ZM2分子各原子最外层均满足8e-稳定结构
C.原子半径:M>Z>Y
D.Y离子的结构示意图可表示为:
①在实验室里,要证明钠、镁、铝的金属性依次减弱的实验,除钠、镁、铝以外,还需的试剂为_________________________。
②在实验室里,要做证明Cl、Br、I的非金属性依次减弱的实验,所需的试剂除:NaCl溶液,NaBr溶液,KI溶液外,还需要的试剂为____________________。
反应的离子方程式为:_______________________________________________________
__________ ______________ __________________
________ ____
在原子序数1—18号的元素中:
(1)与水反应最剧烈的金属是_________ ____。 (2)阳离子半径最大的是_____________。
(3)原子半径最小的元素是____ __。 (4)气态氢化物水溶液呈碱性的元素是_______。
(5)气态氢化物最稳定的化学式是________。
(6)最高价氧化物对应水化物的酸性最强的酸是_____________。
在Na2S、KOH、CH4、Cl2、Na2O2、H2O2、NH4Cl中,只含有离子键的是__________,只含有极性键的是__________,含有非极性键的是__________,既含有离子键又有共价键的是______________________
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:
A ,B ,C ,D ,E
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
。
(3)写出A、B两元素相互反应的化学方程式:
。
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)
。
有A、B、C、D、E五种微粒,其组成均有氢元素,且电子总数为10个,A是双原子的阴离子,它们之间能发生下列变化:
(1)A+B C+D↑ (2)C+C
C+D↑ (2)C+C A+E (3)D+E
A+E (3)D+E B+C
B+C
由此可知它们的化学式分别为:
A ,B ,
C ,D ,E 。
下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ______,⑦ __ __。
(2)在①~(12)元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是____。(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)第三周期中原子半径最大的元素是 ,跟它与⑦元素可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: 。
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,请用电子式表示其化合物: .

 粤公网安备 44130202000953号
粤公网安备 44130202000953号